Punjab State Board PSEB 10th Class Science Important Questions Chapter 1 रासायनिक अभिक्रियाएँ एवं समीकरण Important Questions and Answers.
PSEB 10th Class Science Important Questions Chapter 1 रासायनिक अभिक्रियाएँ एवं समीकरण
दीर्घ उत्तरात्मक प्रश्न (Long Answer Type Questions)
प्रश्न 1.
संतुलित रासायनिक समीकरण को किस प्रकार लिखा जाता है ? इसके विभिन्न चरणों का वर्णन कीजिए।
उत्तर-
संतुलित रासायनिक समीकरण को लिखने के तरीके के बारे में जानने के लिए एक उदाहरण लेते हैं।
जिंक + सल्फ्यूरिक अम्ल → जिंक सल्फेट + हाइड्रोजन इस समीकरण को निम्नलिखित रासायनिक समीकरण से प्रकट किया जा सकता है।
Zn + H2 SO4 → ZnSO4 + H2
तीर के निशान के दोनों ओर के तत्वों के परमाणुओं की संख्या की जांच कर लें।
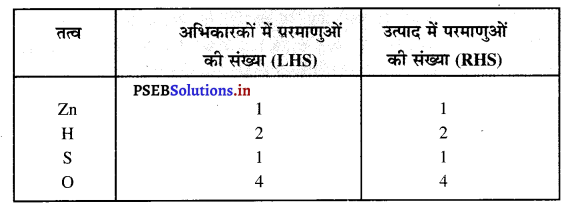
समीकरण में, तीर के चिह्न के दोनों तरफ के प्रत्येक तत्व के परमाणुओं की संख्या बराबर है इसलिए यह एक संतुलित रासायनिक समीकरण है। अब निम्नलिखित रासायनिक समीकरण को संतुलित करने का प्रयत्न करते हैं
Fe + H2O → Fe3O4 + H2
चरण 1. रासायनिक समीकरण को संतुलित करने के लिए सबसे पहले प्रत्येक सूत्र के चारों ओर एक बॉक्स बना लें। समीकरण को संतुलित करते समय बॉक्स के अंदर कुछ भी बदलाव न करें।
Fe + H2O → Fe3O4 + H2
चरण 2.
असंतुलित समीकरण में उपस्थित विभिन्न तत्वों के परमाणुओं की संख्या की सूची बनाइए-

चरण 3. सबसे अधिक परमाणु वाले यौगिक को पहले संतुलित करें चाहे वह अभिकारक हो या उत्पाद। उस यौगिक में सबसे अधिक परमाणु वाले तत्व को चुन लें। इस आधार पर हम Fe3O4, और उसके ऑक्सीजन तत्व को चुन लेते हैं। दायीं ओर ऑक्सीजन के चार परमाणु हैं और बायीं ओर केवल एक।
ऑक्सीजन परमाणु को संतुलित करने के लिए-
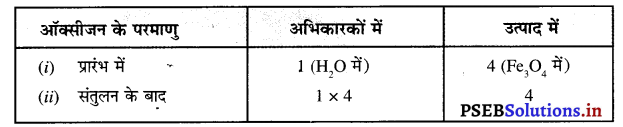
परमाणुओं की संख्या को बराबर करने के लिए हम अभिक्रिया में शामिल तत्वों तथा यौगिकों के सूत्रों को नहीं बदल सकते हैं। जैसे-ऑक्सीजन परमाणु को संतुलित करने के लिए हम ‘4’ गुणांक लगाकर 4H2O लिख सकते हैं लेकिन H2O4 या (H2O4) या (H2O)4 नहीं। आंशिक रूप से संतुलित समीकरण अब इस प्रकार होगा
Fe + 4 H2O → Fe3O4 + H2 (आंशिक रूप से संतुलित समीकरण)
चरण 4. Fe तथा H परमाणु अब भी असंतुलित हैं। इनमें किसी एक तत्व को चुनकर आगे बढ़ते हैं। हाइड्रोजन परमाणु को बराबर करने के लिए दायीं ओर हाइड्रोजन अणु की संख्या को ‘4’ कर देते हैं।

अब समीकरण इस प्रकार होगा
Fe + 4 H2O → Fe3O4 + 4H2
![]()
चरण 5. ऊपर दिए समीकरण की जांच करें तथा तीसरा तत्व चुन लें जो अब तक असंतुलित है। आप पाएंगे कि केवल लोहा ही एक तत्व है, जिसे संतुलित करना शेष है।

Fe को संतुलित करने के लिए बायीं ओर हम Fe के 3 परमाणु लेते हैं।
3 Fe + 4 H2O → Fe3O4 + 4H2
चरण 6. अंत में, इस संतुलित समीकरण की जाँच के लिए समीकरण में दोनों ओर के तत्वों के परमाणुओं की संख्या की गिनती करते हैं।
3 Fe + 4H2O → Fe3O4+4 H2
(संतुलित समीकरण) समीकरण में दोनों ओर के तत्वों के परमाणुओं की संख्या बराबर है। अतः यह समीकरण अब संतुलित है। रासायनिक समीकरणों को संतुलित करने की इस विधि को हिट एंड ट्रायल विधि कहते हैं क्योंकि सबसे छोटी पूर्णांक संख्या के गुणांक का उपयोग करके समीकरण को सुंतलित करने का प्रयत्न करते हैं।
चरण 7.
भौतिक अवस्थाओं के संकेत लिखना-ऊपर लिखे संतुलित समीकरण में भौतिक अवस्था की कोई जानकारी नहीं है।
रासायनिक समीकरण को अधिक सूचनापूर्ण बनाने के लिए अभिकारकों तथा उत्पादों के रासायनिक सूत्र के साथ उनकी भौतिक अवस्था को भी दर्शाया जाता है। अभिकारकों तथा उत्पादों के ठोस, गैस, द्रव तथा जलीय अवस्थाओं को क्रमशः (s), (g), (l) तथा (aq) से दर्शाया जाता है। अभिकारक या उत्पादों जब जल में घोल के रूप में उपस्थित रहता है तब (aq) लिखते हैं। अतः संतुलित समीकरण इस प्रकार होगा
3Fe(s) + 4H2O (g) → Fe3O4 (S) + 4H2(g)
प्रश्न 2.
रासायनिक अभिक्रियाओं के प्रकार उदाहरण सहित लिखो।
उत्तर-
रासायनिक अभिक्रिया के दौरान किसी एक तत्व का परमाणु दूसरे तत्व के परमाणु में नहीं बदलता है। न ही कोई परमाणु मिश्रण से बाहर जाता है या बाहर से मिश्रण में आता है। वास्तव में, किसी रासायनिक अभिक्रिया में परमाणुओं के आपसी आबंध के टूटने और जुड़ने से नए पदार्थों का निर्माण होता है।
1. संयुक्त अभिक्रिया-ऐसी अभिक्रिया जिसमें दो या दो से अधिक अभिकारक मिलकर एकल उत्पाद का निर्माण करते हैं उसे संयुक्त अभिक्रिया कहते हैं। जैसे-कैल्सियम ऑक्साइड जल के साथ तीव्रता से अभिक्रिया करके बुझे हुए चूने (कैल्सियम हाइड्रोक्साइड) का निर्माण करके अत्यधिक मात्रा में ऊष्मा उत्पन्न करता है।
उदाहरण –
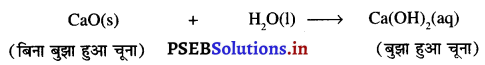
इस अभिक्रिया में कैल्सियम ऑक्साइड तथा जल मिलकर एकल उत्पाद, कैल्सियम हाइड्रोक्साइड बनाते हैं।
2. वियोजन अभिक्रिया-वह अभिक्रिया जिसमें कोई यौगिक दो या दो से अधिक सरल पदार्थों में टूटता है उसे वियोजन अभिक्रिया कहते हैं।
उदाहरण –

3. विस्थापन अभिक्रिया-जब कोई तत्व दूसरे तत्व को उसके यौगिक से विस्थापित कर देता है तो वह विस्थापन अभिक्रिया होती है।
उदाहरण
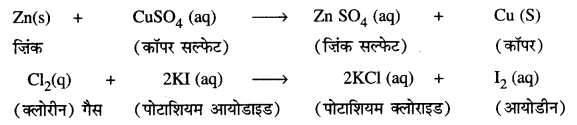
4. द्विविस्थापन अभिक्रिया-द्विविस्थापन अभिक्रिया में दो अलग-अलग परमाणु या परमाणुओं के समूह का आपस में आदान-प्रदान होता है।
उदाहरण –
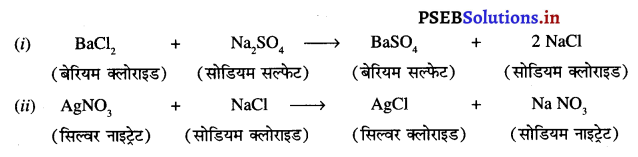
प्रश्न 3.
उपचयन एवं अपचयन की उदाहरण सहित संक्षेप में व्याख्या कीजिए
उत्तर-
उपचयन तथा अपचयन-किसी अभिक्रिया में पदार्थ का उपचयन तब होता है जब उसमें ऑक्सीजन की वृद्धि या हाइड्रोजन का ह्रास होता है इसके विपरीत पदार्थ का अपचयन तब होता है जब उसमें ऑक्सीजन का ह्रास या हाइड्रोजन की वृद्धि होती है।
उदाहरण-
कॉपर चूर्ण के सतह पर कॉपर ऑक्साइड (II) की काली परत चढ़ जाती है। यह काला पदार्थ क्यों बना? यह कॉपर ऑक्साइड कॉपर में ऑक्सीजन के योग से बना है।
![]()
यदि इस गर्म पदार्थ के ऊपर हाइड्रोजन गैस प्रवाहित की जाए तो सतह की काली परत भूरे रंग की हो जाती है क्योंकि इस स्थिति में विपरीत अभिक्रिया होती है तथा कॉपर प्राप्त होता है।
![]()
अभिक्रिया के दौरान जब किसी पदार्थ में ऑक्सीजन की वृद्धि होती है तो कहते हैं कि उसका उपचयन हुआ है और जब अभिक्रिया में किसी पदार्थ में ऑक्सीजन का ह्रास होता है तो कहते हैं कि उसका अपचयन हुआ है।
अभिक्रिया में कॉपर (II) ऑक्साइड में ऑक्सीजन का ह्रास हो रहा है, इसलिए यह अपचयित हुआ है। हाइड्रोजन में ऑक्सीजन की वृद्धि हो रही है, इसलिए यह उपचयित हुआ है। अर्थात्, किसी अभिक्रिया में एक अभिकारक उपचयित तथा दूसरा अभिकारक अपचयित होता है। इन अभिक्रियाओं को उपचयन-अपचयन अथवा रेडॉक्स अभिक्रिया कहते हैं।
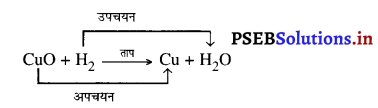
रेडॉक्स अभिक्रिया के कुछ अन्य उदाहरण हैं
ZnO+C → Zn + CO
MnO2 + 4HCl→ MnCl2 + 2H2O + Cl2
अभिक्रिया में कार्बन उपचयित होकर CO तथा ZnO अपचयित होकर Zn बनता है। अभिक्रिया में HCl, Cl2 में उपचयित तथा MnO2, MnCl2 में अपचयित हुआ है।
प्रश्न 4.
अम्ल क्या होता है ? अम्लों के चार गुणों की व्याख्या उदाहरण देकर करो।
उत्तर-
अम्ल-ऐसे यौगिक जिनमें एक अथवा एक से अधिक हाइड्रोजन परमाणु उपस्थित होते हैं तथा वह जल में घुलकर आवेशित हाइड्रोनियम आयन (H3O+) बनाते हैं, अम्ल कहलाते हैं। अम्लों का स्वाद खट्टा होता है।
अम्लों के गुण-
1. धातुओं के साथ क्रिया-अम्ल क्रियाशील धातुएं जैसे जिंक, मैग्नीशियम,लोहा तथा मैंग्नीज़ के साथ क्रिया करके हाइड्रोजन गैस पैदा करती हैं।
Zn(s) + तनु H2SO4(aq) → ZnSO4(aq) + H2(g) ↑
Mg(s) + तनु 2HCl (aq) → MgCl(aq) + H2(g) ↑
2. धात्विक कार्बोनेट तथा धात्विक बाइकार्बोनेट के साथ क्रिया-अम्ल, धात्विक कार्बोनेट तथा धात्विक बाइकार्बोनेट से क्रिया करके कार्बनडाइऑक्साइड गैस उत्सर्जित करते हैं।
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2↑
NaHCO3 +HCl → NaCl + H2O + CO2 ↑
3. शारों के साथ क्रिया-अम्ल, क्षारों के साथ क्रिया करके उदासीनीकरण प्रक्रिया दर्शाते हैं तथा लवण और जल पैदा करते हैं।
HCl + NaOH → NaCl + H2O
HCl + KOH → KCl + H2O
4. धात्विक सल्फाइड तथा हाइड्रोजन सल्फाइड के साथ क्रिया-अम्ल विभिन्न धातु सल्फाइडों तथा हाइड्रोदन सल्फाइडों के साथ क्रिया करके H2S गैस उत्पन्न करते हैं।
FeS + H2SO4→ FeSO4 + H2S(g)
2KHS + 2HCl → 2KCl + 2H2S(g)
प्रश्न 5.
चित्र में किस प्रकार की रासायनिक क्रिया दर्शायी गई है ? इस क्रिया की परिभाषा उदाहरण सहित लिखो।
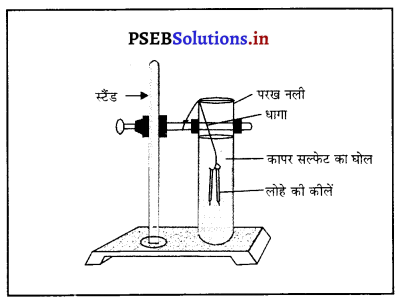
उत्तर-
चित्र में धातुओं की लवणों के विलयनों के साथ अभिक्रिया दर्शाई गई है। यह विस्थापन अभिक्रिया है। विस्थापन अभिकिया जब कोई तत्व दूसरे तत्व को उसके यौगिक से विस्थापित कर देता है तो वह विस्थापन अभिक्रिया होती है।
उदाहरण –

![]()
लघु उत्तरात्मक प्रश्न (Short Answer Type Questions)
प्रश्न 1.
रासायनिक समीकरणों को लिखते समय किन-किन बातों का ध्यान रखना आवश्यक होता है ?
उत्तर-
- रासायनिक परिवर्तन को प्रदर्शित करना।
- अभिकारकों और उत्पादों के सभी तत्वों को प्रतीकों से दर्शाना।
- अभिकारकों और उत्पादों के प्रत्येक तत्व के कुल परिणामों की संख्या का दोनों ओर समान होना।
- भौतिक अवस्था, ऊष्मा और परिस्थितियों को स्पष्ट करना।
प्रश्न 2.
संयुक्त अभिक्रिया की परिभाषा उदाहरण सहित समझाइए।
उत्तर-
संयुक्त अभिक्रिया- ऐसी अभिक्रिया जिसमें दो या दो से अधिक अभिकारक मिलकर एकल उत्पाद का निर्माण करते हैं उसे संयुक्त अभिक्रिया कहते हैं।
उदाहरण-

प्रश्न 3.
बुझे हुए चूने का रासायनिक सूत्र और उसका एक उपयोग बताइए।
उत्तर-
रासायनिक सूत्र → Ca(OH)2
बुझे हुए चूने के विलयन का उपयोग दीवारों की सफ़ेदी करने के लिए होता है।
प्रश्न 4.
सफेदी करने के दो-तीन दिन बाद चमक क्यों आ जाती है?
उत्तर-
कैल्सियम हाइड्रोक्साइड वायु में उपस्थित कार्बन डाइऑक्साइड के साथ धीमी गति से अभिक्रिया करके दीवारों पर कैल्सियम कार्बोनेट की एक पतली परत बना देता है। सफ़ेदी करने के दो-तीन दिन बाद कैल्सियम कार्बोनेट का निर्माण होता है और इससे दीवारों पर चमक आ जाती है।
प्रश्न 5.
संगमरमर का रासायनिक सूत्र तथा उसके बनने की अभिक्रिया बताइए।
उत्तर-
संगमरमर को कैल्सियम कार्बोनेट भी कहते हैं। इसका रासायनिक सूत्र है-CaCO3
इसके बनने की अभिक्रिया –
Ca(OH2) (aq) + CO2(g) → CaCO3(s) + H2O कैल्सियम कार्बोनेट
प्रश्न 6.
ऊष्माक्षेपी अभिक्रिया की परिभाषा तथा दो उदाहरण दीजिए।
उत्तर-
ऊष्माक्षेपी अभिक्रिया (Exothermic Reaction)-जिन अभिक्रियाओं में उत्पाद के निर्माण के साथ-साथ ऊष्मा भी उत्पन्न होती है उन्हें ऊष्माक्षेपी रासायनिक अभिक्रिया कहते हैं। A + B→ C + D + ऊष्मा इन अभिक्रियाओं में अभिकारकों की कुल ऊर्जा उत्पादों की कुल ऊर्जा से अधिक होती है। अभिकारकों की ऊर्जा > उत्पादों की ऊर्जा ऊष्माक्षेपी अभिक्रियाओं के कुछ अन्य उदाहरण हैं –
- प्राकृतिक गैस का दहन –
CH4 (g) + 2O2 (g) → CO2(g) + 2H2O (g) + ऊर्जा - साग-सब्जियों का विघटित होकर कंपोस्ट बनाना भी ऊष्माक्षेपी अभिक्रिया का ही उदाहरण है।
प्रश्न 7.
ऊष्माशोषी अभिक्रियाओं की उदाहरण सहित परिभाषा दीजिए।
उत्तर-
ऊष्माशोषी अभिक्रिया (Endothermic Reaction)-जिन अभिक्रियाओं में ऊष्मा का अवशोषण होता है उन्हें ऊष्माशोषी अभिक्रियाएं कहते हैं।
A+ B + ऊष्मा →C+ D
इस अभिक्रिया में अभिकारकों की कुल ऊर्जा उत्पादों की कुल ऊर्जा से कम होती है। अभिकारकों की ऊर्जा < उत्पादों की ऊर्जा उदाहरण –
- कोक की भाप के साथ अभिक्रिया
C(s) + H2O (g) + ऊष्मा → CO(g) + H2 (g) - N2 और O2 की प्रक्रिया
N2(g) + O2 (g) + ऊष्मा → 2 NO (g)
![]()
प्रश्न 8.
वियोजन अभिक्रिया संयोजन अभिक्रिया से किस प्रकार अलग है?
उत्तर-
संयोजन अभिक्रिया में दो या दो से अधिक पदार्थ मिलकर एक नया पदार्थ बनाते हैं जबकि वियोजन अभिक्रिया इसके विपरीत है। वियोजन अभिक्रिया में एकल पदार्थ वियोजित होकर दो या दो से अधिक पदार्थ प्रदान करता है।
प्रश्न 9.
विस्थापन अभिक्रिया की परिभाषा तथा उदाहरण दीजिए।
उत्तर-
विस्थापन अभिक्रिया-जब कोई तत्व किसी दूसरे तत्व को उसके यौगिक से विस्थापित कर देता है तो वह विस्थापन अभिक्रिया होती है।

उपरोक्त उदाहरण में Zn कॉपर से ज्यादा क्रियाशील है इसलिए वह कॉपर सल्फेट से कॉपर का विस्थापन करके स्वयं सल्फेट के साथ जिंक सल्फेट बनाता है।
प्रश्न 10.
द्विविस्थापन अभिक्रिया की परिभाषा तथा उदाहरण दीजिए।
उत्तर-
द्विविस्थापन अभिक्रिया-वैसी अभिक्रियाएं जिनमें अभिकारकों के बीच आयनों का आदान-प्रदान होता है उन्हें द्विविस्थापन अभिक्रिया कहते हैं।
उदाहरण

उपरोक्त अभिक्रिया में Cl- तथा SO42- आयनों का आदान-प्रदान हो रहा है इसलिए यह द्विविस्थापन अभिक्रिया का उदाहरण है।
प्रश्न 11.

उपरोक्त अभिक्रिया को पूरा करें तथा उत्पाद का रंग भी बताइए।
उत्तर-
उपरोक्त अभिक्रिया है-

यह उत्पाद Pbo पीले रंग का है।
प्रश्न 12.
जंग लगना किसे कहते हैं ? जंग का रासायनिक सूत्र लिखिए। इससे होने वाली हानि क्या है?
उत्तर-
लोहे की बनी नई वस्तुएँ चमकीली होती हैं लेकिन कुछ समय पश्चात् उन पर लालिमा युक्त भूरे रंग की परत चढ़ जाती है। आमतौर पर इस प्रक्रिया को लोहे पर जंग लगना कहते हैं। कॉपर जंग का रासायनिक सूत्र है : Fe2SO3. x H2O जंग हाइड्रेटेड आयरन (III) ऑक्साइड है। यह भंगुर है और समय के साथ धातु की सतह से पृथक् होता रहता है जिस कारण लोहे से बनी वस्तुएं क्षतिग्रस्त होती रहती हैं।
प्रश्न 13.
क्या होता है जब जिंक की छड़ कॉपर सल्फेट के विलयन में रखी जाती है? अभिक्रिया का रासायनिक समीकरण दीजिए।
उत्तर-
जिंक कॉपर से अधिक अभिक्रियाशील है। वह कॉपर सल्फेट विलयन से कॉपर को विस्थापित कर देता है, और जिंक सल्फेट बनता है। कॉपर सल्फेट का नीला विलयन धीरे-धीरे सफेद होता चला जाता है।
![]()
प्रश्न 14.
‘चूना शमन’ का तात्पर्य क्या होता है? इस प्रक्रिया में सूं-सूं की ध्वनि क्यों होती है? संबंधित अभिक्रिया को प्रदर्शित करने वाली रासायनिक समीकरण लिखिए।
उत्तर-
चूना शमन-जब चूने में जल मिलाया जाता है, यह बुझे चूने में बदल जाता है। इसे चूना शमन कहते हैं। यह एक उष्मापेक्षी अभिक्रिया है जिसमें उष्मा बाहर निकलती है जिसके कारण सूं-सूं की ध्वनि उत्पन्न होती है।

प्रश्न 15.
निम्नलिखित रासायनिक समीकरणों को संतुलित कीजिए
(i) H2 + N2 → NH3
(ii) BaCl2 + Al2(SO4)3 → AlCl3 + 3BaSO4
(iii) H2S + O2 → SO2 + H2O
(iv) KBr + BaI2 → KI + BaBr2
(v) Al + CuCl2 → AICl3 + Cu
(vi) AgNO3 + Cu2 + → Cu(NO3)2 + Ag
(vii) AI (OH)3 → Al2O3+ H2O
(viii) NH3 + CuO → Cu + N2 + H2O
(ix) KClO3 → KCl+ O2
(x) KNO2 → KNO2 + O2
(xi) BaCl2 + K2SO4 → + BaSO4 + KCl.
उत्तर-
(i) 3H2 + N2 → 2NH3
(ii) 3BaCl2 + Al2(SO4)2 → 2Alcl3 + 3BaSO4
(iii) 2H2S + 3O2 → 2SO2 + 2H2O
(iv) 2KBr + Bal2 → 2KI + BaBr2
(v) 2Al + 3CuCl2 → 2AlCl3 + 3Cu
(vi) 2AgNO3 + Cu → Cu (NO3)2 + 2Ag
(vii) 2AI (OH)3 → AlO3 + 3H2O
(viii) 2NH2 + 3CuO → Cu + N2 + 3H2O
(ix) 2KCIO3 → 2KCl + 3O2
(x) 2KNO3 → 2KNO2 + O2
(xi) BaCl2 + K2SO4 → BaSO4 + 2KCl.
प्रश्न 16.
निम्न समीकरणों में उपचयित और अपचयित पदार्थों के नाम लिखिए
(i) SO2 + 2H2S → 2H2O+ 3S
(ii) 2Al + 3HCl → 2AlCl3 + 3H2
(iii) 2H2S + SO2 → 3S + 2H2O
(iv) Zn + 2AgNO3 → Zn (NO3)2 + 2Ag
(v) H2 + CuO → Cu + H2O.
उत्तर-
(i) SO2 में S का अपचयन तथा H2S में S का उपचयन हुआ।
(ii) एलुमीनियम उपचयित तथा क्लोरीन अपचयित हुआ।
(iii) हाइड्रोजन का उपचयन हुआ और सल्फर का अपचयन हुआ।
(iv) जिंक का उपचयन हुआ और सिल्वर का अपचयन हुआ।
(v) हाइड्रोजन का उपचयन हुआ तथा तांबा का अपचयन हुआ।
प्रश्न 17.
निम्नलिखित क्रियाओं के लिए संकेतों और सूत्रों द्वारा संतुलित रासायनिक समीकरण लिखो :
(i) जिंक + सिल्वर नाइट्रेट → जिंक नाइट्रेट + सिल्वर
(ii) कॉपर ऑक्साइड + हाइड्रोजन → कॉपर + पानी
(ii) बेरियम क्लोराइड + एल्युमीनियम सल्फेट → बेरियम सल्फेट + एल्युमीनियम क्लोराइड।
उत्तर-
(i) Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
(ii) CuO + H2 → Cu + H2O
(iii) 3BaCl2 + Al2(SO4)3 → 3BaSO4 + 2AlCl3
प्रश्न 18.
निम्नलिखित समीकरणों को पूरा करें :
(i) कैल्सियम हाइड्रॉक्साइड + कार्बनडाइऑक्साइड → ………………….. +
(ii) सोडियम + पानी → …………………………….. + ………………………………
(iii) हाइड्रोजन + क्लोरीन → …………………………….
उत्तर –
(i) कैल्सियम + कार्बनडाइऑक्साइड → कैल्सियम कार्बोनेट + पानी हाइड्रॉक्साइड
(ii) सोडियम + पानी → सोडियम हाइड्रॉक्साइड + हाइड्रोजन
(iii) हाइड्रोजन + क्लोरीन → हाइड्रोजन क्लोराइड गैस
![]()
प्रश्न 19.
निम्नलिखित कथनों को रासायनिक समीकरणों (सूत्रों सहित ) में लिखकर संतुलित करो :
(i) पोटाशियम धातु जल के साथ अभिक्रिया करके पोटाशियम हाइड्रॉक्साइड और हाइड्रोजन गैस देती है।
(ii) हाइड्रोजन सल्फाइड गैस का वायु/ऑक्सीजन में दहन होने पर जल एवं सल्फर डाइऑक्साइड गैस बनाती है।
(ii) हाइड्रोजन गैस नाइट्रोजन से संयोग करके अमोनिया बनाती है। (P.S.E.B. March 2017, Set-III)
उत्तर
(i) 2K + 2H2O → 2KOH + H2
(ii) 2H2S + 3O2 → 2H2O + 2SO2
(iii) 3H2 + N2 → 2NH3
प्रश्न 20.
नीचे दिए गए फ्लास्क में किस प्रकार की रासायनिक अभिक्रिया हो रही है ? इसके लिए रासायनिक समीकरण लिखें। उत्पन्न हो रही गैस का नाम एवं एक गुण भी लिखें।
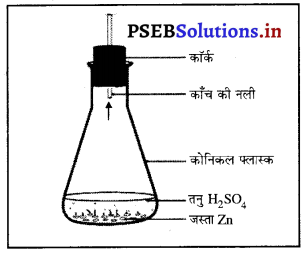
उत्तर-
रासायनिक समीकरण

इस अभिक्रिया में हाइड्रोजन गैस उत्पन्न हो रही है।
हाईड्रोजन गैस का गुण-हाईड्रोजन गैस एक ज्वलनशील गैस है जो नीली-पीली ज्वाला के साथ धमाके के साथ जलती है।
प्रश्न 21.
सामने चित्र में दिखाई गई परखनली में रासायनिक अभिक्रिया के दौरान कौन-सी गैस पैदा हो रही है ? यह गैस चूने के पानी/कैल्शियम हाइड्रॉक्साइड से किस तरह क्रिया करती है ?
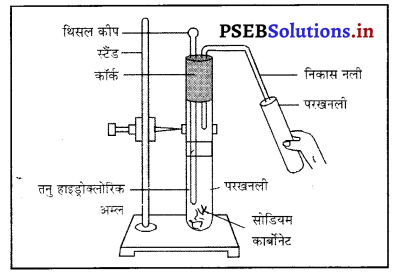
उत्तर-
- सोडियम कार्बोनेट तथा तनु हाइड्रोक्लोरिक की क्रिया के दौरान कार्बनडाइऑक्साइड गैस पैदा होती है।
- कार्बनडाइऑक्साड गैस चूने के पानी (कैल्शियम हाइड्राक्साइड) के साथ क्रिया करके सफेद रंग का कैल्शियम कार्बोनेट बनाती है जिससे चूने के पानी का रंग दुधिया हो जाता है।
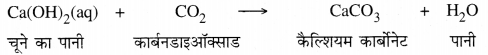
प्रश्न 22.
सामने दिए गये चित्र में दर्शाई परखनली में हो रही रासायनिक क्रिया को समीकरण के रूप में लिखो। घोल/विलयन के रंग में किस प्रकार परिवर्तन होता है ? लोहे की कीलों के रंग में क्या परिवर्तन होता है ?
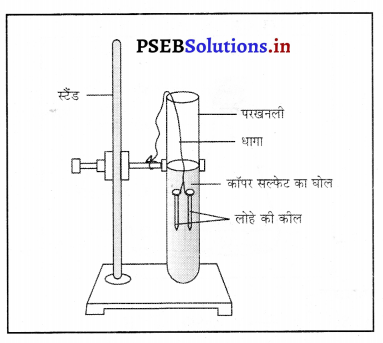
उत्तर-
रासायनिक क्रिया का समीकरण :

जब लोहे की कीलों को कॉपर सल्फेट के घोल मे डुबोया जाता है तो नीले रंग का घोल धीरे-धीरे फीका हो जाता है तथा कीलों का रंग भूरा हो जाता है।
अति लघु उत्तरात्मक प्रश्न (Very Short Answer Type Questions)
प्रश्न 1.
बुझे हुए चूने का एक उपयोग बताइए।
उत्तर-
दीवारों की सफ़ेदी करने के लिए।
प्रश्न 2.
संगमरमर का रासायनिक फार्मूला लिखिए।
उत्तर-
CaCO3.
प्रश्न 3.
प्राकृतिक गैस का दहन करने पर क्या प्राप्त होता है ?
उत्तर-
CO2 H2O और ऊर्जा ।
प्रश्न 4.
फ़ेरस सल्फेट का सूत्र लिखिए।
उत्तर-
FeSO4.7H2O
![]()
प्रश्न 5.
तैलीय तथा वसायुक्त खाद्य सामग्री जब लंबे समय तक रखी रह जाती है तो उसमें स्वाद और गंध किस क्रिया के कारण बदल जाते हैं ?
उत्तर-
उपचयन के कारण।
प्रश्न 6.
चिप्स बनाने वाले चिप्स की थैली में क्या युक्त कर देते हैं ताकि उनमें उपचयन न हो सके?
उत्तर-
नाइट्रोजन गैस।
प्रश्न 7.
किसी अभिक्रिया में पदार्थ का उपचयन कब होता है?
उत्तर-
जब O2 की वृद्धि या H2 का ह्रास होता है।
प्रश्न 8.
ऊष्मा देने पर कैल्सियम कार्बोनेट किसमें नियोजित होता है ?
उत्तर-
कैल्सियम ऑक्साइड तथा कार्बन डाइऑक्साइड ।
प्रश्न 9.
बुझे हुए चूने का रासायनिक सूत्र लिखिए।
उत्तर-
CaO.
प्रश्न 10.
प्राकृतिक गैस का दहन होने पर होने वाली अभिक्रिया को लिखिए।
उत्तर-
CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (g) + ऊर्जा।
प्रश्न 11.
कोयले का दहन तथा H2 और O2, से जल का निर्माण कैसी अभिक्रिया को दर्शाते हैं?
उत्तर-
संयोजन अभिक्रिया।
प्रश्न 12.

उत्तर-
क्लोरोफ़िल।
प्रश्न 13.
अपचयन क्रिया क्या है ?
उत्तर-
अपचयन वह क्रिया है जिसमें 0, का ह्रास तथा H, की वृद्धि होती है।
प्रश्न 14.
उपचयन क्रिया क्या है ?
उत्तर-
उपचयन वह क्रिया है जिसमें H, का ह्रास तथा O2, की वृद्धि होती है।
प्रश्न 15.
मैग्नीशियम रिबन को वायु में जलाने से कौन-सा पदार्थ बनता है ? ( मॉडल पेपर)
उत्तर-
सफेद पाउडर मैग्नीशियम ऑक्साइड (MgO).
![]()
प्रश्न 16.
नीचे लिखी समीकरण में रिक्त स्थान भरो :
![]()
उत्तर-

प्रश्न 17.
जिंक की तनु सल्फ्यूरिक अम्ल के साथ अभिक्रिया होने से कौन-सी गैस बनती है ?
उत्तर-
हाइड्रोजन गैस (H2)
प्रश्न 18.
निम्नलिखित रासायनिक समीकरण में रिक्त स्थान भरो : BaCl2 + Na2SO4 → …………. + …….
उत्तर-
BaCl2 + Na2SO4 → BaSO4 + 2NaCl
प्रश्न 19.
कार्बनडाइऑक्साइड गैस को चूने के पानी में से प्रवाहित करने पर चूने के पानी में क्या परिवर्तन होता है ?
उत्तर-
चूने का पानी दुधिया हो जाता है।
प्रश्न 20.
निम्नलिखित रासायनिक समीकरण को पूरा करें :
Fe(s) + CuSO4 (aq) → ………………. +
उत्तर-
Fe(s) + CuSO4 (aq) → FeSO4 (aq) + Cu(s)
प्रश्न 21.
निम्नलिखित समीकरण को पूरा करो :
![]()
उत्तर-
![]()
प्रश्न 22.
Zn(s) + CuSO4(aq) → ZnSO4(aq)+ Cu(s) इस रासायनिक समीकरण में किस प्रकार की अभिक्रिया दर्शायी गयी है ?
(क) संयोजन अभिक्रिया
(ख) वियोजन अभिक्रिया
(ग) विस्थापन अभिक्रिया
(घ) द्विविस्थापन अभिक्रिया।
उत्तर-
(ग) विस्थापन अभिक्रिया।
प्रश्न 23.
Na2SO4(aq) + BaCl2→ BaSO4(s) + NaCl(aq) उपरोक्त रासायनिक समीकरण किस प्रकार की रासायनिक अभिक्रिया का उदाहरण है ?
(क) संयोजन अभिक्रिया
(ख) वियोजन अभिक्रिया
(ग) विस्थापन अभिक्रिया
(घ) द्विविस्थापन अभिक्रिया।
उत्तर-
(घ) द्विविस्थापन अभिक्रिया।
वस्तुनिष्ठ प्रश्न (Objective Type Questions)
बहु-विकल्पीय प्रश्न
प्रश्न 1.
BaCl2 (aq) + Na2SO4 (aq) → BaSO4(s) + 2NaCl (aq) है
(a) विस्थापन अभिक्रिया
(b) द्विविस्थापन अभिक्रिया
(c) संयोजन अभिक्रिया
(d) वियोजन अभिक्रिया।
उत्तर-
(b) द्विविस्थापन अभिक्रिया।
प्रश्न 2.
वह अभिक्रिया जिसमें ऊष्मा उत्पन्न होती है, कहलाती है –
(a) बहुलीकरण अभिक्रिया
(b) ऊष्माशोषी अभिक्रिया
(c) ऊष्माक्षेपी अभिक्रिया
(d) उपर्युक्त सभी।
उत्तर-
(c) ऊष्माक्षेपी अभिक्रिया।
![]()
प्रश्न 3.
जल के विद्युत् अपघटन पर उत्पन्न हाइड्रोजन एवं ऑक्सीजन का मोल अनुपात है –
(a) 2:1
(b) 1:1
(c) 2:2
(d) 4:1.
उत्तर-
(a) 2:1.
प्रश्न 4.
जंग का रासायनिक सूत्र है –
(a) Fe2O3
(b) FeCO3
(c) Fe2O3.xH2O
(d) FeCO3.xH2O.
उत्तर-
(c) Fe2O3.xH2O.
प्रश्न 5.
वियोजन अभिक्रिया का उदाहरण है-
(a) CH4 + 2O2, → CO2 + 2H2O
(b) 2Pb (NO3)2 → 2PbO + 4NO2 + O2,
(c) NH3 + HCl → NH4Cl
(d) PB + CuCl2 → PbCl2 + CU.
उत्तर-
(b) 2Pb (NO3)2 → 2PbO + 4NO2 + O2.
प्रश्न 6.
लोहा किसे उसके विलयन से विस्थापित कर सकता है ?
(a) Al
(b) Zn
(c) Cu
(d) AU.
उत्तर-
(c) Cu.
प्रश्न 7.
निम्नलिखित में से कौन-सी अधातु है जो धातुओं की सक्रियता क्रम में उपस्थित रहती है –
(a) O2,
(b) Cl
(c) Br
(d) H2.
उत्तर-
(d) H2.
![]()
रिक्त स्थानों की पूर्ति कीजिए
(i) अपघटन अभिक्रिया ………….. की विपरीत अभिक्रिया है।
उत्तर-
संयोजन अभिक्रिया
(ii) अम्ल व क्षारक की निश्चित मात्रा एवं आयतन मिलाने से ……….. तथा ……….. बनता है।
उत्तर-
लवण, जल
(iii) ऑक्सीजन का समावेश ……….. कहलाता है।
उत्तर-
ऑक्सीकरण
(iv) वह अभिक्रिया जिसमें ऊष्मा का उत्सर्जन होता है, ……… अभिक्रिया कहलाती है।
उत्तर-
ऊष्माक्षेपी
(v) ऑक्सीकरण तथा अपचयन एक-दूसरे की …………. हैं।
उत्तर-
पूरक।
