Punjab State Board PSEB 10th Class Science Book Solutions Chapter 1 ਰਸਾਇਣਿਕ ਕਿਰਿਆਵਾਂ ਅਤੇ ਸਮੀਕਰਣਾਂ Textbook Exercise Questions and Answers.
PSEB Solutions for Class 10 Science Chapter 1 ਰਸਾਇਣਿਕ ਕਿਰਿਆਵਾਂ ਅਤੇ ਸਮੀਕਰਣਾਂ
PSEB 10th Class Science Guide ਰਸਾਇਣਿਕ ਕਿਰਿਆਵਾਂ ਅਤੇ ਸਮੀਕਰਣਾਂ Textbook Questions and Answers
ਪ੍ਰਸ਼ਨ 1.
ਹੇਠ ਲਿਖੀ ਗਈ ਰਸਾਇਣਿਕ ਕਿਰਿਆ ਦੇ ਸੰਬੰਧ ਵਿੱਚ ਕਿਹੜੇ ਕਥਨ ਗਲਤ ਹਨ:
2PbO(s) + C(s) → 2Pb(s) + CO2(g)
(a) ਸ਼ੈੱਡ ਦਾ ਲਘੂਕਰਨ ਹੋ ਰਿਹਾ ਹੈ ।
(b) ਕਾਰਬਨ-ਡਾਈਆਕਸਾਈਡ ਦਾ ਆਕਸੀਕਰਨ ਹੋ ਰਿਹਾ ਹੈ ।
(c) ਕਾਰਬਨ ਦਾ ਆਕਸੀਕਰਨ ਹੋ ਰਿਹਾ ਹੈ ।
(d) ਚੈੱਡ ਆਕਸਾਈਡ ਦਾ ਲਘੂਕਰਨ ਹੋ ਰਿਹਾ ਹੈ ।
(i) (a) ਅਤੇ (b)
(ii) (a) ਅਤੇ (c)
(iii) (a), (b) ਅਤੇ (c)
(iv) ਸਾਰੇ ।
ਉੱਤਰ-
(i) (a) ਅਤੇ (b) ।
ਪ੍ਰਸ਼ਨ 2.
Fe2O3 + 2Al → Al2O3 + 2Fe ਉਪਰੋਕਤ ਰਸਾਇਣਿਕ ਕਿਰਿਆ ਇੱਕ ਉਦਾਹਰਣ ਹੈ :
(a) ਸੰਯੋਜਨ ਕਿਰਿਆ
(b) ਦੂਹਰਾ ਵਿਸਥਾਪਨ ਕਿਰਿਆ
(c) ਅਪਘਟਨ ਕਿਰਿਆ ।
(d) ਵਿਸਥਾਪਨ ਕਿਰਿਆ ।
ਉੱਤਰ-
ਉਪਰੋਕਤ ਰਸਾਇਣਿਕ ਕਿਰਿਆ ਵਿਸਥਾਪਨ ਕਿਰਿਆ ਹੈ ਜਿਸ ਵਿੱਚ Al, Fe2O3 ਦੇ Fe ਨੂੰ ਵਿਸਥਾਪਿਤ ਕਰਦਾ ਹੈ । ਇਸ ਲਈ (d) ਸਹੀ ਉੱਤਰ ਹੈ ।
![]()
ਪ੍ਰਸ਼ਨ 3.
ਕੀ ਹੁੰਦਾ ਹੈ ਜਦੋਂ ਪਤਲਾ ਹਾਈਡਰੋਕਲੋਰਿਕ ਐਸਿਡ ਲੋਹ ਬੂਰਨ ਉੱਤੇ ਪਾਇਆ ਜਾਂਦਾ ਹੈ ? ਸਹੀ ਉੱਤਰ ਤੇ ਨਿਸ਼ਾਨ ਲਗਾਉ ।
(a) ਹਾਈਡਰੋਜਨ ਗੈਸ ਅਤੇ ਆਇਰਨ ਕਲੋਰਾਈਡ ਪੈਦਾ ਹੁੰਦੇ ਹਨ ।
(b) ਕਲੋਰੀਨ ਗੈਸ ਅਤੇ ਆਇਰਨ ਹਾਈਡਰੋਕਸਾਈਡ ਪੈਦਾ ਹੁੰਦੇ ਹਨ ।
(c) ਕੋਈ ਕਿਰਿਆ ਨਹੀਂ ਹੁੰਦੀ ।
(d) ਆਇਰਨੇ ਲੂਣ ਅਤੇ ਪਾਣੀ ਪੈਦਾ ਹੁੰਦੇ ਹਨ ।
ਉੱਤਰ-
ਉਪਰੋਕਤ ਕਿਰਿਆ ਇਸ ਪ੍ਰਕਾਰ ਹੈ –

ਜਿਸ ਵਿੱਚ H2 ਅਤੇ FeCl2 ਮਿਲਦੇ ਹਨ । ਇਸ ਲਈ (a) ਸਹੀ ਉੱਤਰ ਹੈ ।
ਪ੍ਰਸ਼ਨ 4.
ਸੰਤੁਲਿਤ ਰਸਾਇਣਿਕ ਸਮੀਕਰਣ ਕੀ ਹੁੰਦੀ ਹੈ ? ਰਸਾਇਣਿਕ ਸਮੀਕਰਣ ਨੂੰ ਸੰਤੁਲਿਤ ਕਿਉਂ ਕੀਤਾ ਜਾਣਾ ਚਾਹੀਦਾ ਹੈ ?
ਉੱਤਰ-
ਸੰਤੁਲਿਤ ਰਸਾਇਣਿਕ ਸਮੀਕਰਣ-ਜੇ ਕਿਸੇ ਰਸਾਇਣਿਕ ਪ੍ਰਤੀਕਿਰਿਆ ਵਿੱਚ ਅਭਿਕਾਰਕ ਅਤੇ ਉਤਪਾਦਾਂ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਬਰਾਬਰ ਹੋਵੇ, ਤਾਂ ਉਹ ਸੰਤੁਲਿਤ ਰਸਾਇਣਿਕ ਸਮੀਕਰਣ ਕਹਾਉਂਦੀ ਹੈ ।
ਸਮੀਕਰਣ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰਨਾ ਜ਼ਰੂਰੀ ਹੈ ਕਿਉਂਕਿ ਪੁੰਜ ਦੇ ਸੁਰੱਖਿਅਣ ਦੇ ਨਿਯਮ ਅਨੁਸਾਰ ਕਿਸੇ ਵੀ ਰਸਾਇਣਿਕ ਪ੍ਰਤੀਕਿਰਿਆ ਵਿੱਚ ਪੁੰਜ ਦਾ ਨਾ ਤਾਂ ਨਿਰਮਾਣ ਹੁੰਦਾ ਹੈ ਅਤੇ ਨਾ ਹੀ ਵਿਨਾਸ਼ ਇਸਦੇ ਅਨੁਸਾਰ ਦੋਵੇਂ ਪਾਸੇ ਪੁੰਜ ਸਮਾਨ ਹੋਣਾ ਚਾਹੀਦਾ ਹੈ ਅਤੇ ਇਹ ਉਦੋਂ ਹੀ ਸੰਭਵ ਹੈ ਜਦੋਂ ਦੋਨੋਂ ਪਾਸੇ ਦੇ ਤੱਤਾਂ ਦੇ ਪਰਮਾਣੂਆਂ ਦੀ ਗਿਣਤੀ ਬਰਾਬਰ ਹੋਵੇ ।
ਪ੍ਰਸ਼ਨ 5.
ਹੇਠ ਲਿਖੇ ਕਥਨਾਂ ਨੂੰ ਰਸਾਇਣਿਕ ਸਮੀਕਰਣਾਂ ਦੇ ਰੂਪ ਵਿੱਚ ਬਦਲੋ ਅਤੇ ਫਿਰ ਸੰਤੁਲਿਤ ਕਰੋ :
(a) ਹਾਈਡਰੋਜਨ ਗੈਸ ਨਾਈਟਰੋਜਨ ਗੈਸ ਨਾਲ ਜੁੜ ਕੇ ਅਮੋਨੀਆ ਬਣਾਉਂਦੀ ਹੈ ।
(b) ਹਾਈਡਰੋਜਨ ਸਲਫਾਈਡ ਗੈਸ ਹਵਾ ਵਿੱਚ ਬਲ ਕੇ ਪਾਣੀ ਅਤੇ ਸਲਫਰ ਡਾਈਆਕਸਾਈਡ ਬਣਾਉਂਦੀ ਹੈ ।
(c) ਬੇਰੀਅਮ ਕਲੋਰਾਈਡ ਅਤੇ ਐਲੂਮੀਨੀਅਮ ਸਲਫੇਟ ਦੇ ਘੋਲ ਪ੍ਰਤੀਕਿਰਿਆ ਕਰਕੇ ਐਲੂਮੀਨੀਅਮ ਕਲੋਰਾਈਡ ਅਤੇ ਬੇਰੀਅਮ ਸਲਫੇਟ ਦਾ ਅਵਖੇਪ ਬਣਾਉਂਦੇ ਹਨ ।.
(d) ਪੋਟਾਸ਼ੀਅਮ ਧਾਤ ਪਾਣੀ ਨਾਲ ਕਿਰਿਆ ਕਰਕੇ ਪੋਟਾਸ਼ੀਅਮ ਹਾਈਡਰੋਕਸਾਈਡ ਅਤੇ ਹਾਈਡਰੋਜਨ ਗੈਸ ਪੈਦਾ ਕਰਦੀ ਹੈ ।
ਉੱਤਰ-
(a) N2(g) + 32H(g) → 2NH3(g)
(b) 2H2S(g) + 3O2(g) → 2H2O(l) + 2SO2(g)
(c) Al2(SO4)3 + BaCl2(s) → 3BaSO4↓+ 2AlCl3(aq)
(d) 2K(S) + 2H2O(l) → 2KOH(aq) + H2(g).
ਪ੍ਰਸ਼ਨ 6.
ਹੇਠ ਲਿਖੀਆਂ ਰਸਾਇਣਿਕ ਸਮੀਕਰਣਾਂ ਨੂੰ ਸੰਤੁਲਿਤ ਕਰੋ :
(a) HNO3 + Ca(OH)2 → Ca(NO3)2 + H2O
(b) NaOH + H2SO4 → Na2SO4 + H2O
(c) NaCl + AgNO3 → AgCl + NaNO3
(a) BaCl2 + H2SO4 → BaSO4 + HCl.
ਉੱਤਰ-
(a) 2HNO3 + Ca(OH)2 → Ca(NO3)2 + 2H2O
(b) 2NaOH + H2SO4 → Na2SO4 + 2H2O
(c) NaCl + AgNO3 → AgCl + NaNO3
(d) BaCl2 + H2SO4 → BaSO4 + 2HCl
![]()
ਪ੍ਰਸ਼ਨ 7.
ਹੇਠ ਲਿਖੀਆਂ ਕਿਰਿਆਵਾਂ ਲਈ ਸੰਤੁਲਿਤ ਰਸਾਇਣਿਕ ਸਮੀਕਰਣਾਂ ਲਿਖੋ-
(a) ਕੈਲਸ਼ੀਅਮ ਹਾਈਡਰੋਕਸਾਈਡ + ਕਾਰਬਨ-ਡਾਈਆਕਸਾਈਡ → ਕੈਲਸ਼ੀਅਮ ਕਾਰਬੋਨੇਟ + ਪਾਣੀ
(b) ਜ਼ਿੰਕ + ਸਿਲਵਰ ਨਾਈਟਰੇਟ → ਜਿੰਕ ਨਾਈਟਰੇਟ + ਸਿਲਵਰ
(c) ਐਲੂਮੀਨੀਅਮ + ਕਾਪਰ ਕਲੋਰਾਈਡ → ਐਲੂਮੀਨੀਅਮ ਕਲੋਰਾਈਡ + ਕਾਪਰ
d) ਬੇਰੀਅਮ ਕਲੋਰਾਈਡ + ਪੋਟਾਸ਼ੀਅਮ ਸਲਫੇਟ → ਬੇਰੀਅਮ ਸਲਫੇਟ + ਪੋਟਾਸ਼ੀਅਮ ਕਲੋਰਾਈਡ ।
ਉੱਤਰ-
(a) Ca(OH)2 + CO2 → CaCO3 + H2O
(b) Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
(c) 2Al + 3CuCl2 → 2AlCl3 + 3Cu
d) BaCl3 +K2SO4 → BaSO4 + 2KCl
ਪ੍ਰਸ਼ਨ 8.
ਹੇਠ ਲਿਖਿਆਂ ਲਈ ਸੰਤੁਲਿਤ ਰਸਾਇਣਿਕ ਸਮੀਕਰਣਾਂ ਲਿਖੋ ਅਤੇ ਹਰ ਇੱਕ ਰਸਾਇਣਿਕ ਕਿਰਿਆ ਦੀ , ਕਿਸਮ ਦੱਸੋ !
(a) ਪੋਟਾਸ਼ੀਅਮ ਬੋਮਾਈਡ (aq) + ਬੇਰੀਅਮ ਆਈਓਡਾਈਡ (aq) → ਪੋਟਾਸ਼ੀਅਮ ਆਇਓਡਾਈਡ (aq) + ਬੇਰੀਅਮ ਬੋਮਾਈਡ (s)
(b) ਜ਼ਿੰਕ ਕਾਰਬੋਨੇਟ (s) → ਜ਼ਿੰਕ ਆਕਸਾਈਡ (s) + ਕਾਰਬਨ-ਡਾਈਆਕਸਾਈਡ (g)
(c) ਹਾਈਡਰੋਜਨ (g) + ਕਲੋਰੀਨ (g) – ਹਾਈਡਰੋਜਨ ਕਲੋਰਾਈਡ (g)
(d) ਮੈਗਨੀਸ਼ੀਅਮ (s) + ਹਾਈਡਰੋਕਲੋਰਿਕ ਐਸਿਡ (aq) → ਮੈਗਨੀਸ਼ੀਅਮ ਕਲੋਰਾਈਡ (aq) + ਹਾਈਡਰੋਜਨ (g)
ਉੱਤਰ-
(a) 2KBr (aq) + BaI2(aq) → 2KI(aq) + BaBr2(aq) ਇਹ ਇਕ ਦੋਹਰੀ ਵਿਸਥਾਪਨ ਕਿਰਿਆ ਹੈ ।
(b) ZnCO3 (s) → ZnO(s) + CO2 (g) ਇਹ ਵਿਯੋਜਨ (ਅਪਘਟਨ) ਅਭਿਕਿਰਿਆ ਹੈ ।
(c) H2(g) + Cl2(g) → 2HCl(g)
ਇਹ ਸੰਯੋਜਨ ਕਿਰਿਆ ਹੈ ।
(d) Mg(s) + 2HCl (aq) – MgCl2(aq) + H(g)
ਇਹ ਵਿਸਥਾਪਨ ਕਿਰਿਆ ਹੈ ।
ਪ੍ਰਸ਼ਨ 9.
ਤਾਪ-ਨਿਕਾਸੀ ਅਤੇ ਤਾਪ-ਸੋਖੀ ਕਿਰਿਆ ਤੋਂ ਕੀ ਭਾਵ ਹੈ ? ਉਦਾਹਰਨਾਂ ਦਿਉ ।
ਉੱਤਰ-
ਤਾਪ-ਨਿਕਾਸੀ ਕਿਰਿਆ (Exothermic reaction)-ਜਿਹੜੀਆਂ ਕਿਰਿਆਵਾਂ ਵਿੱਚ ਉਤਪਾਦ ਦੇ ਨਾਲ ਤਾਪ ਦਾ ਵੀ ਉਤਸਰਜਨ ਹੁੰਦਾ ਹੈ, ਉਸਨੂੰ ਤਾਪ-ਨਿਕਾਸੀ ਕਿਰਿਆ ਕਹਿੰਦੇ ਹਨ ।
ਉਦਾਹਰਨ-
(1) ਕੁਦਰਤੀ ਗੈਸ ਦਾ ਦਹਿਣ
CH4(g) + 2O2(g) → CO2(g) + 2H2O (1) + ਤਾਪ
(2) ਕੋਕ ਦਾ ਵਹਿਣ
C(s) + O2(g) → CO2(g) + ਤਾਪ
(3) ਸਾਹ ਦੌਰਾਨ ਸਰੀਰ ਵਿੱਚ ਤਾਪ ਊਰਜਾ ਪੈਦਾ ਹੋਣਾ ।
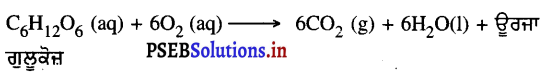
C6H12O6(ag) + 6O2 (g) → 6CO2(g) + 6H2O (1) + ਤਾਪ
ਤਾਪ-ਸੋਖੀ ਕਿਰਿਆ (Endothermic reaction)
ਜਿਹੜੀਆਂ ਕਿਰਿਆਵਾਂ ਵਿੱਚ ਤਾਪ ਦਾ ਸੋਖਣ ਹੁੰਦਾ ਹੈ ਉਨ੍ਹਾਂ ਨੂੰ ਤਾਪ-ਸੋਖੀ ਕਿਰਿਆ ਕਹਿੰਦੇ ਹਨ ।
ਉਦਾਹਰਨਾਂ-
(1) ਕੋਕ ਦੀ ਭਾਫ਼ ਨਾਲ ਕਿਰਿਆ
C(s) + H2O(s) + ਤਾਪ → CO(s) + H2(g)
(2) N2 ਅਤੇ O2 ਦੀ ਕਿਰਿਆ
N2(g) + O2(g) + ਤਾਪ ਊਰਜਾ → 2NO(g) ਨਾਈਟਰਿਕ ਆਕਸਾਈਡ
(3) CaCO3 ਦਾ ਗਰਮ ਹੋਣਾ
CaCO3 + ਤਾਪ → CaO(s) + CO2(g)
ਪ੍ਰਸ਼ਨ 10.
ਸਾਹ ਕਿਰਿਆ ਨੂੰ ਤਾਪ-ਨਿਕਾਸੀ ਕਿਰਿਆ ਕਿਉਂ ਸਮਝਿਆ ਜਾਂਦਾ ਹੈ ? ਵਿਆਖਿਆ ਕਰੋ ।
ਜਾਂ
ਸਾਹ ਕਿਰਿਆ ਨੂੰ ਤਾਪ-ਨਿਕਾਸੀ ਕਿਰਿਆ ਕਿਉਂ ਕਹਿੰਦੇ ਹਨ ?
ਉੱਤਰਜੀਉਂਦੇ ਰਹਿਣ ਲਈ ਸਾਨੂੰ ਉਰਜਾ ਦੀ ਲੋੜ ਹੁੰਦੀ ਹੈ । ਇਹ ਉਰਜਾ ਸਾਨੂੰ ਭੋਜਨ ਤੋਂ ਪ੍ਰਾਪਤ ਹੁੰਦੀ ਹੈ । ਪਾਚਨ ਕਿਰਿਆ ਦੇ ਦੌਰਾਨ ਖਾਧ ਪਦਾਰਥ ਛੋਟੇ-ਛੋਟੇ ਟੁਕੜਿਆਂ ਵਿੱਚ ਟੁੱਟ ਜਾਂਦਾ ਹੈ , ਜਿਵੇਂ-ਚਾਵਲ, ਆਲੂ ਅਤੇ ਬੈਡ ਵਿੱਚ ਕਾਰਬੋਹਾਈਡਰੇਟ ਹੁੰਦਾ ਹੈ । ਕਾਰਬੋਹਾਈਡਰੇਟ ਦੇ ਟੁੱਟਣ ਨਾਲ ਗੁਲੂਕੋਜ਼ ਪ੍ਰਾਪਤ ਹੁੰਦਾ ਹੈ । ਇਹ ਗੁਲੂਕੋਜ਼ ਸਾਡੀਆਂ ਸਰੀਰ ਦੀਆਂ ਕੋਸ਼ਿਕਾਵਾਂ ਵਿੱਚ ਮੌਜੂਦ ਆਕਸੀਜਨ ਨਾਲ ਮਿਲ ਕੇ ਸਾਨੂੰ ਊਰਜਾ ਪ੍ਰਦਾਨ ਕਰਦਾ ਹੈ । ਅਰਥਾਤ ਸਾਹ ਕਿਰਿਆ ਵਿੱਚ ਊਰਜਾ ਪੈਦਾ ਹੁੰਦੀ ਹੈ । ਇਸ ਲਈ ਸਾਹ, ਕਿਰਿਆ ਨੂੰ ਤਾਪ-ਨਿਕਾਸੀ ਕਿਰਿਆ ਆਖਦੇ ਹਨ ।
![]()
ਪ੍ਰਸ਼ਨ 11.
ਅਪਘਟਨ ਕਿਰਿਆਵਾਂ ਨੂੰ ਸੰਯੋਜਨ ਕਿਰਿਆਵਾਂ ਦੇ ਉਲਟ ਕਿਉਂ ਆਖਿਆ ਜਾਂਦਾ ਹੈ ? ਇਹਨਾਂ ਕਿਰਿਆਵਾਂ ਲਈ ਸਮੀਕਰਣਾਂ ਲਿਖੋ ।
ਉੱਤਰ-
ਸੰਯੋਜਨ ਕਿਰਿਆ ਵਿੱਚ ਦੋ ਜਾਂ ਦੋ ਤੋਂ ਵੱਧ ਪਦਾਰਥ ਮਿਲ ਕੇ ਇਕ ਨਵਾਂ ਪਦਾਰਥ ਪ੍ਰਦਾਨ ਕਰਦਾ ਹੈ । ਅਪਘਟਨ ਕਿਰਿਆ ਸੰਯੋਜਨ ਕਿਰਿਆ ਦੇ ਉਲਟ ਹੁੰਦੀ ਹੈ | ਅਪਘਟਨ ਕਿਰਿਆ ਵਿੱਚ ਏਕਲ ਪਦਾਰਥ ਅਪਘਟਿਤ ਹੋ ਕੇ ਦੋ ਜਾਂ ਦੋ ਤੋਂ ਵੱਧ ਪਦਾਰਥ ਪ੍ਰਦਾਨ ਕਰਦਾ ਹੈ ।
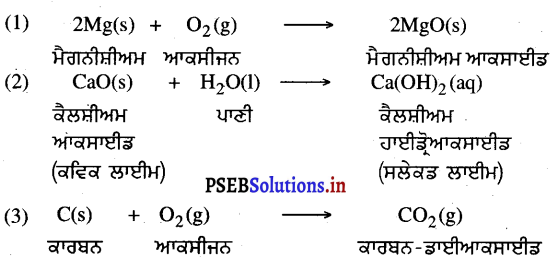
ਅਪਘਟਨ ਕਿਰਿਆ ਦੇ ਉਦਾਹਰਨ ਹਨ-

ਪ੍ਰਸ਼ਨ 12.
ਉਨ੍ਹਾਂ ਅਪਘਟਨ ਕਿਰਿਆਵਾਂ ਦੀ ਇਕ-ਇਕ ਸਮੀਕਰਨ ਲਿਖੋ ਜਿਨ੍ਹਾਂ ਨੂੰ ਤਾਪ ਊਰਜਾ, ਪ੍ਰਕਾਸ਼ ਅਤੇ ਬਿਜਲੀ ਦੇ ਰੂਪ ਵਿੱਚ ਊਰਜਾ ਦਿੱਤੀ ਜਾਂਦੀ ਹੈ ।
ਉੱਤਰ-
(1) ਅਪਘਟਨ ਕਿਰਿਆ ਜਿਸ ਵਿੱਚ ਤਾਪ ਦੀ ਵਰਤੋਂ ਹੁੰਦੀ ਹੈ-


ਪ੍ਰਸ਼ਨ 13.
ਵਿਸਥਾਪਨ ਕਿਰਿਆ ਅਤੇ ਦੂਹਰਾ-ਵਿਸਥਾਪਨ ਕਿਰਿਆ ਵਿੱਚ ਕੀ ਅੰਤਰ ਹੈ ? ਇਨ੍ਹਾਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਦੀਆਂ ਸਮੀਕਰਣਾਂ ਲਿਖੋ ।
ਉੱਤਰ-
ਵਿਸਥਾਪਨ ਕਿਰਿਆ-ਜਦੋਂ ਕੋਈ ਇਕ ਤੱਤ ਦੂਸਰੇ ਤੱਤ ਨੂੰ ਉਸਦੇ ਯੌਗਿਕ ਨਾਲ ਵਿਸਥਾਪਿਤ ਕਰ ਦਿੰਦਾ ਹੈ, ਤਾਂ ਉਹ ਵਿਸਥਾਪਨ ਕਿਰਿਆ ਹੁੰਦੀ ਹੈ ।
ਉਦਾਹਰਨ-

ਦੂਹਰਾ-ਵਿਸਥਾਪਨ ਕਿਰਿਆ – ਦੂਹਰਾ-ਵਿਸਥਾਪਨ ਕਿਰਿਆ ਵਿੱਚ ਦੋ ਵੱਖ-ਵੱਖ ਪਰਮਾਣੂ ਜਾਂ ਪਰਮਾਣੂਆਂ ਦੇ ਸਮੂਹ (ਆਇਨ’ ਦਾ ਆਪਸ ਵਿੱਚ ਆਦਾਨ-ਪ੍ਰਦਾਨ ਹੁੰਦਾ ਹੈ ।
ਉਦਾਹਰਨ-

ਉਪਰੋਕਤ ਉਦਾਹਰਨ ਵਿਸਥਾਪਨ ਅਤੇ ਦੂਹਰਾ ਵਿਸਥਾਪਨ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਦਾ ਅੰਤਰ ਸਪੱਸ਼ਟ ਕਰਦੇ ਹਨ ।
![]()
ਪ੍ਰਸ਼ਨ 14.
ਸਿਲਵਰ ਦੇ ਸ਼ੁੱਧੀਕਰਨ ਵਿੱਚ, ਸਿਲਵਰ ਨਾਈਟਰੇਟ ਦੇ ਘੋਲ ਤੋਂ ਸਿਲਵਰ ਪ੍ਰਾਪਤ ਕਰਨ ਲਈ ਕਾਪਰ ਧਾਤ ਦੁਆਰਾ ਵਿਸਥਾਪਨ ਕੀਤਾ ਜਾਂਦਾ ਹੈ । ਇਸ ਪ੍ਰਕਿਰਿਆ ਨਾਲ ਸੰਬੰਧਿਤ ਰਸਾਇਣਿਕ ਕਿਰਿਆ ਲਿਖੋ ।
ਉੱਤਰ-
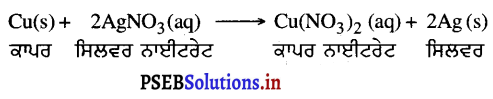
ਪ੍ਰਸ਼ਨ 15.
ਅਵਖੇਪਨ ਪ੍ਰਤੀਕਿਰਿਆ ਤੋਂ ਤੁਹਾਡਾ ਕੀ ਭਾਵ ਹੈ ? ਉਦਾਹਰਣ ਦੇ ਕੇ ਵਿਆਖਿਆ ਕਰੋ ।
ਉੱਤਰ-
ਅਵਖੇਪਨ ਪ੍ਰਤੀਕਿਰਿਆ-ਜਦੋਂ ਦੋ ਘੋਲਾਂ ਨੂੰ ਮਿਲਾਇਆ ਜਾਂਦਾ ਹੈ ਅਤੇ ਉਨ੍ਹਾਂ ਦੀ ਪ੍ਰਤੀਕਿਰਿਆ ਨਾਲ ਸਫ਼ੈਦ ਰੰਗ ਦੇ ਪਦਾਰਥ ਦਾ ਨਿਰਮਾਣ ਹੁੰਦਾ ਹੈ ਜੋ ਪਾਣੀ ਵਿੱਚ ਅਘੁਲਣਸ਼ੀਲ ਹੋਣ । ਇਸ ਅਘੁਲਣਸ਼ੀਲ ਪਦਾਰਥ ਨੂੰ ਅਵਖੇਪ ਕਿਹਾ ਜਾਂਦਾ ਹੈ, ਜਿਸ ਪ੍ਰਤੀਕਿਰਿਆ ਵਿੱਚ ਅਵਖੇਪਾਂ ਦਾ ਨਿਰਮਾਣ ਹੁੰਦਾ ਹੈ, ਉਸ ਨੂੰ ਅਵਖੇਪਣ ਤੀਕਿਰਿਆ ਕਹਿੰਦੇ ਹਨ ।

Ba2+ ਅਤੇ \(\mathrm{SO}_{4}^{2-}\) ਦੀ ਕਿਰਿਆ ਵਿੱਚ BaSO4 ਦੇ ਅਵਖੇਪ ਦਾ ਨਿਰਮਾਣ ਹੁੰਦਾ ਹੈ ।
ਪ੍ਰਸ਼ਨ 16.
ਆਕਸੀਜਨ ਦੀ ਪ੍ਰਾਪਤੀ ਜਾਂ ਹਾਨੀ ਦੇ ਸੰਬੰਧ ਵਿੱਚ ਹੇਠ ਦਿੱਤੀਆਂ ਦੀ ਵਿਆਖਿਆ ਦੋ-ਦੋ ਉਦਾਹਰਨਾਂ ਦੇ ਕੇ ਕਰੋ ।
(a) ਆਕਸੀਕਰਨ
(b) ਲਘੂਕਰਨ ।
ਉੱਤਰ-
(a) ਆਕਸੀਕਰਨ-ਕਿਸੇ ਪ੍ਰਤੀਕਿਰਿਆ ਵਿੱਚ ਪਦਾਰਥ ਦਾ ਆਕਸੀਕਰਨ ਉਦੋਂ ਹੁੰਦਾ ਹੈ ਜਦੋਂ ਉਸ ਵਿੱਚ ਆਕਸੀਜਨ ਦਾ ਵਾਧਾ ਜਾਂ ਹਾਈਡਰੋਜਨ ਦੀ ਹਾਨੀ ਹੁੰਦੀ ਹੈ ।
ਉਦਾਹਰਨ-
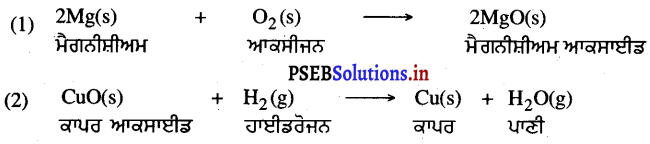
ਇੱਥੇ H2 ਵਿੱਚ O2 ਦਾ ਵਾਧਾ ਅਰਥਾਤ H2 ਦੇ ਨਾਲ O2 ਨੇ ਮਿਲ ਕੇ ਪਾਣੀ ਬਣਾਇਆ ਹੈ ।
(b) ਲਘੂਕਰਨ- ਪਦਾਰਥ ਦਾ ਲਘੂਕਰਨ ਉਦੋਂ ਹੁੰਦਾ ਹੈ ਜਦੋਂ ਉਸ ਵਿੱਚ ਆਕਸੀਜਨ ਦੀ ਹਾਨੀ ਜਾਂ ਹਾਈਡਰੋਜਨ ਦਾ ਵਾਧਾ ਹੁੰਦਾ ਹੈ ।
ਉਦਾਹਰਨ-

ਪ੍ਰਸ਼ਨ 17.
ਇੱਕ ਭੂਰੇ (Brown) ਰੰਗ ਦਾ ਚਮਕਦਾਰ ਤੱਤ ਝੂ’ ਹਵਾ ਦੀ ਹੋਂਦ ਵਿੱਚ ਗਰਮ ਕਰਨ ਨਾਲ ਕਾਲੇ ਰੰਗ ਦਾ ਹੋ ਜਾਂਦਾ ਹੈ । ਇਸ ਤੱਤ ‘x’ ਅਤੇ ਕਾਲੇ ਰੰਗ ਦੇ ਪੈਦਾ ਹੋਏ ਯੌਗਿਕ ਦਾ ਨਾਂ ਦੱਸੋ ।
ਉੱਤਰ-
ਇਹ ਤੱਤ ‘X’ ਕਾਪਰ ਹੈ ਕਿਉਂਕਿ ਕਾਪਰ ਹੀ ਇਕ ਭੂਰੇ ਰੰਗ ਦਾ ਚਮਕਦਾਰ ਤੱਤ ਹੈ ਜੋ ਹਵਾ ਦੀ ਮੌਜੂਦਗੀ ਵਿੱਚ ਗਰਮ ਕਰਨ, ਤੇ ਕਾਲੇ ਰੰਗ ਦਾ ਹੋ ਜਾਂਦਾ ਹੈ ਕਿਉਂਕਿ 0 ਨਾਲ ਪ੍ਰਤੀਕਿਰਿਆ ਕਰਕੇ ਇਹ ਕਾਪਰ ਆਕਸਾਈਡ ਬਣਾਉਂਦਾ ਹੈ ।

![]()
ਪ੍ਰਸ਼ਨ 18.
ਲੋਹੇ ਦੀਆਂ ਵਸਤੂਆਂ ਨੂੰ ਅਸੀਂ ਪੇਂਟ ਕਿਉਂ ਕਰਦੇ ਹਾਂ ?
ਉੱਤਰ-
ਪੇਂਟ ਕਰਨ ਨਾਲ ਲੋਹੇ ਦਾ ਉੱਪਰੀ ਭਾਗ ਛੁਪ ਜਾਂਦਾ ਹੈ । ਇਹ ਹਵਾ ਦੇ ਨਾਲ ਸਿੱਧਾ ਸੰਪਰਕ ਵਿੱਚ ਨਹੀਂ ਆਉਂਦਾ ਜਿਸ ਕਾਰਨ ਉਸ ਵਿੱਚ ਜੰਗ ਨਹੀਂ ਲੱਗਦਾ । ਇਸ ਲਈ ਪੇਂਟ ਕਰਨ ਨਾਲ ਅਸੀਂ ਲੋਹੇ ਦੇ ਉਸ ਪਦਾਰਥ ਨੂੰ ਢੰਗ ਲੱਗਣ ਤੋਂ ਬਚਾ ਸਕਦੇ ਹਾਂ ।
ਪ੍ਰਸ਼ਨ 19.
ਤੇਲ ਅਤੇ ਫੈਟਸ (Fat) ਰੱਖਣ ਵਾਲੀਆਂ ਭੋਜਨ ਵਸਤਾਂ ਨੂੰ ਨਾਈਟਰੋਜਨ ਨਾਲ ਕਿਉਂ ਪ੍ਰਭਾਵਿਤ ਕੀਤਾ ਜਾਂਦਾ ਹੈ ?
ਉੱਤਰ-
ਤੇਲ ਅਤੇ ਫੈਟਸ (Fat) ਰੱਖਣ ਵਾਲੀਆਂ ਭੋਜਨ ਵਸਤਾਂ ਨੂੰ ਹਵਾ-ਰੋਧੀ ਬਰਤਨਾਂ ਵਿੱਚ ਰੱਖਣ ਨਾਲ ਆਕਸੀਕਰਨ ਦੀ ਗਤੀ ਹੌਲੀ ਹੋ ਜਾਂਦੀ ਹੈ । ਤੇਲ ਅਤੇ ਵਸਾਯੁਕਤ ਪਦਾਰਥ ਨੂੰ ਨਾਈਟਰੋਜਨ ਨਾਲ ਇਸ ਲਈ ਯੁਕਤ ਕੀਤਾ ਜਾਂਦਾ ਹੈ ਤਾਂ ਕਿ ਉਸ ਵਿੱਚ ਆਕਸੀਕਰਨ ਨਾ ਹੋ ਸਕੇ ।
ਪ੍ਰਸ਼ਨ 20.
ਹੇਠ ਲਿਖੇ ਪਦਾਂ ਦੀ ਵਿਆਖਿਆ ਉਦਾਹਰਨ ਦੇ ਕੇ ਕਰੋ ।
(a) ਖੋਰਨ
(b) ਦੁਰਗੰਧਤਾ ।
ਉੱਤਰ-
(a) ਖੋਰਨ (Corrosion) – ਲੋਹੇ ਤੋਂ ਬਣੀਆਂ ਵਸਤਾਂ ਚਮਕੀਲੀਆਂ ਹੁੰਦੀਆਂ ਹਨ ਪਰ ਕੁਝ ਸਮੇਂ ਬਾਅਦ ਇਨ੍ਹਾਂ ਤੇ ਲਾਲ ਜਿਹੀ ਭੂਰੇ ਰੰਗ ਦੀ ਪਰਤ ਚੜ ਜਾਂਦੀ ਹੈ । ਆਮ ਤੌਰ ‘ਤੇ ਇਸ ਪ੍ਰਕਿਰਿਆ ਨੂੰ ਲੋਹੇ ਤੇ ਜ਼ੰਗ ਲੱਗਣਾ ਕਹਿੰਦੇ ਹਨ । ਕੁੱਝ ਹੋਰ ਧਾਤਾਂ ਵਿੱਚ ਵੀ ਅਜਿਹਾ ਹੀ ਪਰਿਵਰਤਨ ਹੁੰਦਾ ਹੈ । ਜਦੋਂ ਕੋਈ ਧਾਤ ਆਪਣੇ ਆਸ-ਪਾਸ ਤੇਜ਼ਾਬ, ਨਮੀ ਆਦਿ ਦੇ ਸੰਪਰਕ ਵਿੱਚ ਆਉਂਦੀ ਹੈ ਤਾਂ ਇਹ ਖੁਰਣ ਲਗਦੀ ਹੈ ਅਤੇ ਇਸ ਪ੍ਰਕਿਰਿਆ ਨੂੰ ਖੋਰਨ ਕਿਰਿਆ ਕਹਿੰਦੇ ਹਨ । ਚਾਂਦੀ ਦੇ ਉੱਪਰ ਕਾਲੀ ਪਰਤ ਅਤੇ ਤਾਂਬੇ ਉੱਪਰ ਹਰੀ ਪਰਤ ਚੜਨਾ ਖੋਰਨ ਦੇ ਉਦਾਹਰਨ ਹਨ ।
ਖੋਰਨ ਕਾਰਨ ਕਾਰ ਦੇ ਢਾਂਚੇ, ਪੁਲ, ਜਹਾਜ਼ ਅਤੇ ਧਾਤ ਖ਼ਾਸ ਕਰਕੇ ਲੋਹੇ ਤੋਂ ਬਣੀਆਂ ਵਸਤਾਂ ਨੂੰ ਬਹੁਤ ਹਾਨੀ ਪੁੱਜਦੀ ਹੈ ।
(b) ਦੁਰਗੰਧਤਾ (Rancidity) – ਵਸਾਯੁਕਤ ਅਤੇ ਤੇਲ ਯੁਕਤ ਪਦਾਰਥ ਸਮੱਗਰੀ ਜਦੋਂ ਲੰਬੇ ਸਮੇਂ ਤੱਕ ਰੱਖੀ ਜਾਂਦੀ ਹੈ ਤਾਂ ਉਸਦੇ ਸਵਾਦ ਜਾਂ ਗੰਧ ਵਿੱਚ ਬਦਲਾਓ ਆ ਜਾਂਦਾ ਹੈ । ਆਕਸੀਕਰਨ ਹੋਣ ਤੇ ਤੇਲ ਅਤੇ ਵਸਾ ਵਿਕ੍ਰਿਤ ਧੀ ਹੋ ਜਾਂਦੇ ਹਨ ਅਤੇ ਉਨ੍ਹਾਂ ਦੇ ਸਵਾਦ ਅਤੇ ਗੰਧ ਬਦਲ ਜਾਂਦੇ ਹਨ | ਆਮ ਤੌਰ ‘ਤੇ ਤੇਲ ਯੁਕਤ ਅਤੇ ਵਸਾਯੁਕਤ ਖਾਧ ਸਮੱਗਰੀ ਵਿੱਚ ਆਕਸੀਕਰਨ ਰੋਕਣ ਵਾਲੇ ਪਦਾਰਥ ਪ੍ਰਤੀ ਆਕਸੀਕਰਨ) ਮਿਲਾਏ ਜਾਂਦੇ ਹਨ । ਵਾਯੁਰੋਧੀ ਬਰਤਨਾਂ ਵਿੱਚ ਖਾਧ ਸਮੱਗਰੀ ਰੱਖਣ ਨਾਲ ਆਕਸੀਕਰਨ ਦੀ ਗਤੀ ਹੌਲੀ ਹੋ ਜਾਂਦੀ ਹੈ । ਕੀ ਤੁਸੀਂ ਜਾਣਦੇ ਹੋ ਕਿ ਚਿਪਸ ਬਣਾਉਣ ਵਾਲੇ ਚਿਪਸ ਦੀ ਥੈਲੀ ਨੂੰ ਨਾਈਟਰੋਜਨ ਵਰਗੀ ਗੈਸ ਨਾਲ ਭਰ ਦਿੰਦੇ ਹਨ ਤਾਂਕਿ ਚਿਪਸ ਦਾ ਆਕਸੀਕਰਨ ਨਾ ਹੋ ਸਕੇ ਅਤੇ ਉਨ੍ਹਾਂ ਨੂੰ ਦੇਰ ਤੱਕ ਸੁਰੱਖਿਅਤ ਰੱਖਿਆ ਜਾ ਸਕੇ ।
Science Guide for Class 10 PSEB ਰਸਾਇਣਿਕ ਕਿਰਿਆਵਾਂ ਅਤੇ ਸਮੀਕਰਣਾਂ InText Questions and Answers
ਅਧਿਆਇ ਦੇ ਅੰਦਰ ਦਿੱਤੇ ਗਏ ਪ੍ਰਸ਼ਨ ਅਤੇ ਉਨ੍ਹਾਂ ਦੇ ਉੱਤਰ
ਪ੍ਰਸ਼ਨ 1.
ਹਵਾ ਵਿੱਚ ਜਲਾਉਣ ਤੋਂ ਪਹਿਲਾਂ ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਨੂੰ ਸਾਫ਼ ਕਿਉਂ ਕੀਤਾ ਜਾਂਦਾ ਹੈ ?
ਉੱਤਰ-
ਜੇ ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਨਮ ਹਵਾ ਦੇ ਸੰਪਰਕ ਵਿੱਚ ਰਹਿੰਦਾ ਹੈ, ਤਾਂ ਉਸ ਉੱਪਰ ਸਫ਼ੈਦ ਰੰਗ ਦੀ ਮੈਗਨੀਸ਼ੀਅਮ ਆਕਸਾਈਡ ਦੀ ਪਰਤ ਜੰਮ ਜਾਂਦੀ ਹੈ, ਇਹ ਪਰਤ ਮੈਗਨੀਸ਼ੀਅਮ ਦੇ ਜਲਾਉਣ ਵਿੱਚ ਅਵਰੋਧ ਪੈਦਾ ਕਰਦੀ ਹੈ । ਇਸ ਲਈ ਮੈਗਨੀਸ਼ੀਅਮ ਰਿਬਨ ਨੂੰ ਜਲਾਉਣ ਤੋਂ ਪਹਿਲਾਂ ਰੋਗਮਾਰ ਨਾਲ ਸਾਫ਼ ਕੀਤਾ ਜਾਂਦਾ ਹੈ ।
ਪ੍ਰਸ਼ਨ 2.
ਹੇਠ ਲਿਖੀਆਂ ਰਸਾਇਣਿਕ ਕਿਰਿਆਵਾਂ ਦੀਆਂ ਸੰਤੁਲਿਤ ਸਮੀਕਰਣਾਂ ਲਿਖੋ
(i) ਹਾਈਡਰੋਜਨ + ਕਲੋਰੀਨ → ਹਾਈਡਰੋਜਨ ਕਲੋਰਾਈਡ .
(ii) ਬੇਰੀਅਮ ਕਲੋਰਾਈਡ + ਐਲੂਮੀਨੀਅਮ ਸਲਫੇਟ → ਬੇਰੀਅਮ ਸਲਫੇਟ + ਐਲੂਮੀਨੀਅਮ ਕਲੋਰਾਈਡ
(iii) ਸੋਡੀਅਮ + ਪਾਣੀ → ਸੋਡੀਅਮ ਹਾਈਡਰੋਕਸਾਈਡ + ਹਾਈਡਰੋਜਨ ।
ਉੱਤਰ-
(i) H2 + Cl2 → 2HCl
(ii) 3BaCl2 + Al2(SO4) → 3BaSO4 + 2AlCl3
(iii) 2Na + 2H2O → 2NaOH + H2
![]()
ਪ੍ਰਸ਼ਨ 3.
ਨਿਮਨਲਿਖਤ ਰਸਾਇਣਿਕ ਕਿਰਿਆਵਾਂ ਲਈ ਸੰਕੇਤਾਂ ਸਹਿਤ ਸੰਤੁਲਿਤ ਰਸਾਇਣਿਕ ਸਮੀਕਰਣਾਂ ਲਿਖੋ
(i) ਬੇਰੀਅਮ ਕਲੋਰਾਈਡ ਅਤੇ ਸੋਡੀਅਮ ਸਲਫੇਟ ਦੇ ਪਾਣੀ ਵਿੱਚ ਘੋਲ ਆਪਸ ਵਿੱਚ ਕਿਰਿਆ ਕਰਕੇ ਅਘੁਲ ਸੋਡੀਅਮ ਸਲਫੇਟ ਅਤੇ ਸੋਡੀਅਮ ਕਲੋਰਾਈਡ ਦਾ ਘੋਲ ਪੈਦਾ ਕਰਦੇ ਹਨ ।
(ii) ਸੋਡੀਅਮ ਹਾਈਡਰੋਕਸਾਈਡ ਦਾ ਪਾਣੀ ਵਿੱਚ ਘੋਲ ਹਾਈਡਰੋਕਲੋਰਿਕ ਐਸਿਡ ਦੇ ਪਾਣੀ ਘੋਲ ਨਾਲ ਕਿਰਿਆ ਕਰਕੇ ਸੋਡੀਅਮ ਕਲੋਰਾਈਡ ਦਾ ਪਾਣੀ ਵਿੱਚ ਘੋਲ ਅਤੇ ਪਾਣੀ ਬਣਾਉਂਦੇ ਹਨ ।
ਉੱਤਰ-
(i) BaCl2 (aq) + Na2SO4 (aq) →BaSO4(s) + 2NaCl(aq)
(ii) NaOH (aq) + HCl (aq) → NaCl (aq) + H2O (l).
ਪ੍ਰਸ਼ਨ 4.
ਕਿਸੇ ਵਸਤੂ ‘X’ ਦਾ ਘੋਲ ਸਫੈਦੀ ਲਈ ਉਪਯੋਗ ਕੀਤਾ ਜਾਂਦਾ ਹੈ :
(i) ਵਸਤੂ ‘X’ ਦਾ ਨਾਂ ਅਤੇ ਉਸਦਾ ਸੂਤਰ ਲਿਖੋ ।
(ii) ਉਕਤ (i) ਵਿੱਚ ਲਿਖੀ ਵਸਤੂ ‘X’ ਦੀ ਪਾਣੀ ਨਾਲ ਹੁੰਦੀ ਕਿਰਿਆ ਲਿਖੋ ।
ਉੱਤਰ-
(i) ‘X’ ਦਾ ਨਾਮ ਹੈ – ਬਿਨਾਂ ਬੁੱਝਿਆ ਚੂਨਾ ਅਰਥਾਤ ਕੈਲਸ਼ੀਅਮ ਆਕਸਾਈਡ, ਸੂਤਰ = CaO
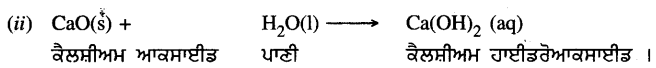
ਪ੍ਰਸ਼ਨ 5.
ਕਿਰਿਆ 1.7 ਵਿੱਚ ਇੱਕ ਪਰਖਨਲੀ ਵਿੱਚ ਇਕੱਤਰ ਹੋਈ ਗੈਸ ਦੀ ਮਾਤਰਾ ਦੂਜੀ ਨਾਲੋਂ ਦੁੱਗਣੀ ਕਿਉਂ ਹੁੰਦੀ ਹੈ ? ਉਸ ਗੈਸ ਦਾ ਨਾਂ ਦੱਸੋ ।
ਉੱਤਰ-
ਪਾਣੀ ਦੇ ਬਿਜਲਈ ਅਪਘਟਨ ਵਿੱਚ ਹੇਠ ਲਿਖੀ ਪ੍ਰਤੀਕਿਰਿਆ ਹੁੰਦੀ ਹੈ-
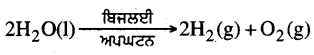
ਇਸ ਪ੍ਰਤੀਕਿਰਿਆ ਵਿੱਚ ਹਾਈਡਰੋਜਨ ਅਤੇ ਆਕਸੀਜਨ 2:1 ਦੀ ਮਾਤਰਾ ਵਿੱਚ ਮਿਲਦੀ ਹੈ ।
ਦੁੱਗਣੀ ਪਾਈ ਜਾਣ ਵਾਲੀ ਗੈਸ ਹਾਈਡਰੋਜਨ ਹੈ । ਅਧਿਆਇ ਦੇ
ਪ੍ਰਸ਼ਨ 6.
ਜਦੋਂ ਲੋਹੇ (IRON) ਦੀ ਮੇਖ ਨੂੰ ਕਾਪਰ ਸਲਫੇਟ ਦੇ ਘੋਲ ਵਿੱਚ ਡੁਬੋਇਆ ਜਾਂਦਾ ਹੈ ਤਾਂ ਘੋਲ ਦਾ ਰੰਗ ਕਿਉਂ ਬਦਲ ਜਾਂਦਾ ਹੈ ?
ਉੱਤਰ-
ਜਦੋਂ ਲੋਹੇ ਦੀ ਮੇਖ ਨੂੰ ਕਾਪਰ ਸਲਫੇਟ ਦੇ ਘੋਲ ਵਿੱਚ ਡੁਬੋਇਆ ਜਾਂਦਾ ਹੈ ਤਾਂ ਇਹ ਕਾਪਰ ਸਲਫੇਟ ਦੇ ਘੋਲ ਵਿੱਚੋਂ ਕਾਪਰ ਨੂੰ ਪ੍ਰਸਥਾਪਿਤ ਕਰਨ ਦੀ ਸਮਰੱਥਾ ਰੱਖਦਾ ਹੈ । ਜਿਸ ਕਰਕੇ ਆਇਰਨ ਸਲਫੇਟ ਬਣ ਜਾਂਦਾ ਹੈ ।

ਇਸ ਪ੍ਰਤੀਕਿਰਿਆ ਦੇ ਦੌਰਾਨ CuSO4 ਦਾ ਨੀਲਾ ਰੰਗ ਹੌਲੀ-ਹੌਲੀ ਛਿੱਕਾ ਹੋ ਜਾਂਦਾ ਹੈ ।
![]()
ਪ੍ਰਸ਼ਨ 7.
ਕਿਰਿਆ 1.10 ਵਿੱਚ ਦਿੱਤੀ ਉਦਾਹਰਣ ਤੋਂ ਬਿਨਾਂ ਦੂਹਰੇ-ਵਿਸਥਾਪਨ ਕਿਰਿਆ ਦੀ ਹੋਰ ਉਦਾਹਰਨ ਦਿਓ ।
ਉੱਤਰ-

ਪ੍ਰਸ਼ਨ 8.
ਹੇਠ ਲਿਖੀਆਂ ਰਸਾਇਣਿਕ ਕਿਰਿਆਵਾਂ ਵਿੱਚ ਆਕਸੀਕਰਿਤ ਅਤੇ ਲਘੂਕਰਿਤ ਹੋਈਆਂ ਵਸਤਾਂ ਦੀ ਪਛਾਣ ਕਰੋ-
(i) 4Na(s) + O2(g) → 2Na2O(s)
(ii) CuO(s) + H2(g) → Cu(s) + H2O(1)
ਉੱਤਰ-
(i) 4Na (s) + O2(g) → 2Na2O(s)
ਆਕਸੀਕਰਿਤ ਪਦਾਰਥ = Na
ਲਘੂਕਰਿਤ ਪਦਾਰਥ = O2
(ii) CuO(s) + H2(g) → Cu(s) + H2O(1) .
ਆਕਸੀਕਰਿਤ ਪਦਾਰਥ = H2
ਲਘੂਕਰਿਤ ਪਦਾਰਥ = CuO
