Punjab State Board PSEB 10th Class Science Book Solutions Chapter 5 तत्वों का आवर्त वर्गीकरण Textbook Exercise Questions, and Answers.
PSEB Solutions for Class 10 Science Chapter 5 तत्वों का आवर्त वर्गीकरण
PSEB 10th Class Science Guide तत्वों का आवर्त वर्गीकरण Textbook Questions and Answers
प्रश्न 1.
आवर्त सारणी में बाएँ से दाएँ जाने पर प्रवृत्तियों के बारे में कौन-सा कथन असत्य है ?
(a) तत्वों की धात्विक प्रकृति घटती है।
(b) संयोजकता इलैक्ट्रॉनों की संख्या बढ़ जाती है।
(c) परमाणु आसानी से इलैक्ट्रॉन का त्याग करते हैं।
(d) इनके ऑक्साइड अधिक अम्लीय हो जाते हैं।
उत्तर-
कथन (c) असत्य है क्योंकि आवर्त सारणी में बाएँ से दाएँ जाने पर परमाणु आसानी से इलैक्ट्रॉन का त्याग करते हैं।
प्रश्न 2.
तत्व X, XCI, सूत्र वाला एक क्लोराइड बनाता है, जो एक ठोस है और जिसका गलनांक अधिक है। आवर्त सारणी में यह तत्व संभवत : किस समूह के अंतर्गत होगा ?
(a) Na
(b) Mg
(c) Al
(d) Si.
उत्तर-
यदि तत्व X, XCI, सूत्र का क्लोराइड बनाता है तो X तत्व के संयोजक इलैक्ट्रॉन की संख्या 2 होगी अर्थात् उसके बाह्यतम कक्ष में संयोजकता इलैक्ट्रॉन की संख्या 2 होगी। आवर्त सारणी के अनुसार केवल वर्ग 2 के तत्व Be, Mg, Ca, Sr, Ba एवं Ra की संयोजकता इलैक्ट्रॉनों की संख्या दो है। इसलिए X तत्व Mg (मैग्नीशियम) है क्योंकि मैग्नीशियम एक धातु होते हुए भी एक आयनिक क्लोराइड बनाने की क्षमता रखता है, जिसका गलनांक उच्च है। अतः तत्व X संभवत: Mg समूह के अंतर्गत होगा।
प्रश्न 3.
किस तत्व में
(a) दो कोश है तथा दोनों इलैक्ट्रॉनों से पूरित हैं ?
(b) इलैक्ट्रॉनिक विन्यास 2, 8, 2 है ?
(c) कुल तीन कोश हैं तथा संयोजकता कोश में चार इलैक्ट्रॉन हैं ?
(d) कुल दो कोश हैं तथा संयोजकता कोश में तीन इलैक्ट्रॉन हैं ?
(e) दूसरे कोश में पहले कोश से दुगुने इलैक्ट्रॉन हैं ?
उत्तर-
(a) उत्कृष्ट गैसों के सभी कोश इलैक्ट्रॉन से भरे होते हैं। इसलिए दिया गया तत्व एक उत्कृष्ट तत्व गैस है। क्योंकि इसके दो कोश पूर्णतः इलैक्ट्रॉनों से भरे हैं। इस प्रकार यह तत्व Ne (निऑन) (2, 8) है।
(b) इलैक्ट्रॉनिक विन्यास 2, 8, 2 का जोड़ 12 जो इस तत्व का परमाणु अंक है और 12 परमाणु अंक वाला तत्व (Mg) मैग्नीशियम है।
(c) कुल तीन कोशों में से बाह्यतम कोश में इलैक्ट्रॉनों की संख्या 4 है। अतः तत्व का इलैक्ट्रॉनिक विन्यास है2, 8, 4 का जोड़ होगा 14 (Si) सिलिकॉन इस प्रकार 14 परमाणु अंक वाला तत्व है।
(d) कुल दो कोश हैं बाह्यतम कोश में 3 इलैक्ट्रॉन हैं। इस प्रकार तत्व का इलैक्ट्रॉनिक विन्यास है-(2, 3) तथा विन्यास जोड़ 5 है। अतः इलैक्ट्रॉनिक विन्यास 5 वाला तत्व है बोरॉन (B)।
(e) दूसरे कोश में पहले की अपेक्षा दुगुने इलैक्ट्रॉन हैं। अतः तत्व का इलैक्ट्रॉनिक विन्यास है-2, 4 तथा विन्यास जोड़ 6 होगा। इस प्रकार परमाणु संख्या 6 वाला तत्व है- कार्बन (C)।
प्रश्न 4.
(a) आवर्त सारणी में बोरॉन के स्तंभ के सभी तत्वों के कौन से गुणधर्म समान हैं ?
(b) आवर्त सारणी में फ्लुओरीन के स्तंभ के सभी तत्वों के कौन से गुणधर्म समान हैं ?
उत्तर-
(a) आवर्त सारणी में बोरॉन स्तंभ के सभी तत्व परमाणु संख्या 13 से संबंध रखते हैं। इसलिए इन सबके बाह्यतम संयोजकता कोश में इलैक्ट्रॉन की संख्या तीन (3) होगी। बोरॉन (B) को छोड़कर जो एक अधातु है, शेष सभी तत्व धातुएं हैं, जैसे-AI, Ga, In एवं Th
(b) फ्लुओरीन के स्तंभ में आने वाले सभी तत्व उत्कृष्ट तत्व हैं तथा परमाणु संख्या 17 से संबंध रखते हैं। इसलिए उनके बाह्यतम कोश में इलैक्ट्रॉन की संख्या 7 होगी। ये सभी तत्व F, CI, Br, I अधातुएँ हैं।
प्रश्न 5.
एक परमाणु का इलैक्ट्रॉनिक विन्यास 2, 8, 7 है।
(a) इस तत्व की परमाणु-संख्या क्या है ?
(b) निम्न में से किस तत्व के साथ इसकी रासायनिक समानता होगी ? (परमाणु-संख्या कोष्ठक में दी गई है) N(7), F (9), P(15), Ar(18).
उत्तर-
(a) तत्व की परमाणु संख्या = 2 + 8 + 7 = 17 है और यह तत्व क्लोरीन है।
(b) क्योंकि तत्व के बाह्यतम संयोजकता कोश में इलैक्ट्रॉनों की संख्या 7 है। इसलिए यह उत्कृष्ट तत्वों के वर्ग 17 से संबंध रखता है। इस परिवार के अन्य तत्वों की परमाणु संख्या एवं इलैक्ट्रॉनिक विन्यास निम्न सारणी में दिए हैं-
| तत्व | परमाणु संख्या | इलैक्ट्रॉनिक विन्यास |
| फ्लुओरिन (F) | 9 | 2, 7 |
| ब्रोमीन (Br) | 35 | 2, 8, 18, 7 |
| आयोडीन (I) | 53 | 2, 8, 18, 18, 7 |
इस प्रकार तत्व F जिसकी परमाणु संख्या 9 है उत्कृष्ट तत्वों के परिवार से संबंध रखता है। अतः यह तत्व क्लोरीन तत्व के रासायनिक रूप के समान होगा।
प्रश्न 6.
आवर्त सारणी में तीन तत्व A, B तथा C की स्थिति निम्न प्रकार है :

अब बताइए कि :
(a) A धातु है या अधातु।
(b) A की अपेक्षा C अधिक अभिक्रियाशील है या कम ?
(c) C का साइज़ B से बड़ा होगा या छोटा ?
(d) तत्व A, किस प्रकार के आयन, धनायन या ऋणायन बनाएगा ?
उत्तर-
(a) समूह 17 के तत्वों के बाह्यतम संयोजकता कोश में इलैक्ट्रॉन की संख्या 7 है और सभी तत्व एक इलैक्ट्रॉन धारण करने की उच्च क्षमता रखते हैं। अतः सभी तत्व अधातु हैं।
(b) एक वर्ग में नीचे की ओर आने पर परमाणु आकार बढ़ता है। इसलिए नाभिक की बाह्यतम इलैक्ट्रॉन को खींचने की क्षमता कम हो जाती है। इस प्रकार किसी वर्ग में नीचे आने पर अभिक्रियाशीलता कम हो जाती है। अतः तत्व C तत्व A से कम अभिक्रियाशील है।
(c) तत्व B की तुलना में तत्व से आकार छोटा होगा।
(d) तत्व A ऋणायन बनाएगा।
प्रश्न 7.
नाइट्रोजन (परमाणु संख्या 7) तथा फ़ॉस्फोरस (परमाणु संख्या 15) आवर्त सारणी के समूह 15 के तत्व हैं। इन दोनों तत्वों को इलैक्ट्रॉनिक विन्यास लिखिए। इनमें से कौन सा तत्व अधिक ऋण विद्युत् होगा और क्यों?
उत्तर-
नाइट्रोजन का इलैक्ट्रॉनिक विन्यास : N (7) : (2, 5) फ़ॉस्फोरस का इलेक्ट्रॉनिक विन्यास : P (15) : (2, 8, 5) नाइट्रोजन की विद्युत् ऋणात्मकता अधिक होगी क्योंकि इसका बाह्यतम कोश केंद्र के अधिक समीप है। इसलिए परमाणु केंद्र इलेक्ट्रॉन को अधिक बल से आकर्षित करेगा।
प्रश्न 8.
तत्वों के इलैक्ट्रॉनिक विन्यास का आधुनिक आवर्त सारणी में तत्व की स्थिति से क्या संबंध है ?
उत्तर-
किसी परमाणु का इलैक्ट्रॉनिक विन्यास आधुनिक आवर्त सारणी में इसकी स्थिति से इस प्रकार संबंधित होता है कि जिन परमाणुओं के बाह्यतम कोशों में इलैक्ट्रॉनों की समान संख्या होती है, उन्हें समान वर्ग में रखा जाता है। बाह्यतम कोश में उपस्थित इलेक्ट्रॉनों की संख्या उस तत्व की समूह संख्या को सूचित करती है तथा बाह्यतम कोश संख्या उस तत्व की आवर्त को सूचित करता है। जब किसी आवर्त में बाएँ से दाएँ चलते हैं, तब संयोजकता कोश इलैक्ट्रॉनों की संख्या इकाई बढ़ जाती है, चूंकि परमाणु क्रमांक इकाई बढ़ जाता है।
प्रश्न 9.
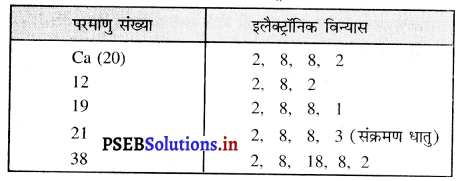
आधुनिक आवर्त सारणी में कैल्सियम (परमाणु-संख्या 20) के चारों ओर 12, 19, 21 तथा 38 परमाणु-संख्या वाले तत्व स्थित हैं। इनमें से किन तत्वों के भौतिक एवं रासायनिक गुणधर्म कैल्सियम के समान हैं ?
उत्तर-
परमाणु संख्या 12 वाले तत्व के भौतिक एवं रासायनिक गुणधर्म परमाणु संख्या 20 तथा 38 वाले तत्वों के समान होगा, क्योंकि इन तत्वों के बाहरी कोश में 2 इलैक्ट्रॉन हैं।
प्रश्न 10.
आधुनिक आवर्त सारणी एवं मेन्डलीफ की आवर्त सारणी में तत्वों की व्यवस्था की तुलना कीजिए।
उत्तर-
मेन्डलीफ की आवर्त सारणी की आवर्त सारणी के दीर्घ रूप से तुलना मेन्डलीफ की आवर्त सारणी और आधुनिक आवर्त सारणी में तत्वों को एक समान तालिका के रूप में स्थान दिया गया है। दोनों सारणियों में एक समान गुणों वाले तत्वों को एक ही ग्रुप में रखा गया है लेकिन इन दोनों में काफ़ी समानताएँ हैं ; जैसे-
| मेन्डलीफ की आवर्त सारणी | आधुनिक आवर्त सारणी |
| (1) उस समय तक ज्ञात 63 तत्वों को बढ़ते परमाणु द्रव्यमानों में व्यवस्थित किया गया था। | (1) कुल 118 तत्वों को बढ़ते परमाणु क्रमांक में व्यवस्थित किया गया है। |
| (2) इस आवर्त सारणी में 8 ऊर्ध्वाधर स्तंभ हैं, जिन्हें वर्ग 7 आवर्त हैं। | (2) इसमें 18 ऊर्ध्वाधर स्तंभ हैं जिन्हें वर्ग कहते हैं तथा कहते हैं। |
| (3) तत्वों के समस्थानिकों को सारणी में स्थान नहीं मिल सका। | (3) तत्वों के समस्थानिकों को सारणी में स्थान नहीं मिल हुआ क्योंकि उनके परमाणु क्रमांक एक-समान होते हैं। |
| (4) रासायनिक दृष्टि से असमान तत्वों को भी एक साथ रखा गया था। | (4) रासायनिक दृष्टि से असमान तत्वों को अलग-अलग वर्गों में स्थान दिया गया। |
| (5) सभी संक्रमण तत्वों को एक ही वर्ग VIII में रखा गया। | (5) संक्रमण तत्वों को वर्ग 3 से वर्ग 12 में रखा गया। |
| (6) उत्कृष्ट गैसों की इस सारणी के बनने तक खोज ही नहीं हो पाई थी। | (6) उत्कृष्ट गैसों को वर्ग 18 में स्थान दिया गया है। |
| (7) कुछ उच्च द्रव्यमान वाले तत्वों को उन तत्वों से पहले स्थान दिया गया जिनका परमाणु द्रव्यमान कम है। | (7) इस सारणी में वर्गीकरण का आधार परमाणु क्रमांक है इसलिए इसमें प्रतिलोम क्रम का दोष नहीं है। |
Science Guide for Class 10 PSEB तत्वों का आवर्त वर्गीकरण InText Questions and Answers
प्रश्न 1.
क्या डॉबेराइनर के त्रिक, न्यूलैंड्स के अष्टक के स्तंभ में भी पाए जाते हैं ? तुलना करके पता कीजिए।
उत्तर-
हाँ, डॉबेराइनर के त्रिक, न्यूलैंड्स के अष्टक स्तंभ में भी पाए जाते हैं। उदाहरण के लिए-
लीथियम (Li), सोडियम (Na) तथा पोटाशियम (K) एक डॉबेराइनर का त्रिक बनाते हैं। यदि Li को पहला तत्व मानें तो उससे आठवें स्थान पर Na आता है और यदि Na को पहला तत्व मानें तो उसके आठवें स्थान पर K आता है। इस प्रकार डॉबेराइनर का यह त्रिक, न्यूलैंड्स के अष्टक के स्तंभ ‘रे’ में पाया जाता है।
डॉबेराइनर का त्रिक Ca, Sr तथा Ba न्यूलैंड्स के अष्टक के स्तंभ Br ‘गा’ में उपस्थित है।

डॉबेराइनर का त्रिक Cl, Br तथा I न्यूलैंड्स के अष्टक के स्तंभ ‘सा’ में उपस्थित है।
प्रश्न 2.
डॉबेराइनर के वर्गीकरण की क्या सीमाएँ हैं ?
उत्तर-
डॉबेराइनर के वर्गीकरण की सबसे बड़ी सीमा यह थी कि इस नियम के अनुसार उस समय के ज्ञात 30 तत्वों में से केवल 9 तत्वों को ही तीन त्रिकों में व्यवस्थित किया जा सका। अत: यह वर्गीकरण सर्वमान्य नहीं हो पाया।
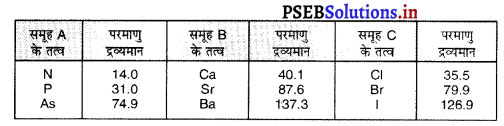
उदाहरण-
तीन तत्व; नाइट्रोजन (N), फॉस्फोरस (P) तथा ऑरसेनिक (As) के रासायनिक गुणधर्म समान हैं इसलिए इन्हें एक ही त्रिक का होना चाहिए जबकि N परमाणु द्रव्यमान (14,0 u), As का (74.9 a) तथा P का (31/0 u) है जिसके अनुसार यह एक त्रिक के तत्व नहीं हैं।
प्रश्न 3.
न्यूलैंड्स के अष्टक सिद्धांत की क्या सीमाएँ हैं ?
उत्तर-
न्यूलैंड्स के अष्टक सिद्धांत की सीमाएं निम्नलिखित हैं –
(i) यह सिद्धांत केवल कैल्सियम तक ही लागू हो सका क्योंकि कैल्सियम के बाद आने वाले प्रत्येक आठवें तत्व का गुणधर्म पहले तत्व के समान नहीं मिलता था।
(ii) न्यूलैंड्स ने कल्पना की थी कि प्रकृति में केवल 56 तत्व विद्यमान हैं और भविष्य में कोई नया तत्व नहीं मिलेगा। लेकिन बाद में कई तत्व खोजे गए जिनके गुणधर्म अष्टक नियम के अनुसार नहीं थे और इस कारण इसमें व्यवस्थित नहीं हो सके।
(iii) अपनी सारणी में तत्वों को समंजित करने के लिए न्यूलैंड्स ने दो तत्वों को एक साथ रख दिया था और कुछ असमान तत्वों को एक स्थान में रख दिया था। उदाहरणार्थ- कोबाल्ट तथा निकिल को एक ही स्थान पर रखा गया हैं, परंतु उन्हें फ्लुओरोन, क्लोरीन तथा ब्रोमीन के साथ एक ही स्तम्भ ‘सा’ के अंतर्गत रखा गया है, जबकि कोबाल्ट तथा निकिल के गुण प्लुओरीन, क्लोरीन तथा ब्रोमीन से सर्वथा भिन्न हैं। दूसरी ओर आयरन, जो कि गुणों से कोबाल्ट तथा निकिल के समान है, को इनसे दूर ‘ना’ स्तम्भ में रखा गया है। संगीत के सुर (डो)
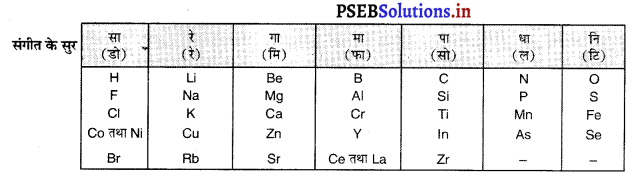
(iv) न्यूलैंड्स अष्टक सिद्धांत केवल हल्के तत्वों के लिए ठीक से लागू हो सका।
प्रश्न 4.
मेन्डलीफ के आवर्त सारणी का उपयोग कर निम्नलिखित तत्वों के ऑक्साइड के सूत्र का अनुमान कीजिए
K, C, AI, Si, Ba
उत्तर-
- पोटैशियम (K) वर्ग IA का तत्व है। इसकी संयोजकता 1 है। इसलिए इसके ऑक्साइड का सूत्र K2O है।
- कार्बन (C) वर्ग: IV A का तत्व है। इसकी संयोजकता 4 है तथा इसके ऑक्साइड का सूत्र CO2 है।
- AI, वर्ग III A का तत्व है। इसकी संयोजकता 3 है। इसलिए इसके ऑक्साइड का सूत्र Al2O3 है।
- सिलिकॉन (Si) IV A वर्ग का तत्व है। इसकी संयोजकता 4 है। इसलिए इसके ऑक्साइड का सूत्र SiO2 है।
- Ba वर्ग II A का तत्व है। इसकी संयोजकता 2 है। इसलिए इसकी ऑक्साइड का सूत्र Ba0 है।
प्रश्न 5.
गैलियम के अतिरिक्त, अब तक कौन-कौन से तत्वों का पता चला है जिसके लिए मेन्डलीफ ने अपनी आवर्त सारणी में खाली स्थान छोड़ दिया था ? दो उदाहरण दीजिए।
उत्तर-
जर्मेनियम (Ge) तथा स्कैंडियम वर्ग IV A के दो तत्व हैं। इन दोनों तत्वों के लिए भी मेन्डलीफ ने अपनी आवर्त सारणी में खाली स्थान छोड़ दिया था। मेन्डलीफ ने इनके गुणधर्म पहले से ही बता दिए थे। जब बाद में इन तत्वों की खोज हुई तो इनके गुणधर्म लगभग वही थे जो मेन्डलीफ ने दिए थे।
प्रश्न 6.
मेन्डलीफ ने अपनी आवर्त सारणी तैयार करने के लिए कौन-सा मापदंड अपनाया था?
उत्तर-
- तत्वों को उनके बढ़ते हुए परमाणु द्रव्यमान के क्रम में व्यवस्थित किया।
- समान गुण वाले तत्वों को एक समूह में रखने का प्रयास किया।
- तत्वों के ऑक्साइडों एवं हाइड्राइड्रों के अणु-सूत्रों को एक आधारभूत गुण मानकर तत्वों का वर्गीकरण किया।
प्रश्न 7.
आपके अनुसार उत्कृष्ट गैसों को अलग समूह में क्यों रखा गया ?
उत्तर-
अक्रिय या उत्कृष्ट गैसों को अलग समूह में रखा गया क्योंकि
- ये गैसें बहुत ही अक्रियाशील होती हैं एवं इनकी खोज बहुत बाद में हुई।
- इन गैसों को एक नये समूह में बिना आवर्त सारणी में छेड़-छाड़ किए हुए रखा गया।
प्रश्न 8.
आधुनिक आवर्त सारणी द्वारा किस प्रकार से मेन्डलीफ की आवर्त सारणी की विविध विसंगतियों को दूर किया गया ?
उत्तर-
मेन्डलीफ की आवर्त सारणी परमाणु द्रव्यमान (Atomic Mass) के सिद्धांत पर आधारित थी जबकि आधुनिक आवर्त सारणी परमाणु संख्या (Atomic number) पर आधारित है। आधुनिक आवर्त नियम के द्वारा मेन्डलीफ की सारणी की विसंगतियों को निम्नलिखित प्रकार सुलझाया गया है –
- आधुनिक आवर्त सारणी में सभी समस्थानिकों को एक ही स्थान दिया गया है क्योंकि समस्थानिकों में प्रोटॉनों की संख्या तो सदा समान होती है। इसलिए परमाणु संख्या भी एक समान ही होगी।
- आर्गन तथा पोटैशियम की परमाणु संख्या क्रमशः 18 और 19 है। तत्वों की बढ़ती परमाणु संख्या के आधार पर व्यवस्थित करने पर आर्गन पहले आ जाता है और पोटैशियम का स्थान पीछे हो जाता है जबकि उनके परमाणु द्रव्यमान इसके विपरीत हैं। आधुनिक आवर्त सारणी में इस दोष को दूर किया गया है।
- तत्वों, उत्कृष्ट गैसों और संक्रमण तत्वों को स्पष्ट रूप से अलग-अलग किया गया है।
- आधुनिक आवर्त सारणी स्पष्ट रूप से दर्शाती है कि तत्वों के गुणों की पुनरावृत्ति क्यों होती है।
प्रश्न 9.
मैग्नीशियम की तरह रासायनिक अभिक्रियाशीलता दिखाने वाले दो तत्वों के नाम लिखिए। आपके चयन का क्या आधार है ?
उत्तर-
आधुनिक आवर्त सारणी के अनुसार, जिन तत्वों की बाहरी इलैक्ट्रॉनिक विन्यास समान होती है उनके गुणधर्म भी समान होते हैं। मैग्नीशियम के बाहरी कक्ष (या कोश) में दो इलैक्ट्रॉन हैं इसलिए वे सभी तत्व जिनके बाहरी कोश में 2 संयोजी इलैक्ट्रॉन होंगे वे Mg के समान ही गुणधर्म प्रदर्शित करेंगे। उदाहरण-कैल्सियम (Ca), परमाणु संख्या = 20
कक्ष में व्यवस्थित इलैक्ट्रॉन = (2, 8, 8, 2) मैग्नीशियम (Mg), परमाणु संख्या = 12
कक्ष में व्यवस्थित इलैक्ट्रॉन = (2, 8, 2)
प्रश्न 3. निम्न के नाम बताइए :
(a) तीन तत्वों जिनके सबसे बाहरी कोश में एक इलैक्ट्रॉन उपस्थित हो।
(b) दो तत्वों जिनके सबसे बाहरी कोश में दो इलैक्ट्रॉन उपस्थित हों।
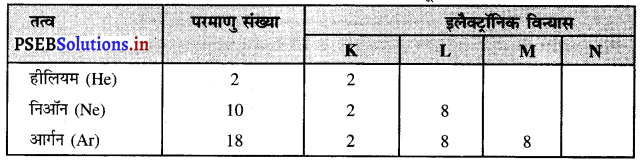
(c) तीन तत्वों जिनका बाहरी कोश पूर्ण हो।
उत्तर-
(a) तीन तत्व जिनके सबसे बाहरी कोश में एक इलैक्ट्रॉन उपस्थित है। Li, Na तथा k तीन ऐसे तत्व हैं जिनके सबसे बाहरी कोश में एक इलैक्ट्रॉन होता है।
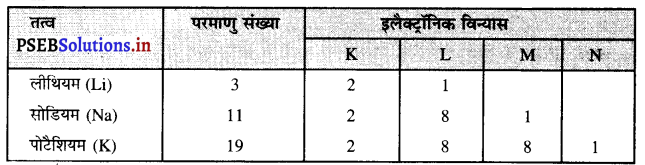
(b) दो तत्व जिनके बाहरी कोश में 2 इलैक्ट्रॉन हैं –
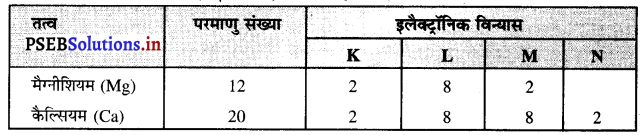
(c) ऐसे तीन तत्व जिनका बाहरी कोश पूर्ण हैंहीलियम, निऑन तथा आर्गन तीन ऐसे तत्व हैं जिनके बाहरी कोश पूर्ण हैं।
प्रश्न 4.
(a) लीथियम, सोडियम, पोटैशियम, ये सभी धातुएँ जल से अभिक्रिया कर हाइड्रोजन गैस मुक्त करती हैं। क्या इन तत्वों के परमाणुओं में कोई समानता है ?
(b) हीलियम एक अक्रियाशील गैस है जबकि निऑन की अभिक्रियाशीलता अत्यंत कम है। इनके परमाणुओं में कोई समानता है ?
उत्तर-
(a) लीथियम, सोडियम तथा पोटैशियम की जल के साथ अभिक्रिया –

इन तीनों धातुओं के बाहरी कोश में केवल एक ही इलैक्ट्रॉन है।
(b) हीलियम (He) तथा निआन (Ne) दोनों ही उत्कृष्ट गैसें हैं इसलिए ये अक्रियाशील हैं। इनके बाहरी कोश पूर्ण हैं। हीलियम (He) के पास केवल K कोश है और यह पूर्ण है पर दूसरी तरफ निआन (Ne) के पास K तथा L दो कोश हैं और ये दोनों भी पूर्ण हैं। K कोश के पास 2 तथा L कोश के पास 8 इलैक्ट्रॉन हैं। इसलिए निऑन की अभिक्रियाशीलता अत्यंत कम है।
प्रश्न 5.
आधुनिक आवर्त सारणी के पहले दस तत्वों में कौन-सी धातुएँ हैं ?
उत्तर-
आधुनिक आवर्त सारणी के पहले दस तत्व हैं- H, He, Li, Be, B, C, N, O, F तथा Ne इन सब तत्वों में से धातुएँ हैं- (लीथियम Li) तथा (बैरीलियम Be)
प्रश्न 6.
आवर्त सारणी में इनके स्थान के आधार पर इनमें से किस तत्व में सबसे अधिक धात्विक अभिलक्षण की विशेषता है ?
Ga, Ge, As, Se, Be.
उत्तर-
पहले इनका वर्गीकरण बढ़ती हुई परमाणु संख्या के अनुसार करते हैं-

हम जानते हैं कि धात्विक अभिलक्षण स्तंभ में बाएँ से दाएँ तरफ जाने पर कम होता है। इस बात को ध्यान में रखते हुए Be तथा Ga का धात्विक अभिलक्षण अधिकतम है। इसलिए दाईं तरफ वाले तत्व अधातु हैं।
