Punjab State Board PSEB 10th Class Science Book Solutions Chapter 5 ਤੱਤਾਂ ਦਾ ਆਵਰਤੀ ਵਰਗੀਕਰਨ Textbook Exercise Questions and Answers.
PSEB Solutions for Class 10 Science Chapter 5 ਤੱਤਾਂ ਦਾ ਆਵਰਤੀ ਵਰਗੀਕਰਨ
PSEB 10th Class Science Guide ਤੱਤਾਂ ਦਾ ਆਵਰਤੀ ਵਰਗੀਕਰਨ Textbook Questions and Answers
ਪ੍ਰਸ਼ਨ 1.
ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਖੱਬੇ ਤੋਂ ਸੱਜੇ ਪਾਸੇ ਵੱਲ ਜਾਣ ਨਾਲ ਤਰਤੀਬ ਬਾਰੇ ਕਿਹੜਾ ਕਥਨ ਸੱਚ ਨਹੀਂ :
(a) ਤੱਤਾਂ ਦਾ ਧਾਤਵੀ ਸੁਭਾਅ ਘੱਟਦਾ ਹੈ ।
(b) ਸੰਯੋਜਕ ਇਲੈੱਕਟਾਨਾਂ ਦੀ ਸੰਖਿਆ ਵੱਧ ਜਾਂਦੀ ਹੈ ।
(c) ਪਰਮਾਣੂ ਸੋਖ ਨਾਲ ਇਲੈੱਕਟ੍ਰਾਨਾਂ ਨੂੰ ਗੁਆ ਦਿੰਦੇ ਹਨ ।
(d) ਇਨ੍ਹਾਂ ਦੇ ਆਕਸਾਈਡ ਵਧੇਰੇ ਤੇਜ਼ਾਬੀ ਹੋ ਜਾਂਦੇ ਹਨ ।
ਉੱਤਰ-
ਕਥਨ (c) ਸੱਚ ਨਹੀਂ ਹੈ, ਕਿਉਂਕਿ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਖੱਬਿਉਂ ਸੱਜੇ ਜਾਣ ਨਾਲ ਪਰਮਾਣੂ ਦੀ ਇਲੈੱਕਟ੍ਰਾਨ ਗੁਆਉਣ ਦੀ ਸਮਰੱਥਾ ਘੱਟਦੀ ਹੈ ।
ਪ੍ਰਸ਼ਨ 2.
ਤੱਤ X, XCl2 ਸੂਤਰ ਵਾਲਾ ਇੱਕ ਕਲੋਰਾਈਡ ਬਣਾਉਂਦਾ ਹੈ ਜੋ ਕਿ ਇੱਕ ਉੱਚ ਪਿਘਲਣ ਅੰਕ ਦਾ ਠੋਸ ਹੈ । ਇਹ ਤੱਤ X ਸੰਭਵ ਤੌਰ ‘ਤੇ ਆਵਰਤੀ ਸਾਰਨੀ ਦੇ ਉਸ ਗਰੁੱਪ ਵਿੱਚ ਹੋਵੇਗਾ ਜਿਸ ਵਿੱਚ ਹੈ :
(a) Na
(b) Mg
(c) Al
(d) Si.
ਉੱਤਰ-
ਜੇਕਰ ਤੱਤ X, XCl2 ਸੂਤਰ ਦਾ ਕਲੋਰਾਈਡ ਬਣਾਉਂਦਾ ਹੈ ਤਾਂ ਤੱਤ X ਦੇ ਸੰਯੋਜਨ ਇਲੈੱਕਟ੍ਰਾਨਾਂ ਦੀ ਸੰਖਿਆ 2 ਹੋਵੇਗੀ ਅਰਥਾਤ ਉਸਦੇ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਸੰਯੋਜਕੜਾ ਇਲੈੱਕਟਾਨ ਦੀ ਸੰਖਿਆ 2 ਹੋਵੇਗੀ । ਆਵਰਤੀ ਸਾਰਨੀ ਅਨੁਸਾਰ ਸਿਰਫ ਗਰੁੱਪ 2 ਦੇ ਤੱਤ Be, Mg, Ca, Sr, Ba ਅਤੇ Pa ਦੀ ਸੰਯੋਜਕਤਾ ਇਲੈੱਕਟਾਨਾਂ ਸੰਖਿਆ 2 ਹੈ । ਇਸ ਲਈ X ਤੱਤ ਉਸ ਗਰੁੱਪ ਵਿੱਚ ਹੈ ਜਿਸ ਵਿੱਚ ਮੈਗਨੀਸ਼ੀਅਮ (Mg) ਹੈ, ਕਿਉਂਕਿ ਮੈਗਨੀਸ਼ੀਅਮ ਇੱਕ ਧਾਤ ਹੁੰਦੇ ਹੋਏ ਵੀ ਇੱਕ ਆਇਨੀ ਕਲੋਰਾਈਡ ਬਣਾਉਣ ਦੀ ਸਮਰੱਥਾ ਰੱਖਦਾ ਹੈ ਜਿਸਦਾ ਉੱਚਾ ਪਿਘਲਣ ਅੰਕ ਹੈ ।
![]()
ਪ੍ਰਸ਼ਨ 3.
ਕਿਸ ਤੱਤ ਵਿੱਚ :
(a) ਦੋ ਸੈੱਲ ਹਨ ਅਤੇ ਦੋਵੇਂ ਇਲੈੱਕਟ੍ਰਾਨਾਂ ਨਾਲ ਪੂਰੇ ਭਰੇ ਹਨ ।
(b) ਇਲੈੱਕਟ੍ਰਾਨੀ ਤਰਤੀਬ 2,8,2 ਹੈ,
(c) ਕੁੱਲ ਤਿੰਨ ਸੈੱਲ ਹਨ ਅਤੇ ਸੰਯੋਜਕ ਸੈੱਲ ਵਿੱਚ ਚਾਰ ਇਲੈਂਕਨ ਹਨ ।
(d) ਦੂਜੇ ਸੈੱਲ ਵਿੱਚ ਪਹਿਲੇ ਸੈੱਲ ਨਾਲੋਂ ਦੁੱਗਣੇ ਇਲੈਂਕਟਾਨ ਹਨ ।
ਉੱਤਰ-
(a) ਨੋਬਲ ਗੈਸਾਂ ਦੇ ਸਾਰੇ ਸੈੱਲ ਇਲੈੱਕਟਾਨ ਨਾਲ ਭਰੇ ਹੁੰਦੇ ਹਨ । ਇਸ ਲਈ ਦਿੱਤਾ ਗਿਆ ਤੱਤ ਇੱਕ ਨੋਬਲ ਤੱਤ ਗੈਸ ਹੈ ਕਿਉਂਕਿ ਇਸਦੇ ਦੋ ਸੈੱਲ ਪੂਰੀ ਤਰ੍ਹਾਂ ਭਰੇ ਹੋਏ ਹਨ । ਇਸ ਤਰ੍ਹਾਂ ਤੱਤ ਨਿਆਨ (Ne) (2,8) ਇੱਕ ਤੱਤ ਹੈ ।
(b) ਇਲੈੱਕਟ੍ਰਾਨੀ ਤਰਤੀਬ 2,8,2 ਦਾ ਜੋੜ 12 ਇਸ ਤੱਤ ਦਾ ਪਰਮਾਣੂ-ਅੰਕ ਹੈ ਅਤੇ ਪਰਮਾਣੂ ਅੰਕ 12 ਵਾਲਾ ਤੱਤ ਮੈਗਨੀਸ਼ੀਅਮ (Mg) ਹੈ । ਇਸ ਲਈ ਦਿੱਤਾ ਗਿਆ ਤੱਤ ਮੈਗਨੀਸ਼ੀਅਮ (Mg) ਹੈ ।
(c) ਕੁੱਲ ਤਿੰਨ ਸੈੱਲਾਂ ਵਿੱਚੋਂ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਇਲੈੱਕਟਾਨ ਸੰਖਿਆ 4 ਹੈ । ਇਸ ਲਈ ਤੱਤ ਦਾ ਇਲੈੱਕਟ੍ਰਾਨ ਤਰਤੀਬ ਹੈ (2,8,4) ਜਿਸਦਾ ਜੋੜ 14 ਹੈ । ਇਸ ਤਰ੍ਹਾਂ ਪਰਮਾਣੂ ਅੰਕ 14 ਵਾਲਾ ਤੱਤ ਸਿਲੀਕਾਨ (Si) ਹੈ । ਕੁੱਲ ਦੋ ਸੈੱਲ ਹਨ | ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ 3 ਇਲੈੱਕਵਾਨ ਹਨ । ਇਸ ਤਰ੍ਹਾਂ ਤੱਤ ਦਾ ਇਲੈੱਕਟਾਨੀ ਤਰਤੀਬ (2,3) ਹੈ ਅਤੇ ਤਰਤੀਬ ਇਲੈੱਕਟ੍ਰਾਨਾਂ ਦਾ ਜੋੜ 5 ਹੈ ।
ਇਸ ਲਈ ਇਲੈੱਕਟ੍ਰਾਨ ਤਰਤੀਬ ਜੋੜ 5 ਵਾਲਾ ਤੱਤ ਬੋਨ (B) ਹੈ ।
d) ਦੂਸਰੇ ਸੈੱਲ ਵਿੱਚ ਪਹਿਲੇ ਸੈੱਲ ਦੀ ਤੁਲਨਾ ਵਿੱਚ ਦੁੱਗਣੇ ਇਲੈਂਕਟਾਨ ਹਨ । ਇਸ ਲਈ ਇਲੈੱਕਟ੍ਰਾਨੀ ਤਰਤੀਬ (2,4) ਅਤੇ ਇਲੈੱਕਟ੍ਰਾਨਾਂ ਦਾ ਜੋੜ 6 ਹੈ । ਇਸ ਤਰ੍ਹਾਂ ਪਰਮਾਣੂ ਸੰਖਿਆ 6 ਵਾਲਾ ਤੱਤ ਕਾਰਬਨ (C) ਹੈ !
ਪ੍ਰਸ਼ਨ 4.
(a) ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਬੋਰਾਂਨ ਕਾਲਮ ਦੇ ਸਾਰੇ ਤੱਤਾਂ ਦਾ ਸਾਂਝਾ ਗੁਣ ਕੀ ਹੈ ?
(b) ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਫਲੋਰੀਨ ਕਾਲਮ ਦੇ ਸਾਰੇ ਤੱਤਾਂ ਦਾ ਸਾਂਝਾ ਗੁਣ ਕੀ ਹੈ ?
ਉੱਤਰ-
(a) ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਬੋਰਾਂਨ ਕਾਲਮ ਦੇ ਸਾਰੇ ਤੱਤ ਪਰਮਾਣੂ ਸੰਖਿਆ 13 ਨਾਲ ਸੰਬੰਧ ਰੱਖਦੇ ਹਨ । ਇਸ ਲਈ ਇਨ੍ਹਾਂ ਸਾਰਿਆਂ ਦੇ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਇਲੈੱਕਟ੍ਰਾਨਾਂ ਦੀ ਸੰਖਿਆ ਹੋਵੇਗੀ । ਬੋਰਾਨ (B) ਨੂੰ ਛੱਡ ਕੇ ਜੋ ਇੱਕ ਆਧਾਤ ਹੈ ਬਾਕੀ ਸਾਰੇ ਤੱਤ (Al, Ga, In ਅਤੇ Th) ਧਾਤਾਂ ਹਨ ।
(b) ਫਲੋਰੀਨ ਕਾਲਮ ਦੇ ਵਿੱਚ ਆਉਣ ਵਾਲੇ ਸਾਰੇ ਤੱਤ ਨੋਬਲ ਤੱਤ ਹਨ ਅਤੇ ਪਰਮਾਣੂ ਸੰਖਿਆ 17 ਨਾਲ ਸੰਬੰਧ ਰੱਖਦੇ ਹਨ । ਇਸ ਲਈ ਉਨ੍ਹਾਂ ਦੇ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਫਲੋਰੀ ਵਾਂਗ 7 ਇਲੈੱਕਟ੍ਰਾਨ ਹੋਣਗੇ । ਇਹ ਸਾਰੇ ਤੱਤ (F, Cl, Br, I) ਅਧਾਤਾਂ ਹਨ ।
ਪ੍ਰਸ਼ਨ 5.
ਇੱਕ ਪਰਮਾਣੂ ਦੀ ਇਲੈੱਕਟ੍ਰਾਨੀ ਤਰਤੀਬ 2,8,7 ਹੈ :
(a) ਇਸ ਤੱਤ ਦਾ ਪਰਮਾਣੁ ਅੰਕ ਕੀ ਹੈ ?
(b) ਹੇਠ ਲਿਖਿਆਂ ਵਿੱਚੋਂ ਕਿਸ ਨਾਲ ਇਸ ਦੀ ਰਸਾਇਣਿਕ ਸਮਾਨਤਾ ਹੋਵੇਗੀ ?
(ਪਰਮਾਣੂ ਅੰਕ ਬੈਕਟ ਵਿੱਚ ਦਿੱਤੇ ਗਏ ਹਨ)
N(7), F(9), P(15), Ar(18) ।
ਉੱਤਰ-
(a) ਤੱਤ ਦੀ ਪਰਮਾਣੂ ਸੰਖਿਆ = 2 + 8 +7 = 17 ਹੈ ਅਤੇ ਇਹ ਤੱਤ ਕਲੋਰੀਨ ਹੈ ।
(b) ਕਿਉਂਕਿ ਤੱਤ ਦੇ ਬਾਹਰਲੇ ਸੰਯੋਜਕਤਾ ਸੈੱਲ ਵਿੱਚ ਇਲੈੱਕਟ੍ਰਾਨਾਂ ਦੀ ਸੰਖਿਆ 7 ਹੈ । ਇਸ ਲਈ ਇਹ ਗਰੁੱਪ ਪਰਮਾਣੂ ਸੰਖਿਆ 17 ਨਾਲ ਸੰਬੰਧ ਰੱਖਦਾ ਹੈ । ਇਸ ਪਰਿਵਾਰ ਦੇ ਹੋਰ ਤੱਤਾਂ ਦੀ ਪਰਮਾਣੂ ਸੰਖਿਆ ਅਤੇ ਇਲੈੱਕਟਾਨੀ ਹੇਠ ਲਿਖੇ ਅਨੁਸਾਰ ਹੈ :-
| ਤੱਤ | ਪਰਮਾਣੂ ਸੰਖਿਆ | ਇਲੈੱਕਟਾਨੀ ਤਰਤੀਬ |
| ਫਲੋਰੀਨ (F) | 9 | 2, 7 |
| ਕਲੋਰੀਨ (Cl) | 35 | 2, 8, 18, 7 |
| ਆਇਓਡੀਨ (I) | 53 | 2, 8, 18, 18, 7 |
ਇਸ ਲਈ ਤੱਤ F(a) ਪਰਮਾਣੂ ਸੰਖਿਆ 9 ਹੋਣ ਕਾਰਨ ਨੋਬਲ ਗੈਸ ਪਰਿਵਾਰ ਨਾਲ ਸੰਬੰਧ ਰੱਖਦਾ ਹੈ । ਇਸ ਲਈ ਇਸ ਤੱਤ ਦੀ ਰਸਾਇਣਿਕ ਸਮਾਨਤਾ ਕਲੋਰੀਨ ਨਾਲ ਹੋਵੇਗੀ ।
ਪ੍ਰਸ਼ਨ 6.
ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਤਿੰਨ ਤੱਤਾਂ A, B ਅਤੇ C ਦੀ ਸਥਿਤੀ ਹੇਠ ਦਿੱਤੇ ਅਨੁਸਾਰ ਹੈ :
| ਗਰੁੱਪ 16 | ਗਰੁੱਪ 17 |
| – | – |
| – | A |
| – | – |
| B | C |
(a) ਸੋ A ਧਾਤ ਹੈ ਜਾਂ ਅਧਾਤ ਹੈ ?
(b) ਦੱਸੋ A ਦੇ ਟਾਕਰੇ ਵਿੱਚ C ਵਧੇਰੇ ਕਿਰਿਆਸ਼ੀਲ ਹੈ ਜਾਂ ਘੱਟ ਕਿਰਿਆਸ਼ੀਲ ਹੈ ?
(c) ਕੀ B ਨਾਲੋਂ c ਸਾਈਜ਼ ਵਿੱਚ ਵੱਡਾ ਹੈ ਜਾਂ ਛੋਟਾ ?
(d) ਤੱਤ A ਕਿਸ ਪ੍ਰਕਾਰ ਦਾ ਆਇਨ-ਕੇਟਆਇਨ ਜਾਂ ਐਨਆਇਨ ਬਣਾਏਗਾ ?
ਉੱਤਰ-
(a) ਗਰੁੱਪ 17 ਦੇ ਤੱਤਾਂ ਦੇ ਬਾਹਰਲੇ ਸੰਯੋਜਕਤਾ ਸੈੱਲ ਵਿੱਚ ਇਲੈੱਕਵਾਨਾਂ ਦੀ ਸੰਖਿਆ 7 ਹੈ ਅਤੇ ਸਾਰੇ ਤੱਤਾਂ ਦੀ 1 ਇਲੈੱਕਟ੍ਰਾਨ ਲੈਣ ਦੀ ਸਮਰੱਥਾ ਹੈ । ਇਸ ਲਈ ਸਾਰੇ ਤੱਤ ਅਧਾਤਾਂ ਹਨ ।
(b) ਇੱਕ ਗਰੁੱਪ ਵਿੱਚ ਹੇਠਾਂ ਵੱਲ ਆਉਣ ਨਾਲ ਪਰਮਾਣੂ ਦਾ ਸਾਈਜ਼ ਵੱਧਦਾ ਹੈ । ਇਸ ਲਈ ਨਿਊਕਲੀਅਸ ਨਾਭਿਕ) ਦੇ ਸੰਯੋਜਕਤਾ ਇਲੈੱਕਟ੍ਰਾਨਾਂ ਨੂੰ ਆਕਰਸ਼ਣ ਕਰਨ ਦੀ ਸਮਰੱਥਾ ਘੱਟ ਜਾਂਦੀ ਹੈ । ਇਸ ਤਰ੍ਹਾਂ ਕਿਰਿਆਸ਼ੀਲ ਕਿਸੇ ਗਰੁੱਪ ਵਿੱਚ ਹੇਠਾਂ ਵੱਲ ਆਉਣ ਨਾਲ ਘੱਟਦੀ ਜਾਂਦੀ ਹੈ । ਇਸ ਲਈ c ਤੱਕ, ਤੱਤ A ਦੀ ਤੁਲਨਾ ਵਿਚ ਘੱਟ ਕਿਰਿਆਸ਼ੀਲ ਹੈ ।
(c) ਤੱਤ B ਨਾਲੋਂ ਤੱਤ ਛੋਟਾ ਹੋਵੇਗਾ ।
(d) ਤੱਤ A ਰਿਆਇਨ ਬਣਾਏਗਾ ।
![]()
ਪ੍ਰਸ਼ਨ 7.
ਨਾਈਟਰੋਜਨ (ਪਰਮਾਣੂ ਅੰਕ 7) ਅਤੇ ਫਾਸਫੋਰਸ (ਪਰਮਾਣੂ ਅੰਕ 15) ਆਵਰਤੀ ਸਾਰਨੀ ਦੇ ਗਰੁੱਪ 15 ਦੇ ਤੱਤ ਹਨ । ਇਨ੍ਹਾਂ ਦੋਵੇਂ ਤੱਤਾਂ ਦੀ ਇਲੈੱਕਟ੍ਰਾਨੀ ਤਰਤੀਬ ਲਿਖੋ । ਇਨ੍ਹਾਂ ਵਿੱਚੋਂ ਕਿਹੜਾ ਤੱਤ ਵਧੇਰੇ ਰਿਣ ਬਿਜਲਈ ਹੈ ਅਤੇ ਕਿਉਂ ?
ਉੱਤਰ-
ਨਾਈਟ੍ਰੋਜਨ ਦੀ ਇਲੈੱਕਟ੍ਰਾਨੀ ਤਰਤੀਬ : ਨਾਈਟਰੋਜਨ (ਪਰਮਾਣੂ ਅੰਕ) ਜਾਂ (7) : (2,5)
ਫਾਸਫੋਰਸ ਦੀ ਇਲੈਕਟ੍ਰਾਂਨੀ ਤਰਤੀਬ : ਫਾਸਫੋਰਸ ਪਰਮਾਣੂ ਅੰਕ 15) ਜਾਂ p(15) : (2,8,5)
ਨਾਈਟਰੋਜਨ ਦੀ ਬਿਜਲਈ ਰਿਣਾਤਮਕਤਾ (ਇਲੈੱਕਟ੍ਰੋਨੈਗਟਿਵਤਾ) ਅਧਿਕ ਹੋਵੇਗੀ ਕਿਉਂਕਿ ਇਸਦਾ ਬਾਹਰਲਾ ਸੈੱਲ ਪਰਮਾਣੂ ਦੇ ਕੇਂਦਰ ਦੇ ਨੇੜੇ ਹੈ । ਇਸ ਲਈ ਪਰਮਾਣੂ ਕੇਂਦਰ ਇਲੈੱਕਨ ਨੂੰ ਅਧਿਕ ਬਲ ਨਾਲ ਆਕਰਸ਼ਿਤ ਕਰੇਗਾ ।
ਪ੍ਰਸ਼ਨ 8.
ਤੱਤਾਂ ਦੀ ਇਲੈੱਕਟ੍ਰਾਨੀ ਤਰਤੀਬ ਦਾ ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਤੱਤ ਦੀ ਸਥਿਤੀ ਨਾਲ ਕੀ ਸੰਬੰਧ ਹੈ ?
ਉੱਤਰ-
ਇਲੈੱਕਟਾਨੀ ਤਰਤੀਬ ਦਾ ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਤੱਤ ਦੀ ਸਥਿਤੀ ਨਾਲ ਸੰਬੰਧ-ਕਿਸੇ ਪਰਮਾਣੂ ਦੀ ਇਲੈੱਕਟਾਨੀ ਤਰਤੀਬ ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਇਸਦੀ ਸਥਿਤੀ ਨਾਲ ਇਸ ਤਰ੍ਹਾਂ ਸੰਬੰਧਤ ਹੈ ਕਿ ਜਿਨ੍ਹਾਂ ਪਰਮਾਣੂਆਂ ਦੇ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਇਲੈੱਕਟ੍ਰਾਨਾਂ ਦੀ ਸੰਖਿਆ ਸਮਾਨ ਹੁੰਦੀ ਹੈ ਉਨ੍ਹਾਂ ਨੂੰ ਇੱਕ ਹੀ ਗਰੁੱਪ ਵਿੱਚ ਵਿਵਸਥਿਤ ਕੀਤਾ ਜਾਂਦਾ ਹੈ । ਸਭ ਤੋਂ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਉਪਸਥਿਤ ਇਲੈੱਕਟਾਨਾਂ ਦੀ ਸੰਖਿਆ ਉਸ ਤੱਤ ਦੀ ਸਮੂਹ ਸੰਖਿਆ ਨੂੰ ਦਰਸਾਉਂਦੀ ਹੈ ਅਤੇ ਬਾਹਰਲੇ ਸੈੱਲ ਦੀ ਸੰਖਿਆ ਪੀਰੀਅਡ ਨੂੰ ਸੂਚਿਤ ਕਰਦੀ ਹੈ ।
ਜਦੋਂ ਕਿਸੇ ਪੀਰੀਅਡ ਵਿੱਚ ਖੱਬਿਓਂ ਸੱਜੇ ਵੱਲ ਜਾਂਦੇ ਹਾਂ, ਤਾਂ ਸੰਯੋਜਕਤਾ ਸੈੱਲ ਇਲੈੱਕਵਾਨਾਂ ਦੀ ਸੰਖਿਆ ਇਕਾਈ ਵੱਧ ਜਾਂਦੀ ਹੈ ।
ਪ੍ਰਸ਼ਨ 9.
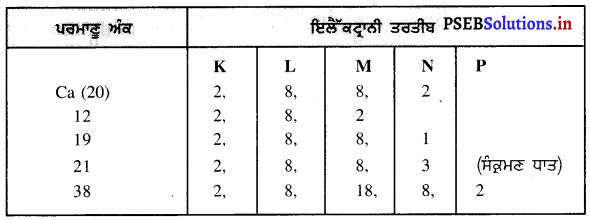
ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਕੈਲਸ਼ੀਅਮ (ਪਰਮਾਣੁ ਅੰਕ 20) ਦੇ ਚਾਰੇ ਪਾਸੇ 12, 19, 21 ਅਤੇ 38 ਪਰਮਾਣੁ ਅੰਕਾਂ ਵਾਲੇ ਤੱਤ ਮੌਜੂਦ ਹਨ । ਇਨ੍ਹਾਂ ਵਿੱਚੋਂ ਕਿਨ੍ਹਾਂ ਤੱਤਾਂ ਦੇ ਭੌਤਿਕ ਅਤੇ ਰਸਾਇਣਿਕ ਗੁਣ ਕੈਲਸ਼ੀਅਮ ਵਰਗੇ ਹਨ ?
ਉੱਤਰ-
ਪਰਮਾਣੂ ਅੰਕ 12 ਵਾਲੇ ਤੱਤ ਦੇ ਭੌਤਿਕ ਅਤੇ ਰਸਾਇਣਿਕ ਗੁਣ ਪਰਮਾਣੂ ਅੰਕ 20 ਅਤੇ 38 ਵਾਲੇ ਤੱਤਾਂ ਦੇ ਸਮਾਨ ਹੋਣਗੇ, ਕਿਉਂਕਿ ਇਨ੍ਹਾਂ ਤੱਤਾਂ ਦੇ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ 2 ਇਲੈਂਕਨ ਹਨ ।
ਪ੍ਰਸ਼ਨ 10.
ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਅਤੇ ਮੈਂਡਲੀਵ ਦੀ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਤੱਤਾਂ ਦੀ ਤਰਤੀਬ ਦੀ ਤੁਲਨਾ ਕਰੋ !
ਉੱਤਰ-
ਮੈਂਡਲੀਵ ਦੀ ਆਵਰਤੀ ਸਾਰਨੀ ਦੀ ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਨਾਲ ਤੁਲਨਾ-ਮੈਂਡਲੀਵ ਦੀ ਆਵਰਤੀ ਸਾਰਨੀ ਅਤੇ ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਤੱਤਾਂ ਨੂੰ ਇੱਕ ਸਮਾਨ ਸਾਰ ਦੇ ਰੂਪ ਵਿੱਚ ਥਾਂ ਦਿੱਤੀ ਗਈ ਹੈ । ਦੋਨਾਂ ਸਾਰਨੀਆਂ ਵਿੱਚ ਇੱਕ ਸਮਾਨ ਗੁਣਾਂ ਵਾਲੇ ਤੱਤਾਂ ਨੂੰ ਇਕੱਠੀ ਗਰੁੱਪ ਵਿੱਚ ਰੱਖਿਆ ਗਿਆ ਹੈ ਪਰੰਤੂ ਇਨ੍ਹਾਂ ਦੋਨਾਂ ਵਿੱਚ ਕਾਫ਼ੀ ਸਮਾਨਤਾਵਾਂ ਹਨ; ਜਿਵੇਂ :-
| ਮੈਂਡਲੀਵ ਦੀ ਆਵਰਤੀ ਸਾਰਨੀ | ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ |
| (1) ਉਸ ਸਮੇਂ ਤੱਕ ਗਿਆਤ 63 ਤੱਤਾਂ ਨੂੰ ਵੱਧਦੇ ਪਰਮਾਣੂ ਪੂੰਜਾਂ ਵਿੱਚ ਵਿਵਸਥਿਤ ਕੀਤਾ ਗਿਆ । | (1) ਕੁੱਲ 118 ਤੱਤਾਂ ਨੂੰ ਵੱਧਦੇ ਪਰਮਾਣੁ ਅੰਕ ਵਿੱਚ ਵਿਵਸਥਿਤ ਕੀਤਾ ਗਿਆ ਹੈ । |
| (2) ਇਸ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ 8 ਲੰਬੇ ਦਾਅ ਦੇ ਸਤੰਭ ਹਨ ਜਿਨ੍ਹਾਂ ਨੂੰ ਗਰੁੱਪ ਕਹਿੰਦੇ ਹਨ । | (2) ਇਸ ਵਿੱਚ 18 ਖੜ੍ਹਵੇਂ ਕਾਲਮ ਹਨ, ਜਿਨ੍ਹਾਂ ਨੂੰ ਗਰੁੱਪ ਕਹਿੰਦੇ ਹਨ ਅਤੇ 7 ਪੀਰੀਅਡ ਹਨ । |
| (3) ਤੱਤਾਂ ਦੇ ਆਈਸੋਟੋਪ ਨੂੰ ਸਾਰਨੀ ਵਿੱਚ ਸਥਾਨ ਨਾ ਮਿਲ ਸਕਿਆ । | (3) ਤੱਤਾਂ ਦੇ ਆਈਸੋਟੋਪਾਂ ਨੂੰ ਆਵਰਤੀ ਵਿੱਚ ਉੱਚਿਤ ਸਥਾਨ ਪ੍ਰਾਪਤ ਹੋਇਆ ਕਿਉਂਕਿ ਉਨ੍ਹਾਂ ਦੇ ਪਰਮਾਣੂ ਅੰਕ ਇੱਕ ਸਮਾਨ ਹੁੰਦੇ ਹਨ । |
| (4) ਰਸਾਇਣਿਕ ਦ੍ਰਿਸ਼ਟੀ ਨਾਲ ਅਸਮਾਨ ਤੱਤਾਂ ਨੂੰ ਵੀ ਇਕੱਠਾ ਰੱਖਿਆ ਗਿਆ | | (4) ਰਸਾਇਣਿਕ ਦ੍ਰਿਸ਼ਟੀ ਤੋਂ ਅਸਮਾਨ ਤੱਤਾਂ ਨੂੰ ਵੱਖ-ਵੱਖ ਗਰੁੱਪਾਂ ਵਿੱਚ ਸਥਾਨ ਦਿੱਤਾ ਗਿਆ ਹੈ । |
| (5) ਸਾਰੇ ਪਰਿਵਰਤਿਤ ਤੱਤਾਂ ਨੂੰ ਇੱਕ ਹੀ ਗਰੁੱਪ VII ਵਿੱਚ ਰੱਖਿਆ ਗਿਆ । | (5) ਪਰਿਵਰਤਿਤ ਤੱਤਾਂ ਨੂੰ ਗਰੁੱਪ 3 ਅਤੇ ਗਰੁੱਪ 12 ਵਿੱਚ ਰੱਖਿਆ ਗਿਆ ਹੈ । |
| (6) ਇਸ ਸਾਰਨੀ ਦੇ ਬਣਨ ਤੱਕ ਨੋਬਲ ਗੈਸਾਂ ਦੀ ਖੋਜ ਨਹੀਂ ਹੋਈ ਸੀ । | (6) ਨੋਬਲ ਗੈਸਾਂ ਨੂੰ ਗਰੁੱਪ 18 ਵਿੱਚ ਸਥਾਨ ਦਿੱਤਾ ਗਿਆ ਹੈ । |
| (7) ਕੁੱਝ ਉੱਚ ਪੁੰਜ ਵਾਲੇ ਤੱਤਾਂ ਨੂੰ ਉਨ੍ਹਾਂ ਤੱਤਾਂ ਤੋਂ ਪਹਿਲਾਂ ਥਾਂ ਦਿੱਤੀ ਗਈ ਜਿਨ੍ਹਾਂ ਦਾ ਪਰਮਾਣੂ ਪੁੰਜ ਘੱਟ ਸੀ । | (7) ਇਸ ਸਾਰਨੀ ਵਿੱਚ ਵਰਗੀਕਰਨ ਦਾ ਆਧਾਰ ਪਰਮਾਣੂ ਅੰਕ ਹੈ, ਇਸ ਲਈ ਇਸ ਵਿੱਚ ਕੋਈ ਉਲਟੇ ਕੂਮ ਦਾ ਦੋਸ਼ ਨਹੀਂ ਹੈ । |
Science Guide for Class 10 PSEB ਤੱਤਾਂ ਦਾ ਆਵਰਤੀ ਵਰਗੀਕਰਨ InText Questions and Answers
ਅਧਿਆਇ ਦੇ ਅੰਦਰ ਦਿੱਤੇ ਗਏ ਪ੍ਰਸ਼ਨ ਅਤੇ ਉਨ੍ਹਾਂ ਦੇ ਉੱਤਰ
ਪ੍ਰਸ਼ਨ 1.
ਕੀ ਡਾਬਰਨੀਅਰ ਦੀਆਂ ਤਿੱਕੜੀਆਂ ਨਿਊਲੈਂਡ ਦੇ ਅਸ਼ਟਕਾਂ ਵਿੱਚ ਵੀ ਮਿਲਦੀਆਂ ਹਨ ? ਤੁਲਨਾ ਕਰਕੇ ਪਤਾ ਕਰੋ ।
ਉੱਤਰ-
ਹਾਂ, ਡਾਬਰਨੀਅਰ ਦੀਆਂ ਤਿੱਕੜੀਆਂ ਨਿਊਲੈਂਡ ਦੇ ਅਸ਼ਟਕਾਂ ਵਿੱਚ ਵੀ ਮਿਲਦੀਆਂ ਹਨ । ਉਦਹਾਰਨ ਵਜੋਂ (i) ਲਿਥੀਅਮ (Li), ਸੋਡੀਅਮ (Na) ਅਤੇ ਪੋਟਾਸ਼ੀਅਮ (K) ਇੱਕ ਡਾਬਰਨੀਅਰ ਦੀ ਤਿੱਕੜੀ ਬਣਾਉਂਦੇ ਹਨ । ਜੇਕਰ ਲਿਥੀਅਮ (Li) ਨੂੰ ਪਹਿਲਾ ਤੱਤ ਮੰਨ ਲਿਆ ਜਾਏ ਤਾਂ ਉਸ ਤੋਂ ਅੱਠਵੇਂ ਸਥਾਨ ਤੇ ਸੋਡੀਅਮ (Na) ਆਉਂਦਾ ਹੈ ਅਤੇ ਜੇਕਰ ਸੋਡੀਅਮ (Na) ਨੂੰ ਪਹਿਲਾ ਤੱਤ ਮੰਨ ਲਿਆ ਜਾਵੇ ਤਾਂ ਇਸ ਤੋਂ ਅੱਠਵੇਂ ਸਥਾਨ ਤੇ ਪੋਟਾਸ਼ੀਅਮ (K) ਆਉਂਦਾ ਹੈ । ਇਸ ਤਰ੍ਹਾਂ ਡਾਬਰਨੀਅਰ ਦੀ ਇਹ ਤਿੱਕੜੀ ਨਿਊਲੈਂਡਸ ਅਸ਼ਟਕ ਦੀ ਤਿੱਕੜੀ ‘ਰੇ ਵਿੱਚ ਮਿਲਦਾ ਹੈ ।

(ii) ਡਾਬਰਨੀਅਰ ਦੀ ਤਿੱਕੜੀ Ca, Sr ਅਤੇ B ਨਿਊਲੈਂਡਸ ਦੇ ਅਸ਼ਟਕ ਦੀ ਤਿੱਕੜੀ ‘ਸਾ’ ਵਿੱਚ ਮੌਜੂਦ ਹੈ ।
(iii) ਡਾਬਰਨੀਅਰ ਦੀ ਤਿੱਕੜੀ Cl, Br ਅਤੇ 1 ਨਿਊਲੈਂਡਸ ਦੇ ਅਸ਼ਟਕ ਦੀ ਤਿੱਕੜੀ ‘ਸਾ’ ਵਿੱਚ ਉਪਸਥਿਤ ਹੈ ।
ਪ੍ਰਸ਼ਨ 2.
ਡਾਬਰਨੀਅਰ ਦੇ ਵਰਗੀਕਰਨ ਦੀਆਂ ਕੀ ਸੀਮਾਵਾਂ ਹਨ ?
ਉੱਤਰ-
ਡਾਬਰਨੀਅਰ ਦੇ ਵਰਗੀਕਰਨ ਦੀਆਂ ਸੀਮਾਵਾਂ-ਡਾਬਰਨੀਅਰ ਵਰਗੀਕਰਨ ਦੀ ਸਭ ਤੋਂ ਵੱਡੀ ਸੀਮਾ ਇਹ ਸੀ ਕਿ ਇਸ ਨਿਯਮ ਦੇ ਅਨੁਸਾਰ ਉਸ ਸਮੇਂ ਦੇ ਗਿਆਤ 30 ਤੱਤਾਂ ਵਿੱਚੋਂ ਕੇਵਲ 9 ਤੱਤਾਂ ਨੂੰ ਹੀ ਤਿੰਨ ਤਿੱਕੜੀਆਂ ਵਿੱਚ ਵਿਵਸਥਿਤ ਕੀਤਾ ਜਾ ਸਕਿਆ ਸੀ । ਇਸ ਲਈ ਇਹ ਵਰਗੀਕਰਨ ਸਭ ਨੂੰ ਮਨਜ਼ੂਰ ਨਹੀਂ ਹੋਇਆ ।
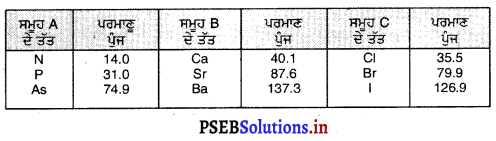
ਉਦਾਹਰਨ – ਤਿੰਨ ਤੱਤ, ਨਾਈਟ੍ਰੋਜਨ (N), ਫਾਸਫ਼ੋਰਸ (P) ਅਤੇ ਆਰਸੈਨਿਕ (As) ਦੇ ਰਸਾਇਣਿਕ ਇੱਕ ਸਮਾਨ ਹਨ, ਇਸ ਲਈ ਇਨ੍ਹਾਂ ਦੀ ਇੱਕ ਹੀ ਤਿੱਕੜੀ ਬਣਨੀ ਚਾਹੀਦੀ ਹੈ ਜਦਕਿ N, ਦਾ ਪਰਮਾਣੂ-ਪੁੰਜ (14.0u), As ਦਾ (74.9u) ਅਤੇ P ਦਾ (31.Ou) ਹੈ ।
ਇਸ ਦੇ ਅਨੁਸਾਰ ਇਹ ਇੱਕ ਤਿੱਕੜੀ ਦੇ ਤੱਤ ਨਹੀਂ ਹਨ ।
ਪ੍ਰਸ਼ਨ 3.
ਨਿਊਲੈਂਡ ਦੇ ਅਸ਼ਟਕ ਸਿਧਾਂਤ ਦੀਆਂ ਕੀ ਸੀਮਾਵਾਂ ਹਨ ?
ਉੱਤਰ-
ਨਿਊਲੈਂਡ ਦੇ ਅਸ਼ਟਕ ਸਿਧਾਂਤ ਦੀਆਂ ਸੀਮਾਵਾਂ-ਨਿਊਲੈਂਡ ਦੇ ਅਸ਼ਟਕ ਸਿਧਾਂਤ ਦੀਆਂ ਹੇਠ ਲਿਖੀਆਂ ਸੀਮਾਵਾਂ ਹਨ-
(i) ਇਹ ਸਿਧਾਂਤ ਸਿਰਫ਼ ਕੈਲਸ਼ੀਅਮ ਤੱਕ ਹੀ ਲਾਗੂ ਹੋ ਸਕਿਆ ਕਿਉਂਕਿ ਕੈਲਸ਼ੀਅਮ ਤੋਂ ਬਾਅਦ ਆਉਣ ਵਾਲੇ ਹਰੇਕ ਅੱਠਵੇਂ ਤੱਤ ਦੇ ਗੁਣ ਪਹਿਲੇ ਤੱਤ ਦੇ ਸਮਾਨ ਨਹੀਂ ਸੀ ।
(ii) ਨਿਉਲੈਂਡ ਨੇ ਕਲਪਨਾ ਕੀਤੀ ਸੀ ਕਿ ਕੁਦਰਤ ਵਿੱਚ ਕੇਵਲ 56 ਤੱਤ ਹਨ ਅਤੇ ਭਵਿੱਖ ਵਿੱਚ ਕੋਈ ਨਵਾਂ ਤੱਤ ਨਹੀਂ ਮਿਲੇਗਾ | ਪਰੰਤੂ ਬਾਅਦ ਵਿੱਚ ਕਈ ਹੋਰ ਨਵੇਂ ਤੱਤਾਂ ਦੀ ਖੋਜ ਕੀਤੀ ਗਈ ਜਿਨ੍ਹਾਂ ਦੇ ਗੁਣ ਅਸ਼ਟਕ ਨਿਯਮ ਅਨੁਸਾਰ ਨਹੀਂ ਸਨ । ਇਸ ਕਾਰਨ ਇਸ ਨਿਯਮ ਵਿੱਚ ਵਿਵਸਥਿਤ ਨਹੀਂ ਹੋ ਸਕੇ ।
(iii) ਨਿਊਲੈਂਡ ਨੇ ਆਪਣੀ ਸਾਰਨੀ ਵਿੱਚ ਤੱਤਾਂ ਨੂੰ ਸੰਯੋਜਿਤ ਕਰਨ ਲਈ ਦੋ ਤੱਤਾਂ ਨੂੰ ਇਕੱਠਿਆਂ ਇੱਕ ਥਾਂ ‘ਤੇ ਰੱਖ ਲਿਆ ਅਤੇ ਕੁਝ ਅਸਮਾਨ ਤੱਤਾਂ ਨੂੰ ਇੱਕ ਥਾਂ ‘ਤੇ ਰੱਖਿਆ ਸੀ ।
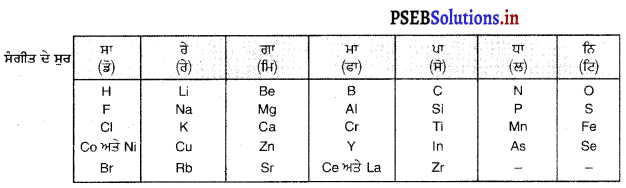
ਉਦਾਹਰਨ – ਕੋਬਾਲਟ ਅਤੇ ਨਿੱਕਲ ਨੂੰ ਇੱਕ ਹੀ ਥਾਂ ‘ਤੇ ਰੱਖਿਆ ਗਿਆ ਪਰੰਤੂ ਉਨ੍ਹਾਂ ਨੂੰ ਫਲੋਰੀਨ, ਕਲੋਰੀਨ ਅਤੇ ਬੋਮੀਨ ਦੇ ਨਾਲ ਇੱਕ ਹੀ ਤਿੱਕੜੀ ‘ਸਾ’ ਵਿੱਚ ਰੱਖਿਆ ਗਿਆ ਹੈ ਜਦਕਿ ਕੋਬਾਲਟ ਅਤੇ ਨਿਕਲ ਦੇ ਗੁਣ ਫਲੋਰੀਨ, ਕਲੋਰੀਨ ਅਤੇ ਬੋਮੀਨ ਤੋਂ ਬਿਲਕੁਲ ਭਿੰਨ ਹਨ । ਦੂਜੇ ਪਾਸੇ ਆਇਰਨ ਜੋ ਗੁਣ ਵਿੱਚ ਕੋਬਾਲਟ ਅਤੇ ਨਿਕਲ ਦੇ ਸਮਾਨ ਹਨ ਨੂੰ ਇਨ੍ਹਾਂ ਤੋਂ ਦੂਰ ਤਿੱਕੜੀ ਵਿੱਚ ਰੱਖਿਆ ਗਿਆ ਹੈ ।
(iv) ਨਿਊਲੈਂਡ ਅਸ਼ਟਕ ਸਿਧਾਂਤ ਸਿਰਫ਼ ਹਲਕੇ ਤੱਤਾਂ ਦੇ ਲਈ ਠੀਕ ਤਰ੍ਹਾਂ ਲਾਗੂ ਹੋ ਸਕਿਆ ।
ਪ੍ਰਸ਼ਨ 4.
ਮੈਂਡਲੀਵ ਦੀ ਆਵਰਤੀ ਸਾਰਨੀ ਦੀ ਵਰਤੋਂ ਕਰਕੇ ਹੇਠ ਲਿਖੇ ਤੱਤਾਂ ਦੇ ਆਕਸਾਈਡਾਂ ਦੇ ਸੂਤਰਾਂ ਦਾ ਅਨੁਮਾਨ ਲਗਾਓ :
K, C, Al, Si, Ba.
ਉੱਤਰ-
- ਪੋਟਾਸ਼ੀਅਮ (K) ਗਰੁੱਪ IA ਦਾ ਤੱਤ ਹੈ । ਇਸਦੀ ਸੰਯੋਜਕਤਾ 1 ਹੈ । ਇਸ ਲਈ ਇਸ ਦੇ ਆਕਸਾਈਡ ਦਾ ਸੂਤਰ K20 ਹੈ ।
- ਕਾਰਬਨ (C) ਗਰੁੱਪ IV A ਦਾ ਤੱਤ ਹੈ । ਇਸ ਦੀ ਸੰਯੋਜਕਤਾ 4 ਹੈ । ਇਸ ਲਈ ਇਸ ਦੇ ਆਕਸਾਈਡ ਦਾ ਸੂਤਰ CO2 ਹੈ ।
- ਐਲੂਮੀਨੀਅਮ (Al) ਗਰੁੱਪ IIIA ਦਾ ਤੱਤ ਹੈ । ਇਸ ਦੀ ਸੰਯੋਜਕਤਾ 3 ਹੈ । ਇਸ ਲਈ ਇਸ ਦੇ ਆਕਸਾਈਡ ਦਾ ਸੂਤਰ Al2O3 ਹੈ ।
- ਸਿਲੀਕਾਨ (Si), ਗਰੁੱਪ IVA ਦਾ ਤੱਤ ਹੈ । ਇਸ ਦੀ ਸੰਯੋਜਕਤਾ 4 ਹੈ । ਇਸ ਲਈ ਇਸ ਦੇ ਆਕਸਾਈਡ ਦਾ ਸੂਤਰ SiO2 ਹੈ ।
- ਬੇਰੀਅਮ (Ba) ਗਰੁੱਪ IIA ਦਾ ਤੱਤ ਹੈ । ਇਸ ਦੀ ਸੰਯੋਜਕਤਾ 2 ਹੈ । ਇਸ ਲਈ ਇਸ ਦੇ ਆਕਸਾਈਡ ਦਾ ਸੂਤਰ BaO ਹੈ ।
![]()
ਪ੍ਰਸ਼ਨ 5.
ਗੈਲੀਅਮ ਤੋਂ ਇਲਾਵਾ ਕਿਹੜੇ ਕਿਹੜੇ ਤੱਤਾਂ ਦੀ ਖੋਜ ਕੀਤੀ ਜਾ ਚੁੱਕੀ ਹੈ ਜਿਨ੍ਹਾਂ ਲਈ ਮੈਂਡਲੀਵ ਨੇ ਆਪਣੀ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਖ਼ਾਲੀ ਥਾਂਵਾਂ ਛੱਡ ਦਿੱਤੀਆਂ ਸਨ (ਕੋਈ ਦੋ ?
ਉੱਤਰ-
ਗੈਲੀਅਮ ਤੋਂ ਇਲਾਵਾ ਦੋ ਹੋਰ ਤੱਤ ਸਕੈਂਡੀਅਮ ਅਤੇ ਜਰਮੇਨੀਅਮ ਹਨ ਜਿਨ੍ਹਾਂ ਦੀ ਖੋਜ ਕੀਤੀ ਜਾ ਚੁੱਕੀ ਹੈ । ਇਨ੍ਹਾਂ ਤੱਤਾਂ ਦੇ ਲਈ ਮੈਂਡਲੀਵ ਨੇ ਆਪਣੀ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਪਹਿਲਾਂ ਤੋਂ ਹੀ ਖਾਲੀ ਸਥਾਨ ਛੱਡਿਆ ਹੋਇਆ ਸੀ । ਮੈਂਡਲੀਵ ਨੇ ਪਹਿਲਾਂ ਹੀ ਇਨ੍ਹਾਂ ਤੱਤਾਂ ਦੇ ਗੁਣਾਂ ਦਾ ਅਨੁਮਾਨ ਲਗਾ ਲਿਆ ਸੀ । ਜਦੋਂ ਬਾਅਦ ਵਿੱਚ ਇਨ੍ਹਾਂ ਤੱਤਾਂ ਦੀ ਖੋਜ ਹੋਈ ਤਾਂ ਉਨ੍ਹਾਂ ਦੇ ਉਹੀ ਗੁਣ ਸਨ ਜਿਨ੍ਹਾਂ ਦਾ ਮੈਂਡਲੀਵ ਕੇ ਅਨੁਮਾਨ ਲਗਾਇਆ ਸੀ ।
ਪ੍ਰਸ਼ਨ 6.
ਮੈਂਡਲੀਵ ਨੇ ਆਪਣੀ ਆਵਰਤੀ ਸਾਰਨੀ ਤਿਆਰ ਕਰਨ ਲਈ ਕਿਹੜਾ ਮਾਪਦੰਡ ਅਪਣਾਇਆ ?
ਉੱਤਰ-
ਮੈਂਡਲੀਵ ਆਵਰਤੀ ਸਾਰਨੀ ਲਈ ਮਾਪਦੰਡ-
- ਤੱਤਾਂ ਨੂੰ ਉਨ੍ਹਾਂ ਦੇ ਵੱਧਦੇ ਪਰਮਾਣੂ ਪੁੰਜ ਦੇ ਕੂਮ ਵਿੱਚ ਵਿਵਸਥਿਤ ਕੀਤਾ ।
- ਸਮਾਨ ਗੁਣਾਂ ਵਾਲੇ ਤੱਤਾਂ ਨੂੰ ਇੱਕ ਸਮੂਹ ਵਿੱਚ ਰੱਖਣ ਦੀ ਕੋਸ਼ਿਸ਼ ਕੀਤੀ ।
- ਤੱਤਾਂ ਦੇ ਆਕਸਾਈਡਾਂ ਅਤੇ ਹਾਈਡਰਾਈਡਾਂ ਦੇ ਅਣੂ ਸੂਤਰ ਨੂੰ ਇੱਕ ਮੂਲ ਗੁਣ ਮੰਨ ਕੇ ਤੱਤਾਂ ਦਾ ਵਰਗੀਕਰਨ ਕੀਤਾ ।
ਪ੍ਰਸ਼ਨ 7.
ਤੁਹਾਡੇ ਵਿਚਾਰ ਅਨੁਸਾਰ ਨੋਬਲ ਗੈਸਾਂ ਨੂੰ ਵੱਖਰੇ ਗਰੁੱਪ ਵਿੱਚ ਕਿਉਂ ਰੱਖਿਆ ਗਿਆ ?
ਉੱਤਰ-
ਨੋਬਲ ਗੈਸਾਂ ਨੂੰ ਵੱਖਰੇ ਗਰੁੱਪ ਵਿੱਚ ਰੱਖਣਾ-ਸਾਰੇ ਤੱਤਾਂ ਵਿਚੋਂ ਨੋਬਲ ਗੈਸਾਂ-ਹੀਲੀਅਮ (He), ਨੀਆਨ (Ne), ਆਰਗਾਨ (Ar), ਕ੍ਰਿਪਾਨ (Kr) ਅਤੇ ਜ਼ੀਨਾਨ (Xe) ਅਕਿਰਿਆਸ਼ੀਲ ਹਨ । ਇਨ੍ਹਾਂ ਦੇ ਗੁਣ ਹੋਰ ਗਰੁੱਪ ਤੱਤਾਂ ਨਾਲ ਨਹੀਂ ਮਿਲਦੇ ਹਨ । ਇਸ ਲਈ ਨੋਬਲ ਗੈਸਾਂ ਨੂੰ ਵੱਖਰੇ ਗਰੁੱਪ ਵਿੱਚ ਰੱਖਿਆ ਗਿਆ ਜਿਸ ਨੂੰ ਜ਼ੀਰੋ (0) ਗਰੁੱਪ ਕਿਹਾ ਜਾਂਦਾ ਹੈ ।
ਪ੍ਰਸ਼ਨ 8.
ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਦੁਆਰਾ ਕਿਸ ਤਰ੍ਹਾਂ ਮੈਂਡਲੀਵ ਦੀ ਆਵਰਤੀ ਸਾਰਨੀ ਦੀਆਂ ਭਿੰਨ ਭਿੰਨ ਖਾਮੀਆਂ ਨੂੰ ਦੂਰ ਕੀਤਾ ਗਿਆ ?
ਉੱਤਰ-
ਮੈਂਡਲੀਵ ਦੀ ਆਵਰਤੀ ਸਾਰਨੀ ਦਾ ਆਧਾਰ ਪਰਮਾਣੂ ਪੁੰਜ (Atomic Mass) ਹੈ, ਜਦੋਂ ਕਿ ਮੋਸਲੇ ਨੇ ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਲਈ ਪਰਮਾਣੂ ਸੰਖਿਆ (Atomic Number) ਨੂੰ ਆਧਾਰ ਮੰਨਿਆ । ਇਸ ਤਰ੍ਹਾਂ ਆਧੁਨਿਕ ਸਾਰਨੀ ਵਿੱਚ ਮੈਂਡਲੀਫ਼ ਵੱਲੋਂ ਦਿੱਤੀ ਗਈ ਸਾਰਨੀ ਦੀਆਂ ਤਰੁੱਟੀਆਂ ਨੂੰ ਦੂਰ ਕੀਤਾ ਗਿਆ ਹੈ ।
- ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਸਾਰੇ ਸਮਸਥਾਨਿਕਾਂ ਨੂੰ ਇੱਕੋ ਹੀ ਸਥਾਨ ਦਿੱਤਾ ਗਿਆ ਹੈ ਕਿਉਂਕਿ ਉਨ੍ਹਾਂ ਵਿੱਚ ਪ੍ਰੋਟਾਨਾਂ ਦੀ ਸੰਖਿਆ ਹਮੇਸ਼ਾ ਬਰਾਬਰ ਹੁੰਦੀ ਹੈ ।
- ਆਰਗਾਨ ਅਤੇ ਪੋਟਾਸ਼ੀਅਮ ਦੀ ਪਰਮਾਣੂ ਸੰਖਿਆ ਲੜੀਵਾਰ 18 ਤੇ 19 ਹੈ । ਤੱਤਾਂ ਦੀ ਵੱਧਦੀ ਹੋਈ ਪਰਮਾਣੂ ਸੰਖਿਆ ਦੇ ਆਧਾਰ ‘ਤੇ ਵਿਵਸਥਿਤ ਕਰਨ ਤੇ ਆਰਗਾਨ ਪਹਿਲਾਂ ਆ ਜਾਂਦਾ ਹੈ ਅਤੇ ਪੋਟਾਸ਼ੀਅਮ ਦਾ ਸਥਾਨ ਪਿੱਛੇ ਰਹਿ ਜਾਂਦਾ ਹੈ ਜਦੋਂ ਕਿ ਉਨ੍ਹਾਂ ਦੋਵਾਂ ਤੱਤਾਂ ਦੇ ਪੁੰਜ ਇਸਦੇ ਉਲਟ ਹਨ । ਨਵੀਂ ਸਾਰਨੀ ਵਿੱਚ ਇਸ ਦੋਸ਼ ਨੂੰ ਦੂਰ ਕੀਤਾ ਗਿਆ ਹੈ ।
- ਆਧੁਨਿਕ ਸਾਰਨੀ ਵਿੱਚ ਤੱਤਾਂ, ਨੋਬਲ ਗੈਸਾਂ (ਅਕਿਰਿਆਸ਼ੀਲ ਗੈਸਾਂ) ਅਤੇ ਮਿਸ਼ਰਤ ਤੱਤਾਂ (Alloys) ਨੂੰ ਸਪੱਸ਼ਟ ਤੌਰ ‘ਤੇ ਵੱਖ-ਵੱਖ ਕੀਤਾ ਗਿਆ ਹੈ ।
- ਆਧੁਨਿਕ ਸਾਰਨੀ ਇਹ ਵੀ ਸਪੱਸ਼ਟ ਕਰਦੀ ਹੈ ਕਿ ਤੱਤਾਂ ਦੇ ਗੁਣਾਂ ਵਿੱਚ ਆਵਰਤਤਾ ਕਿਉਂ ਹੁੰਦੀ ਹੈ ।
ਪ੍ਰਸ਼ਨ 9.
ਮੈਗਨੀਸ਼ੀਅਮ ਦੀ ਤਰ੍ਹਾਂ ਰਸਾਇਣਿਕ ਕਿਰਿਆਸ਼ੀਲਤਾ ਦਿਖਾਉਣ ਵਾਲੇ ਦੋ ਤੱਤਾਂ ਦੇ ਨਾਂ ਦੱਸੋ । ਤੁਹਾਡੀ ਚੋਣ ਦਾ ਕੀ ਅਧਾਰ ਹੈ ?
ਉੱਤਰ-
ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਅਨੁਸਾਰ, ਜਿਨ੍ਹਾਂ ਤੱਤਾਂ ਦੇ ਬਾਹਰਲੇ ਇਲੈੱਕਟਰਾਨੀ ਬਣਤਰ ਸਮਾਨ ਹੁੰਦੀ ਹੈ ਅਤੇ ਉਨ੍ਹਾਂ ਦੇ ਗੁਣ ਵੀ ਸਮਾਨ ਹੁੰਦੇ ਹਨ । ਮੈਗਨੀਸ਼ੀਅਮ ਦੇ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਦੋ ਇਲੈੱਕਟਰਾਨ ਹਨ । ਇਸ ਲਈ ਉਹ ਸਾਰੇ ਤੱਤ ਜਿਨ੍ਹਾਂ ਦੇ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ 2 ਸੰਯੋਜਕ ਇਲੈੱਕਟਰਾਨ ਹੋਣਗੇ Mg ਦੇ ਸਮਾਨ ਹੀ ਗੁਣ ਪ੍ਰਦਰਸ਼ਿਤ ਕਰਨਗੇ ।
ਉਦਾਹਰਨ – ਕੈਲਸ਼ੀਅਮ (Ca), ਪਰਮਾਣੂ ਸੰਖਿਆ = 20
ਵਿਭਿੰਨ ਸੈੱਲਾਂ ਵਿੱਚ ਇਲੈੱਕਟਰਾਨ ਵਿਵਸਥਾ = (2, 8, 9, 2)
ਮੈਗਨੀਸ਼ੀਅਮ (Mg), ਪਰਮਾਣੂ ਸੰਖਿਆ = 12
ਵਿਭਿੰਨ ਸੈੱਲਾਂ ਵਿੱਚ ਇਲੈੱਕਟਰਾਨ ਵਿਵਸਥਾ = (2, 8, 2)
ਪ੍ਰਸ਼ਨ 10.
ਨਾਂ ਦੱਸੋ :
(a) ਤਿੰਨ ਤੱਤ ਜਿਨ੍ਹਾਂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਇੱਕ ਇਲੈੱਕਟਰਾਨ ਹਾਜ਼ਰ ਹਨ ।
(b) ਦੋ ਤੱਤ ਜਿਨ੍ਹਾਂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਦੋ ਇਲੈੱਕਟਰਾਨ ਮੌਜੂਦ ਹਨ ।
(c) ਤਿੰਨ ਤੱਤ ਜਿਨ੍ਹਾਂ ਦਾ ਬਾਹਰੀ ਸ਼ੈਲ ਪੁਰਾ ਹੈ ।
ਉੱਤਰ-
(a) ਤਿੰਨ ਤੱਤ ਜਿਨ੍ਹਾਂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਇੱਕ ਇਲੈੱਕਟਰਾਨ ਮੌਜੂਦ ਹਨ-ਲਿਥੀਅਮ (Li), ਸੋਡੀਅਮ (Na) ਅਤੇ ਪੋਟਾਸ਼ੀਅਮ (K) ਤਿੰਨ ਅਜਿਹੇ ਤੱਤ ਹਨ ਜਿਨ੍ਹਾਂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਇੱਕ ਇਲੈੱਕਟਰਾਨ ਹੁੰਦਾ ਹੈ ।
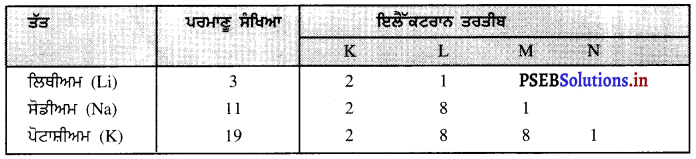
(b) ਦੋ ਤੱਤ ਜਿਨ੍ਹਾਂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਦੋ ਇਲੈੱਕਟਰਾਨ ਉਪਸਥਿਤ ਹਨ – ਮੈਗਨੀਸ਼ੀਅਮ ਅਤੇ ਕੈਲਸ਼ੀਅਮ ਦੋ ਅਜਿਹੇ ਤੱਤ ਹਨ ਜਿਨ੍ਹਾਂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਦੋ ਇਲੈੱਕਟਰਾਨ ਹਨ ।
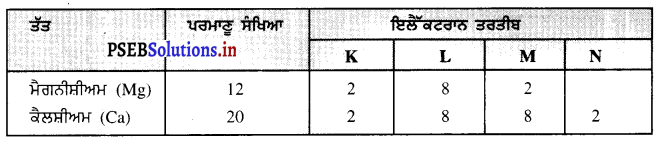
(c) ਤਿੰਨ ਤੱਤ ਜਿਨ੍ਹਾਂ ਦਾ ਬਾਹਰੀ ਸੈੱਲ ਪੂਰਾ ਹੋਵੇ-
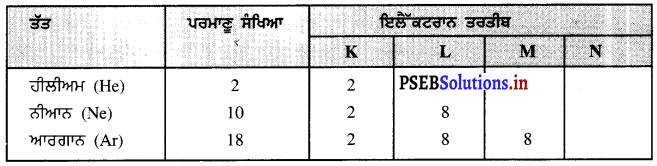
ਹੀਲੀਅਮ, ਨੀਆਨ ਅਤੇ ਆਰਗਾਨ ਤਿੰਨ ਅਜਿਹੇ ਤੱਤ ਹਨ ਜਿਨ੍ਹਾਂ ਦਾ ਬਾਹਰੀ ਛਿੱਲ ਪੂਰਾ ਹੁੰਦਾ ਹੈ ।
![]()
ਪ੍ਰਸ਼ਨ 11.
(a) ਲਿਥੀਅਮ, ਸੋਡੀਅਮ, ਪੋਟਾਸ਼ੀਅਮ ਸਾਰੀਆਂ ਹੀ ਧਾਤਾਂ ਹਨ ਜੋ ਪਾਣੀ ਨਾਲ ਪ੍ਰਤੀਕਿਰਿਆ ਕਰਕੇ ਹਾਈਡਰੋਜਨ ਗੈਸ ਮੁਕਤ ਕਰਦੀਆਂ ਹਨ । ਕੀ ਇਨ੍ਹਾਂ ਤੱਤਾਂ ਦੇ ਪਰਮਾਣੂਆਂ ਵਿੱਚ ਕੋਈ ਸਮਾਨਤਾ ਹੈ ?
(b) ਹੀਲੀਅਮ ਇੱਕ ਅਕਿਰਿਆਸ਼ੀਲ ਗੈਸ ਹੈ ਜਦਕਿ ਨੀਆਨ ਦੀ ਕਿਰਿਆਸ਼ੀਲਤਾ ਬਹੁਤ ਘੱਟ ਹੈ । ਇਨ੍ਹਾਂ ਦੇ ਪਰਮਾਣੂਆਂ ਵਿੱਚ ਕੀ ਸਮਾਨਤਾ ਹੈ ?
ਉੱਤਰ-
(a) ਲਿਥੀਅਮ, ਸੋਡੀਅਮ ਅਤੇ ਪੋਟਾਸ਼ੀਅਮ ਦੀ ਪਾਣੀ ਨਾਲ ਪ੍ਰਤੀਕਿਰਿਆ-

ਇਨ੍ਹਾਂ ਤਿੰਨਾਂ ਧਾਤਾਂ ਦੇ ਬਾਹਰਲੇ ਸੈੱਲ ਵਿੱਚ ਇੱਕ ਹੀ ਇਲੈੱਕਟਰਾਨ ਹੁੰਦਾ ਹੈ ।
(b) ਹੀਲੀਅਮ (He) ਅਤੇ ਨੀਆਨ (Ne) ਦੋਨੋਂ ਨੋਬਲ ਗੈਸਾਂ ਹੋਣ ਕਰਕੇ ਅਕਿਰਿਆਸ਼ੀਲ ਹਨ । ਇਨ੍ਹਾਂ ਦੇ ਬਾਹਰਲੇ ਸੈੱਲ ਪੂਰਨ ਹੁੰਦੇ ਹਨ । ਹੀਲੀਅਮ (He) ਕੋਲ ਸਿਰਫ K ਸੈੱਲ ਹੈ ਅਤੇ ਇਹ ਸੈਂਲ ਪੂਰਨ ਰੂਪ ਨਾਲ ਭਰਿਆ ਹੋਇਆ ਹੈ । ਦੂਜੇ ਪਾਸੇ ਨੀਆਨ (Ne) ਕੋਲ K ਅਤੇ L ਸੈੱਲ ਹਨ ਅਤੇ ਇਹ ਦੋਨੋਂ ਸੈਂਲ ਭਰੇ ਹੋਏ ਹਨ । K ਸ਼ੈੱਲ ਵਿੱਚ 2 ਇਲੈੱਕਟਰਾਨ ਅਤੇ L ਬੈੱਲ ਵਿੱਚ 8 ਇਲੈੱਕਟਰਾਨ ਹਨ । ਇਸ ਲਈ ਨੀਆਨ ਦੀ ਪ੍ਰਤੀਕਿਰਿਆਸ਼ੀਲਤਾ ਬਹੁਤ ਘੱਟ ਹੈ ।
ਪ੍ਰਸ਼ਨ 12.
ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਪਹਿਲੇ 10 ਤੱਤਾਂ ਵਿੱਚ ਕਿਹੜੀਆਂ ਧਾਤਾਂ ਹਨ ?
ਉੱਤਰ-
ਆਧੁਨਿਕ ਆਵਰਤੀ ਸਾਰਨੀ ਦੇ ਪਹਿਲੇ ਦੱਸ ਤੱਤ ਹਨ-H, He, Li, Be, B, C, N, 0, F ਅਤੇ Ne ਇਨ੍ਹਾਂ ਸਾਰੇ ਤੱਤਾਂ ਵਿੱਚੋਂ ਧਾਤਾਂ ਹਨ-ਲਿਥੀਅਮ (Li) ਅਤੇ ਬੈਰੀਲੀਅਮ (Be) ।
ਪ੍ਰਸ਼ਨ 13.
ਆਵਰਤੀ ਸਾਰਨੀ ਵਿੱਚ ਇਨ੍ਹਾਂ ਦੇ ਸਥਾਨ ਦੇ ਆਧਾਰ ਅਤੇ ਇਨ੍ਹਾਂ ਵਿੱਚੋਂ ਕਿਸ ਤੱਤ ਵਿੱਚ ਸਭ ਤੋਂ ਵੱਧ ਧਾਤਵੀ ਗੁਣ ਹੈ ?
Ga, Ge, As, Se, Be.
ਉੱਤਰ-
ਪਹਿਲੇ ਇਨ੍ਹਾਂ ਦਾ ਵਰਗੀਕਰਨ ਵੱਧਦੀ ਹੋਈ ਪਰਮਾਣੂ ਸੰਖਿਆ ਦੇ ਅਨੁਸਾਰ ਕਰਦੇ ਹਾਂ-
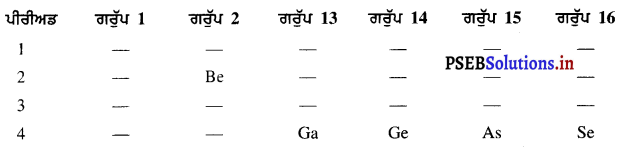
ਅਸੀਂ ਜਾਣਦੇ ਹਾਂ ਕਿ ਧਾਤਿਕ ਆਚਰਨ ਪੀਰੀਅਡ ਵਿੱਚ ਖੱਬੇ ਤੋਂ ਸੱਜੇ ਵੱਲ ਜਾਂਦੇ ਹੋਏ ਘੱਟ ਹੁੰਦਾ ਜਾਂਦਾ ਹੈ । ਇਸ ਗੱਲ ਨੂੰ ਧਿਆਨ ਵਿੱਚ ਰੱਖਦੇ ਹੋਏ ਖੱਬੇ ਪਾਸੇ ਦੇ ਤੱਤ Be ਅਤੇ Ga ਦਾ ਅਧਾਤਿਕ ਆਚਰਨ ਅਧਿਕਤਮ ਹੈ । ਇਸ ਲਈ ਸੱਜੇ ਪਾਸੇ ਵੱਲ ਦੇ ਤੱਤ ਅਧਾਤ ਹਨ ।
