Punjab State Board PSEB 12th Class Physical Education Book Solutions ਕ੍ਰਿਕੇਟ (Cricket) Game Rules.
ਕ੍ਰਿਕੇਟ (Cricket) Game Rules – PSEB 12th Class Physical Education
ਕ੍ਰਿਕੇਟ ਦਾ ਇਤਿਹਾਸ
(History of Cricket)
ਕ੍ਰਿਕੇਟ ਖੇਡ ਦੀ ਸ਼ੁਰੁਆਤ ਇੰਗਲੈਂਡ ਵਿਚ ਹੋਈ ਸੀ, ਪਰ ਕੁਝ ਇਤਿਹਾਸਕਾਰਾਂ ਦੇ ਅਨੁਸਾਰ ਇਸ ਖੇਡ ਦਾ ਜਨਮ ਫਰਾਂਸ ਵਿੱਚ ਹੋਇਆ ਸੀ । ਜ਼ਿਆਦਾਤਰ ਲੋਕ ਇਸ ਦਾ ਜਨਮ ਇੰਗਲੈਂਡ ਵਿੱਚ ਮੰਨਦੇ ਹਨ । ‘ਵਿਜਡਨ’ ਜਿਸਨੂੰ ਕ੍ਰਿਕੇਟ ਦਾ ਬਾਈਬਲ ਕਿਹਾ ਜਾਂਦਾ ਹੈ । ਕ੍ਰਿਕੇਟ ਦਾ ਪਹਿਲਾ ਉਲੇਖ 1300 ਵਿੱਚ ਹੋਇਆ ਸੀ। ਕ੍ਰਿਕੇਟ ਦੀ ਜਾਣਕਾਰੀ ਕਿੰਗ ਐਡਵਰਲਡ ਦੀ ਅਲਮਾਰੀ ਤੋਂ ਮਿਲੇ, ਬੱਲੇ ਤੇ ਗੇਂਦ ਤੋਂ ਹੁੰਦੀ ਹੈ । ਕੁੱਝ ਮਨੁੱਖਾਂ ਅਨੁਸਾਰ 13ਵੀਂ ਸਦੀ ਵਿੱਚ ਇਹ ਖੇਡ ਇੰਗਲੈਂਡ ਦੇ ਗਵਾਲੋਂ ਅਤੇ ਚਰਵਾਹੋਂ ਦੁਆਰਾ ਖੇਡਿਆ ਜਾਂਦਾ ਸੀ । ਸੰਨ 1706 ਵਿੱਚ ਵਿਲੀਅਮ ਗੋਲਡ ਨੇ ਆਪਣੀ ਕਵਿਤਾ ਵਿੱਚ ਵਿਕੇਟ ਦਾ ਵਰਣਨ ਕੀਤਾ ਸੀ । ਸੰਨ 1709 ਵਿੱਚ ਲੰਡਨ ਅਤੇ ਕੈਟ ਦੀਆਂ ਟੀਮਾਂ ਵਿੱਚ ਪਹਿਲਾਂ ਮੈਚ ਖੇਡਿਆ ਗਿਆ । ਫੇਰ 1770 ਵਿੱਚ ਕੈਮਬਰਿਜ ਵਿਸ਼ਵਵਿਦਿਆਲਾ ਫੇਰ 1729 ਵਿੱਚ ਐਕਸਪੋਰਟ ਵਿਸ਼ਵਵਿਦਿਆਲਿਆ ਵਿੱਚ ਇਹ ਖੇਡ ਖੇਡਿਆ ਜਾਂਦਾ ਸੀ ।
ਅਸਲ ਵਿੱਚ ਕ੍ਰਿਕੇਟ ਦਾ ਸੁਨਹਿਰਾ ਅਧਿਆਇ 1760 ਵਿੱਚ ਸ਼ੁਰੂ ਹੋਇਆ । 1760 ਵਿੱਚ ਇੰਗਲੈਂਡ ਵਿੱਚ ਪਹਿਲੀ ਕ੍ਰਿਕੇਟ ਕਲੱਬ ਦੀ ਸਥਾਪਨਾ ਕੀਤੀ ਗਈ । ਇਸ ਕਲੱਬ ਦਾ ਨਾਂ ਹੈਬਲਡਨ ਰੱਖਿਆ ਸੀ । ਤਕਰੀਬਨ 30 ਸਾਲ ਤੱਕ ਇਹ ਕਲੱਬ ਕ੍ਰਿਕੇਟ ਦੇ ਇਤਿਹਾਸ ਵਿੱਚ ਛਾ ਗਿਆ । ‘ਜਾਨ ਨਾਇਰਣ’ ਨਾਮਕ ਖਿਡਾਰੀ ਇਸ ਕਲੱਬ ਦੀ ਦੇਣ ਸੀ । ਕ੍ਰਿਕੇਟ ਦਾ ਦੂਜਾ ਇਤਿਹਾਸ ਦਾ ਸੁਨਹਿਰਾ ਅਧਿਆਇ ਐੱਨ. ਸੀ. ਸੀ. ਕਲੱਬ ਦੀ ਸਥਾਪਨਾ ਨਾਲ ਹੋਇਆ । ਇਸ ਕਲੱਬ ਦੀ ਸਥਾਪਨਾ ਸੰਨ 1787 ਵਿੱਚ ਇੰਗਲੈਂਡ ਵਿੱਚ ਹੋਈ । ਲਾਈਟ ਦੇ ਪ੍ਰਸਿੱਧ ਮੈਦਾਨ ਵਿੱਚ ਪਹਿਲਾਂ ਮੈਚ ਜੂਨ 1788 ਵਿੱਚ ਹੋਇਆ ।
ਸੰਨ 1887 ਵਿੱਚ ਆਸਟ੍ਰੇਲੀਆ ਤੇ ਇੰਗਲੈਂਡ ਵਿੱਚ ਪਹਿਲਾਂ ਮੰਜੂਰਸ਼ੁਦਾ ਟੈਸਟ ਮੈਚ ਖੇਡਿਆ ਗਿਆ । ਇਸ ਮੈਚ ਵਿੱਚ ਜਿੱਤ ਆਸਟ੍ਰੇਲੀਆ ਦੀ ਹੋਈ, ਜਿਸ ਦੇ ਵਿਰੋਧ ਵਿਚ ਅੰਗਰੇਜ਼ ਔਰਤਾਂ ਨੇ ਵੇਦ ਨੂੰ ਜਲਾ ਕੇ ਕ੍ਰਿਕੇਟ ਦਾ ਦਾਹ ਸੰਸਕਾਰ ਕੀਤਾ । ਵੇਦ ਦੀ ਰਾਖ ਨੂੰ ਆਸਟ੍ਰੇਲੀਆ ਦੀ ਟੀਮ ਨੂੰ ਅਰਪਣ ਕੀਤਾ ਗਿਆ |
ਉਸ ਸਮੇਂ ਤੋਂ ਹੀ ਇੰਗਲੈਂਡ ਤੇ ਆਸਟ੍ਰੇਲੀਆ ਦੀਆਂ ਕ੍ਰਿਕੇਟ ਟੀਮਾਂ ਇੱਕ ਦੂਜੇ ਦੇ ਵਿਰੁੱਧ ਐਸ ਲਈ ਮੈਚ ਖੇਡਦੇ ਹਨ । ਇਸ ਤੋਂ ਬਾਅਦ 1909 ਵਿੱਚ ਇੰਗਲੈਂਡ ਵਿੱਚ ਇਨਟਰੀਅਰ ਕ੍ਰਿਕੇਟ ਦੀ ਸਥਾਪਨਾ ਹੋਈ । ਜਿਸ ਦੇ ਨਾਲ ਅੰਤਰ-ਰਾਸ਼ਟਰੀ ਕ੍ਰਿਕੇਟ ਨੂੰ ਮਾਨਤਾ ਮਿਲ ਗਈ ।

ਇੰਗਲੈਂਡ ਤੋਂ ਇਲਾਵਾ ਆਸਟੇਲੀਆ ਤੇ ਦੱਖਣੀ ਅਫ਼ਰੀਕਾ ਵਿੱਚ ਵੀ ਮੈਂਬਰ ਬਣ ਗਏ । ਸੰਨ 1971 ਵਿੱਚ ਰੰਗ ਭੇਦ ਦੀ ਨੀਤੀ ਕਾਰਨ ਦੱਖਣੀ ਅਫ਼ਰੀਕਾ ਦੀ ਮੈਂਬਰਸ਼ਿਪ ਖ਼ਤਮ ਕਰ ਦਿੱਤੀ ਗਈ ਸੀ । ਸੰਨ 1956 ਵਿੱਚ ਇਸ ਕਾਂਗਰਸ ਦਾ ਨਾਂ ਬਦਲ ਕੇ ਇੰਟਰਨੈਸ਼ਨਲ ਕ੍ਰਿਕੇਟ ਕਾਂਗਰਸ ਰੱਖ ਦਿੱਤਾ ਗਿਆ । ਕੁੱਝ ਸਮੇਂ ਬਾਅਦ ਦੂਜੇ ਦੇਸ਼ਾਂ ਨੇ ਇਸਦੀ ਮੈਂਬਰਸ਼ਿਪ ਲੈ ਲਈ । ਹੁਣ ਇੰਗਲੈਂਡ, ਆਸਟ੍ਰੇਲੀਆ, ਭਾਰਤ, ਸ੍ਰੀਲੰਕਾ, ਵੈਸਟ ਇੰਡੀਜ਼, ਨਿਊਜ਼ੀਲੈਂਡ, ਪਾਕਿਸਤਾਨ, ਅਰਜਨਟੀਨਾ, ਕੇਨੈਡਾ, ਡੈਨਮਾਰਕ, ਕੀਨੀਆ, ਜਿੰਬਾਵੇ, ਬੰਗਲਾਦੇਸ਼, ਹਾਲੈਂਡ, ਬਰਹੁੱਡਾ, ਫਿਜੀ, ਸਿੰਗਾਪੁਰ, ਹਾਂਗਕਾਂਗ, ਇਸਰਾਈਲ ਤੇ ਮਲੇਸ਼ੀਆ ਆਦਿ ਦੇਸ਼ ਇਸ ਦੇ ਮੈਂਬਰ ਹਨ ।
5 ਜਨਵਰੀ, 1971 ਵਿੱਚ ਕ੍ਰਿਕੇਟ ਦੇ ਇਤਿਹਾਸ ਦਾ ਪਹਿਲਾ ਇਕ ਦਿਨਾਂ ਅੰਤਰਰਾਸ਼ਟਰੀ ਮੈਚ ਇੰਗਲੈਂਡ ਤੇ ਆਸਟ੍ਰੇਲੀਆ ਵਿੱਚ ਖੇਡਿਆ ਗਿਆ । ਇਸ ਵਿੱਚ 40 ਓਵਰ ਹਰੇਕ ਪਾਰੀ ਵਿੱਚ ਰੱਖੇ ਗਏ । ਇਕ ਦਿਨਾਂ ਅੰਤਰਰਾਸ਼ਟਰੀ ਕ੍ਰਿਕੇਟ ਮੈਚਾਂ ਦੇ ਆਯੋਜਨ ਦੇ ਵਿਕਾਸ ਦਾ ਸਿਹਰਾ ਵੀ ਇੰਗਲੈਂਡ ਨੂੰ ਜਾਂਦਾ ਹੈ । ਇੰਗਲੈਂਡ ਦੇ ਮਿਹਨਤ ਦੇ ਫਲਸਰੂਪ ਇੰਗਲੈਂਡ ਵਿੱਚ ਪਹਿਲਾ ਵਿਸ਼ਵ ਕੱਪ ਦੇ ਮੁਕਾਬਲੇ ਕਰਵਾਏ ਗਏ ।ਇਸ ਵਿਸ਼ਵ ਕੱਪ ਕ੍ਰਿਕੇਟ ਵਿੱਚ 8 ਦੇਸ਼ਾਂ ਦੀਆਂ ਟੀਮਾਂ ਨੇ ਭਾਗ ਲਿਆ। ਇਸ ਵਿਸ਼ਵ ਕੱਪ ਦੇ ਫਾਈਨਲ ਵਿੱਚ ਵੈਸਟ ਇੰਡੀਜ਼ ਨੇ ਆਸਟ੍ਰੇਲੀਆ ਨੂੰ ਸਾਰਿਆਂ ਨਾਲ ਮਿਲਾਇਆ ਸੀ । | ਭਾਰਤ ਵਿੱਚ ਕ੍ਰਿਕੇਟ ਦੀ ਸ਼ੁਰੂਆਤ ਅੰਗਰੇਜ਼ਾਂ ਦੇ ਭਾਰਤ ਆਉਣ ਨਾਲ ਹੋਈ ।
ਭਾਰਤ ਦੇ ਕ੍ਰਿਕੇਟ ਦਾ ਇਤਿਹਾਸ ਸੰਨ 1721 ਤੋਂ ਸ਼ੁਰੂ ਹੁੰਦਾ ਹੈ । ਸੰਨ 1792 ਵਿੱਚ ਕਲਕੱਤਾ ਵਿੱਚ ਕ੍ਰਿਕੇਟ ਕਲੱਬ ਦੀ ਸਥਾਪਨਾ ਹੋਈ । ਪਹਿਲਾਂ-ਪਹਿਲਾ ਕ੍ਰਿਕੇਟ ਰਾਜਘਰਾਨਿਆਂ ਤੱਕ ਹੀ ਸੀਮਿਤ ਰਿਹਾ । ਪਰ ਹੁਣ ਇਹ ਖੇਡ ਸਭ ਤੋਂ ਜ਼ਿਆਦਾ ਮਸ਼ਹੂਰ ਹੋ ਚੁੱਕਿਆ ਹੈ । ਭਾਰਤ ਦੀ ਪਹਿਲੀ ਕ੍ਰਿਕੇਟ ਟੀਮ ਨੇ ਸੰਨ 1874 ਵਿੱਚ ਇੰਗਲੈਂਡ ਦਾ ਦੌਰਾ ਕੀਤਾ ਸੀ ।
ਇਸ ਵਿੱਚ ਭਾਰਤ ਦੇ ਖਿਡਾਰੀਆਂ ਨੇ ਵਿਦੇਸ਼ੀ ਟੀਮਾਂ ਨਾਲ ਮੈਚ ਖੇਡ ਕੇ ਆਪਣੀ ਤਾਕਤ ਯਾਦ ਕਰਵਾਈ । ਸਭ ਤੋਂ ਪਹਿਲਾਂ ਮਹਾਰਾਜਾ ਰਣਜੀਤ ਸਿੰਘ ਨੇ ਇੰਗਲੈਂਡ ਦੀ ਟੀਮ ਵਿੱਚ ਭਾਗ ਲੈ ਕੇ ਵਿਸ਼ਵ ਕੱਪ ਟੀਮ ਵਿੱਚ ਪਹਿਲਾ ਸੈਂਕੜਾ ਬਣਾਇਆ ਸੀ । ਸੰਨ 1952 ਵਿੱਚ ਲਾਈਟ ਦੇ ਮੈਦਾਨ ਵਿੱਚ ਭਾਰਤ ਨੇ ਪਹਿਲਾਂ ਕ੍ਰਿਕੇਟ ਮੈਚ ਇੰਗਲੈਂਡ ਦੇ ਵਿਰੁੱਧ ਖੇਡਿਆ ।
ਸੰਨ 1934 ਵਿੱਚ ਰੰਜ਼ੀ ਵਾਫ਼ੀ ਸ਼ੁਰੂ ਹੋਈ । ਸੰਨ 1928 ਵਿੱਚ ਆਰ.ਈ.’ ਗਾਂਟ ਦੀ ਪ੍ਰਧਾਨਗੀ ਹੇਠ ਭਾਰਤੀ ਕ੍ਰਿਕੇਟ ਕੰਟਰੋਲ ਬੋਰਡ ਦੀ ਸਥਾਪਨਾ ਹੋਈ । ਪਹਿਲਾਂ ਆਈ.ਸੀ.ਸੀ. ਟਵੰਟੀ ਵਰਲੱਡ ਕੱਪ ਕ੍ਰਿਕੇਟ ਸੰਨ 2007 ਵਿੱਚ ਖੇਡਿਆ ਗਿਆ ।
ਯਾਦ ਰੱਖਣ ਯੋਗ ਗੱਲਾਂ
(Tips to Remember)
- ਕ੍ਰਿਕੇਟ ਟੀਮ ਵਿਚ ਖਿਡਾਰੀਆਂ ਦੀ ਗਿਣਤੀ = 16 (11+5)
- ਵਿਕਟਾਂ ਦੇ ਵਿਚਾਲੇ ਦੀ ਦੁਰੀ = 22 ਗਜ਼ (20.12 ਸੈਂ.ਮੀ.).
- ਪਿੱਚ ਦੀ ਚੌੜਾਈ . = 4’4” (3.05 ਮੀ.)
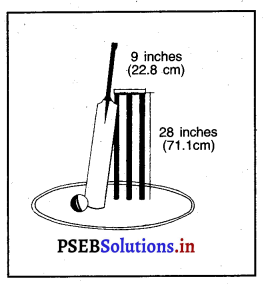
- ਵਿਕਟਾਂ ਦੀ ਚੌੜਾਈ = 9 ਇੰਚ (22.9 ਸੈਂ.ਮੀ.).
- ਕ੍ਰਿਕੇਟ ਗੇਂਦ ਦਾ ਘੇਰਾ = 8.1 ਤੋਂ 9 ਇੰਚ (22.4 ਸੈਂ.ਮੀ.-22.9 ਸੈਂ.ਮੀ.)
- ਕ੍ਰਿਕੇਟ ਗੇਂਦ ਦਾ ਭਾਰ = (155.9 ਗਰਾਮ-163 ਗਰਾਮ)
- ਬੈਟ ਦੀ ਚੌੜਾਈ = 425” ਇੰਚ (10.8 ਸੈਂ.ਮੀ.)
- ਬੈਟ ਦੀ ਲੰਬਾਈ = 38 ਇੰਚ (96.52 ਸੈਂ.ਮੀ.).
- ਗੇਂਦ ਦਾ ਰੰਗ = ਦਿਨ ਦੇ ਮੈਚ ਲਈ ਲਾਲ ਅਤੇ ਰਾਤ ਦੇ ਮੈਚ ਲਈ ਸਫ਼ੈਦ
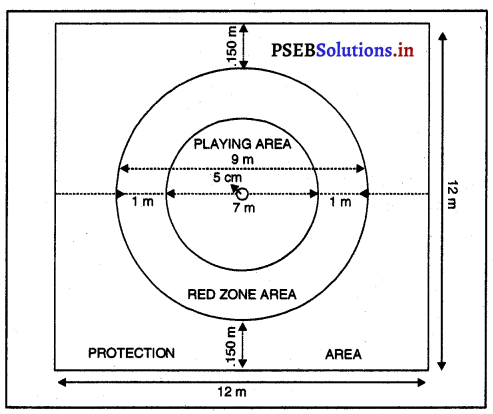
- ਕੇਂਦਰ ਤੋਂ ਵੱਡੇ ਚੱਕਰ ਦੀ ਦੂਰੀ = 75 ਗਜ਼ ਤੋਂ 85 ਗਜ਼ (137 ਮੀ.-150 ਮੀ.)
- ਵਿਕਟਾਂ ਦੀ ਜ਼ਮੀਨ ਤੋਂ ਉਚਾਈ = 28 ਇੰਚ (71 ਸੈਂ.ਮੀ.)
- ਮੈਚ ਦੀਆਂ ਕਿਸਮਾਂ = 20-20, ਇਕ ਦਿਨ ਦਾ ਮੈਚ, ਪੰਜ ਦਿਨ ਦਾ ਟੈਸਟ ਮੈਚ
- ਮੈਚ ਦੇ ਅੰਪਾਇਰਾਂ ਦੀ ਗਿਣਤੀ : 2
- ਤੀਜਾ ਅੰਪਾਇਰ = ਇਕ ਮੈਚ ਰੈਫ਼ਰੀ
- ਛੋਟੇ ਸਰਕਲ ਦਾ ਰੇਡੀਅਸ = 27.4 ਮੀ.
- ਬਾਊਲਿੰਗ ਕੀਜ਼ ਦੀ ਲੰਬਾਈ = 8′.8 (2.64 ਮੀ.)
- ਪੀਚਿੰਗ ਕੁੰਜ . = 4′ (1.22 ਮੀ.)
ਕ੍ਰਿਕੇਟ ਦੇ ਸਧਾਰਨ ਨਿਯਮ
(Latest General Rules of Cricket)
1. ਕ੍ਰਿਕੇਟ ਦਾ ਮੈਚ ਦੋ ਟੀਮਾਂ ਦੇ ਵਿੱਚ ਹੀ ਹੁੰਦਾ ਹੈ ਅਤੇ ਇਸ ਵਿੱਚ ਹਰੇਕ ਟੀਮ ਦੇ 11 ਖਿਡਾਰੀ ਭਾਗ ਲੈਂਦੇ ਹਨ । ਹਰੇਕ ਟੀਮ ਦਾ ਇੱਕ ਖਿਡਾਰੀ ਕੈਪਟਨ ਹੁੰਦਾ ਹੈ । ਜੇਕਰ ਕੈਪਟਨ ਗੈਰ ਹਾਜਰ ਹੋਵੇ ਤਾਂ ਵਾਈਸ-ਕੈਪਟਨ ਹੀ ਕੈਪਟਨ ਦੀ ਭੂਮਿਕਾ ਅਦਾ ਕਰਦਾ ਹੈ ।
2. ਖੇਡਣ ਦੇ ਲਈ ਟਾਸ ਤੋਂ ਪਹਿਲੇ ਕੈਪਟਨ ਰਾਹੀਂ ਖਿਡਾਰੀਆਂ ਦਾ ਨਾਮਾਂਕਨ ਕੀਤਾ ਜਾਂਦਾ ਹੈ ।
3. ਮੈਚ ਦੇ ਦੌਰਾਨ ਕਿਸੇ ਖਿਡਾਰੀ ਦੇ ਬੀਮਾਰ ਹੋਣ ਦੀ ਦਿਸ਼ਾ ਵਿੱਚ ਜਾਂ ਜ਼ਖ਼ਮੀ ਹੋਣ ਤੇ ਉਸਦੇ ਸਥਾਨ ਤੇ ਜ਼ਿਆਦਾ ਖਿਡਾਰੀ (Subsititutes) ਨੂੰ ਅਵਸਰ ਦਿੱਤਾ ਜਾਵੇਗਾ ।
4. ਜ਼ਿਆਦਾਤਰ ਖਿਡਾਰੀ ਨੂੰ ਕੇਵਲ ਫੀਲਡਿੰਗ (Fielding) ਦੇ ਲਈ ਬਦਲਿਆ ਜਾਵੇਗਾ, ਬੈਟਿੰਗ ਜਾਂ ਬਾਲਿੰਗ ਦੇ ਲਈ ਨਹੀਂ ।
5. ਮੈਚ ਦੇ ਦੌਰਾਨ ਇੱਕ ਜ਼ਖ਼ਮੀ ਜਾਂ ਬੀਮਾਰ ਬੈਟਸਮੈਨ ਦੇ ਲਈ ਇਕ ਰਨਰ ਦਿੱਤਾ ਜਾ ਸਕਦਾ ਹੈ । ਇਹ ਖਿਡਾਰੀ . ਜੋ ਰਨਰ ਦੇ ਰੂਪ ਵਿੱਚ ਖੇਡਦਾ ਹੈ, ਉਹ ਬੈਟਿੰਗ ਟੀਮ ਦਾ ਮੈਂਬਰ ਹੋਵੇਗਾ ।
6. ਹਾਲਾਂਕਿ ਵਿਕੇਟ ਨਾਲ ਬਾਊਂਰੀਜ਼ ਦੀ ਦੂਰੀ ਨਿਸ਼ਚਿਤ ਨਹੀਂ ਹੁੰਦੀ, ਪਰ ਇਹ 75 ਤੋਂ 85 ਗਜ ਹੋ ਸਕਦੀ ਹੈ । ਇਸ ਲਈ ਹਰੇਕ ਜਗ੍ਹਾ ਦੇ ਖੇਡ ਮੈਦਾਨ ਅਲੱਗ-ਅਲੱਗ ਆਕਾਰ (Size) ਦਾ ਹੁੰਦਾ ਹੈ ।
7. ਉਹ ਟੀਮ, ਜੋ ਪਹਿਲੇ ਬੈਟਿੰਗ ਕਰਦੀ ਹੈ ਅਤੇ ਪੰਜ ਦਿਨਾਂ ਮੈਚ ਵਿੱਚ 200 ਰਨ ਦੀ ਲੀਡ, ਤਿੰਨ ਦਿਨਾਂ ਮੈਚ ਵਿੱਚ 150 ਰਣ ਦੀ ਫੀਲਡ ਤੇ ਦੋ ਦਿਨਾਂ ਮੈਚ ਵਿਚ 100 ਰਨ ਦੀ ਲੀਡ ਲੈ ਲੈਂਦੀ ਹੈ, ਤਾਂ ਉਹ ਵਿਰੋਧੀ ਟੀਮ ਨੂੰ ਆਪਣੀ ਇਨਿੰਗ ਨੂੰ ਫਾਲੋਆਨ ਦੇ ਲਈ ਕਹਿ ਸਕਦੀ ਹੈ ।
8. ਬਾਲਿੰਗ ਹਰੇਕ ਵਿਕੇਟ ਤੋਂ ਵਾਰ-ਵਾਰ ਨਾਲ ਕਰਨੀ ਚਾਹੀਦੀ । ਇਕ ਓਵਰ ਵਿੱਚ 6 ਤੋਂ 8 ਬਾਲ ਹੋ ਸਕਦੇ ਹਨ।
9. ਕ੍ਰਿਕਟ ਦੇ ਖਿਡਾਰੀਆਲ ਓਵਰ ਵਿੱਚ ਨਹੀਂ ਗਿਣੀ ਚਾਹੀਦੀ । ਇਕ ਓਵਰ ਵਿੱਚ
9. ਕ੍ਰਿਕਟ ਦੇ ਖਿਡਾਰੀ ਲਈ ਕਿੱਟ ਪਹਿਨਣਾ ਜ਼ਰੂਰੀ ਹੈ । ਕਿੱਟ ਤੋਂ ਭਾਵ ਸਫ਼ੈਦ ਪੈਂਟ, ਕਮੀਜ਼, ਬੂਟ, ਜੁਰਾਬਾਂ, ਪੈਡ, ਅਬਡਾਮਨਲ ਗਾਰਡ, ਗਲਵਜ ਅਤੇ ਬੈਟ ਹਨ ।
10. ਬਾਉਲਿੰਗ ਕ੍ਰੀਜ਼ ਸਟੰਪਾਂ ਦੇ ਨਾਲ 8 ਫੁੱਟ 8 ਇੰਚ (2.64 gm) ਲੰਮੀ ਖਿੱਚੀ ਜਾਵੇਗੀ । ਸਟੰਪਾਂ ਵਿਚਕਾਰ ਹੋਣਗੀਆਂ | ਪਾਪਿੰਗ ਝੀਜ਼ ਬਾਉਲਿੰਗ ਕੀਜ਼ ਦੇ ਸਮਾਨਾਂਤਰ 3 ਫੁੱਟ (90 cm) ਤੇ ਖਿੱਚੀ ਜਾਵੇਗੀ ਅਤੇ ਇਹ ਸਟੰਪਾਂ ਦੇ ਦੋਵੇਂ ਪਾਸੇ 6 ਫੁੱਟ (1.80 m) ਵਧਾਈ ਜਾਵੇਗੀ । ਰਿਟਰਨ ਭੀਜ਼ ਬਾਊਲਿੰਗ ਕੀਜ਼ ਦੇ ਦੋਨਾਂ ਸਿਰਿਆਂ ਤੇ ਸਮਕੋਣ ‘ਤੇ ਖਿੱਚੀ ਜਾਵੇਗੀ ਅਤੇ ਇਸ ਨੂੰ ਪਾਪਿੰਗ ਝੀਜ਼ ਦੇ ਮਿਲਣ ਲਈ ਵਧਾਇਆ ਜਾਵੇਗਾ | ਪਾਪਿੰਗ ਝੀਜ਼ ਤੇ ਰਿਟਰਨ ਭੀਜ਼ ਦੋਨੋਂ ਹੀ ਲੰਬਾਈ ਵਿਚ ਅਸੀਮਿਤ ਮੰਨੀਆਂ ਜਾਂਦੀਆਂ ਹਨ । .

11. ਹਰੇਕ ਟੀਮ ਨੂੰ ਵਾਰੀ-ਵਾਰੀ ਨਾਲ ਦੋ ਵਾਰ ਖੇਡਣਾ ਪੈਂਦਾ ਹੈ । ਇਸ ਦਾ ਫੈਸਲਾ ਟਾਸ ਦੁਆਰਾ ਕੀਤਾ ਜਾਵੇਗਾ ਕਿ ਕਿਹੜੀ ਟੀਮ ਪਹਿਲਾਂ ਖੇਡੇ ।
ਜੋ ਵੀ ਟੀਮ ਪਹਿਲੇ ਖੇਡੇਗੀ, ਜੇਕਰ ਉਸ ਨੇ ਵਿਰੋਧੀ ਟੀਮ ਤੇ ਪੰਜ ਦਿਨ ਜਾਂ ਵਧੇਰੇ ਦੇ ਮੈਚ ਵਿਚ 200 ਦੌੜਾਂ, ਤਿੰਨ ਦਿਨ ਦੇ ਮੈਚ ਵਿਚ 150, ਦੋ ਦਿਨ ਦੇ ਮੈਚ ਵਿਚ 100 ਅਤੇ ਇਕ ਦਿਨ ਦੇ ਮੈਚ ਵਿਚ 25 ਦੌੜਾਂ ਵਧੇਰੇ · ਬਣਾ ਲਈਆਂ ਹਨ, ਤਾਂ ਉਹ ਦੁਸਰੀ ਟੀਮ ਨੂੰ ਦੁਬਾਰਾ ਖੇਡਣ ਲਈ ਕਹਿ ਸਕਦੀ ਹੈ ਅਰਥਾਤ Follow on ਕਰਵਾ ਸਕਦੀ ਹੈ । ਬੈਟ ਕਰਨ ਵਾਲੀ ਟੀਮ ਦਾ ਕਪਤਾਨ ਸਮੇਂ ਤੋਂ ਪਹਿਲਾਂ ਵੀ ਪਾਰੀ ਦੀ ਸਮਾਪਤੀ ਦੀ ਘੋਸ਼ਣਾ (Declare) ਕਰ ਸਕਦਾ ਹੈ ।
12. ਹਰੇਕ ਪਾਰੀ ਦੇ ਆਰੰਭ ਤੇ ਪ੍ਰਤੀ ਦਿਨ ਖੇਡ ਆਰੰਭ ਕਰਨ ਤੋਂ ਪਹਿਲਾਂ ਕੈਪਟਨ ਕਹਿੰਦਾ ਹੈ “ਖੇਡੋ’ ਅਤੇ ਜੇਕਰ ਟੀਮ ਖੇਡਣ ਤੋਂ ਇਨਕਾਰ ਕਰੇ, ਤਾਂ ਉਹ ਮੈਚ ਹਾਰ ਜਾਵੇਗੀ । ਹਰੇਕ ਪਾਰੀ ਵਿਚ 10 ਮਿੰਟ ਅਤੇ ਹਰੇਕ ਨਵੇਂ ਬੈਟਸਮੈਨ ਦੇ ਆਉਣ ਵਿਚ ਵੱਧ ਤੋਂ ਵੱਧ ਦੋ ਮਿੰਟ ਦਿੱਤੇ ਜਾਣਗੇ । ਭੋਜਨ ਲਈ ਇੰਟਰਵਲ ਅਕਸਰ 45 ਮਿੰਟ ਤੋਂ ਵੱਧ ਨਹੀਂ ਹੋਵੇਗਾ । ਚਾਹ ਲਈ ਇੰਟਰਵਲ 20 ਮਿੰਟ ਤੋਂ ਜ਼ਿਆਦਾ ਨਹੀਂ ਹੋਵੇਗਾ । ਜੇਕਰ ਚਾਹ ਦੇ ਨਿਰਧਾਰਿਤ ਸਮੇਂ ਤੇ 9 ਖਿਡਾਰੀ ਆਊਟ ਹੋਏ ਹਨ, ਤਾਂ ਖੇਡ ਨੂੰ 30 ਮਿੰਟ ਤਕ ਜਾਂ ਪਾਰੀ ਦੀ ਸਮਾਪਤੀ ਤਕ ਜਾਰੀ ਰੱਖਿਆ ਜਾਂਦਾ ਹੈ ।
ਵੱਖ-ਵੱਖ ਪ੍ਰਕਾਰ ਦੇ ਮੈਚ
(Various Types of Matches)
1. ਟੈਸਟ ਮੈਚ (Test Match-ਟੈਸਟ ਮੈਚ ਵਿਚ ਦੋਨਾਂ ਟੀਮਾਂ ਨੂੰ ਦੋ-ਦੋ ਇਨਿੰਗ ਖੇਡਣ ਦਾ ਮੌਕਾ ਮਿਲਦਾ ਹੈ । ਇਹ ਮੈਚ ਪੰਜ ਦਿਨਾਂ ਦਾ ਹੁੰਦਾ ਹੈ ।
2. ਇਕ ਦਿਨ ਦਾ ਮੈਚ (One day Match)-ਇਕ ਦਿਨ ਦੇ ਮੈਚ ਵਿਚ ਦੋਨੋ ਟੀਮਾਂ 50 ਓਵਰ ਦੇ ਲਈ ਬੈਟ , ਕਰਨਗੀਆਂ । ਇਹ ਮੈਚ ਦਿਨ ਜਾਂ ਰਾਤ ਨੂੰ ਖੋਲ੍ਹਿਆ ਜਾ ਸਕਦਾ ਹੈ ।
3. 20-20 ਮੈਚ (20-20 Match-ਇਹ ਇਕ ਦਿਨ ਦੇ ਮੈਚ ਦੀ ਤਰ੍ਹਾਂ ਹੈ ਇਸ ਨੂੰ 20-20 ਓਵਰ ਹੀ ਬੰਡਦਿਆਂ ਹਨ । ਇਸ ਵਿਚ ਨਵੇਂ ਨਿਯਮ ਜੋ ਇਸ ਤਰ੍ਹਾਂ ਹਨ’-
- ਜਦੋਂ ਬਾਲਰ ਬਾਉਲਿੰਗ ਕਰੀਜ਼ ਪਾਰ ਕਰਕੇ ਬਾਲ ਸੁੱਟਦਾ ਹੈ ਤਾਂ ਉਸ ਨੂੰ ਨੋ ਬਾਲ ਕਿਹਾ ਜਾਂਦਾ ਹੈ ਜਿਸ ਨਾਲ ਬੈਟਸਮੈਨ ਨੂੰ ਫ਼ਰੀ ਹਿੱਟ ਮਿਲਦੀ ਹੈ । ਇਸ ਫ਼ਰੀ ਹਿਟ ਵਿਚ ਬੈਟਸਮੈਨ ਆਊਟ ਨਹੀਂ ਹੋ ਸਕਦਾ ਸਿਰਫ਼ ਰਨ ਆਊਟ ਹੋ ਸਕਦਾ ਹੈ ।
- ਜਦੋਂ ਮੈਚ ਬਰਾਬਰ ਹੋ ਜਾਵੇ ਤਾਂ ਬਾਲ ਆਉਟ ਦੇ ਨਾਲ ਜਿੱਤ ਹਾਰ ਦਾ ਫੈਸਲਾ ਕੀਤਾ ਜਾਂਦਾ ਹੈ । ਇਸ ਵਿਚ । ਦੋਨਾਂ ਟੀਮਾਂ ਦੇ ਪੰਜ-ਪੰਜ ਖਿਡਾਰੀਆਂ ਨੂੰ ਬਾਲ ਦਰਜ ਦਾ ਮੌਕਾ ਦਿੱਤਾ ਜਾਂਦਾ ਹੈ ਇਸ ਗੇਂਦ ਨੂੰ ਬੈਟਸਮੈਨ ਨਹੀਂ ਖੇਡਦਾ . ਜਿਹੜੀ ਟੀਮ ਜ਼ਿਆਦਾ ਵਿਕਟ ਲੈਂਦੀ ਹੈ ਜੇਤੂ ਹੁੰਦੀ ਹੈ ।
- ਕ੍ਰਿਕੇਟ ਵਿਚ ਨਵੇਂ ਨਿਯਮ ਲਾਗੂ ਹਨ ਜੋ ਇਸ ਤਰ੍ਹਾਂ ਹਨ, 50 ਓਵਰ ਦੇ ਮੈਚ ਵਿਚ ਤਿੰਨ ਪਾਵਰ ਪਲੇ 10 ਓਵਰ, 5 ਓਵਰ ਅਤੇ 5 ਓਵਰ ਦੇ ਹੁੰਦੇ ਹਨ, ਪਹਿਲੇ 10 ਪਾਵਰ ਪਲੇ ਖੇਡ ਦੇ ਸ਼ੁਰੂ ਵਿਚ ਲੈਣੇ ਹੁੰਦੇ ਹਨ । ਬਾਕੀ 5, 5 ਓਵਰ ਬੈਟਿੰਗ ਅਤੇ ਫੀਲਡਿੰਗ ਟੀਮ ਜਦੋਂ ਚਾਹੇ ਲੈ ਸਕਦੀ ਹੈ ।
4. ਪਹਿਲਾਂ ਬੈਟਸਮੈਨ ਗੇਂਦ ਨੂੰ ਚੋਟ ਲਗਾਉਣ ਦੇ ਬਾਅਦ ਗੇਂਦ ਮੈਦਾਨ ਵਿਚ ਰਹਿਣ ਦੇ ਸਮੇਂ ਵਿਚ ਇਕ ਸਾਈਡ ਤੋਂ ਦੂਸਰੀ ਸਾਈਡ ਤਕ ਦੌੜਦਾ ਹੈ । ਉਹ ਜਿੰਨੀ ਵਾਰ ਅਜਿਹਾ ਕਰੇਗਾ, ਉਤਨੇ ਰਨ ਹੋ ਜਾਂਦੇ ਹਨ | ਸਕੋਰ ਲਈ ਦੌੜਾਂ ਦੀ ਗਿਣਤੀ ਕੀਤੀ ਜਾਂਦੀ ਹੈ । ਜਦੋਂ ਬੈਟਸਮੈਨ ਗੇਂਦ ਨੂੰ ਹਿੱਟ ਕਰਨ ਮਗਰੋਂ ਇਕ ਸਿਰੇ ਤੋਂ ਦੂਸਰੇ ਸਿਰੇ ‘ਤੇ ਪਹੁੰਚ ਜਾਂਦਾ ਹੈ, ਤਾਂ ਇਕ ਦੌੜ ਪੂਰੀ ਸਮਝੀ ਜਾਂਦੀ ਹੈ । ਜੇਕਰ ਕੋਈ ਬੈਟਸਮੈਨ ਦੂਜੇ ਪਾਸੇ ਪਹੁੰਚੇ ਬਿਨਾਂ ਰਾਹ ਤੋਂ ਵਾਪਸ ਪਰਤ ਜਾਂਦਾ ਹੈ, ਉਹ ਦੌੜ ਨਹੀਂ ਗਿਣੀ ਜਾਂਦੀ । ਇਸ ਨੂੰ ਸ਼ਾਰਟ ਰਨ (Short Run) ਕਹਿੰਦੇ ਹਨ । ਜੇਕਰ ਰਨ ਬਣਾਉਂਦੇ ਸਮੇਂ ਬਾਲ ਹਵਾ ਵਿਚ ਹੋਵੇ, ਉਹ ਲਪਕ ਲਿਆ ਜਾਵੇ, ਤਾਂ ਉਹ ਰਨ (ਦੌੜ) ਗਿਣੀ ਨਹੀਂ ਜਾਵੇਗੀ । ਇਸੇ ਤਰ੍ਹਾਂ ਜੇਕਰ ਬੈਟਸਮੈਨ ਦੌੜ ਬਣਾਉਂਦੇ ਸਮੇਂ ਰਨ ਆਉਟ (Run Out) ਹੋ ਜਾਵੇ, ਤਾਂ ਉਹ ਦੌੜ ਨਹੀਂ ਗਿਣੀ ਜਾਵੇਗੀ । , 17 ਜੇਕਰ ਬੈਟਸਮੈਨ ਦੇ ਹਿਟ ਕਰਨ ਤੇ ਗੇਂਦ ਮੈਦਾਨ ਨੂੰ ਛੂੰਹਦੀ ਹੋਈ ਸੀਮਾ ਰੇਖਾ ਦੇ ਪਾਰ ਚਲੀ ਜਾਂਦੀ ਹੈ, ਤਾਂ ਉਸ ਨੂੰ ਬਾਊਂਡਰੀ ਕਹਿੰਦੇ ਹਨ । ਬਾਊਂਡਰੀ ਦਾ ਚਾਰ ਸਕੋਰ ਹੁੰਦਾ ਹੈ । ਜੇਕਰ ਗੇਂਦ ਜ਼ਮੀਨ ਨੂੰ ਲੱਗੇ ਬਿਨਾਂ ਬਾਊਂਡਰੀ ਤੋਂ ਬਾਹਰ ਜਾ ਕੇ ਡਿੱਗੇ ਤਾਂ 6 ਦੌੜਾਂ ਹੋ ਜਾਂਦੀਆਂ ਹਨ | ਬਾਊਂਡਰੀ ਜੇਕਰ ਓਵਰ ਥਰੋ ਤੇ ਹੋਈ ਹੈ ਜਾਂ ਖੇਤਰ ਰੱਖਿਅਕ ਨੇ ਜਾਣ ਬੁੱਝ ਕੇ ਕੀਤੀ ਹੈ ਤਾਂ ਬਣੇ ਹੋਏ ਰਨ ਅਤੇ ਬਾਊਂਡਰੀ ਦਾ ਸਕੋਰ ਫਲਅੰਕਣ ਵਿਚ ਜੋੜੇ ਜਾਣਗੇ ।
5. ਜੇਕਰ ਗੇਂਦ ਗੁੰਮ ਹੋ ਜਾਵੇ ਤਾਂ ਕੋਈ ਵੀ ਖੇਤਰ ਰੱਖਿਅਕ ਗੁੰਮ ਹੋ ਜਾਣ ਦਾ ਐਲਾਨ ਕਰ ਦਿੰਦਾ ਹੈ | ਅਜਿਹੀ ਹਾਲਤ ਵਿਚ ਅੰਪਾਇਰ ਗੁੰਮ ਹੋਈ ਗੇਂਦ ਨਾਲ ਮਿਲਦੀ-ਜੁਲਦੀ ਹਾਲਤ ਵਾਲੀ ਗੇਂਦ ਨਾਲ ਖੇਡ ਮੁੜ ਸ਼ੁਰੂ ਕਰਵਾ ਦਿੰਦਾ ਹੈ ।
6. ਜੋ ਵੀ ਟੀਮ ਦੋ ਪਾਰੀਆਂ (ਇਨਿੰਗਜ਼) ਵਿਚ ਜ਼ਿਆਦਾ ਦੌੜਾਂ ਬਣਾ ਲੈਂਦੀ ਹੈ ਉਸ ਨੂੰ ਜੇਤੂ ਮੰਨਿਆ ਜਾਵੇਗਾ । | ਪਰ ਜੇਕਰ ਮੈਚ ਪੂਰਾ ਨਾ ਹੋ ਸਕੇ, ਤਾਂ ਇਹ ਬਰਾਬਰ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ ।
ਟਵੰਟੀ-20 ਮੈਚ ਨਾਲ ਸੰਬੰਧਿਤ ਨਿਯਮ .
(Rules Related to Twenty-20 Match)
1. ਹਰੇਕ ਟੀਮ 20 ਓਵਰ ਦੇ ਲਈ ਬੱਲੇਬਾਜ਼ੀ ਕਰੇਗੀ ।
2. ਇਕ ਮੈਚ ਦੀ ਅਵਧੀ 3 ਘੰਟੇ ਹੋਵੇਗੀ | ਪਾਰੀਆਂ ਦੇ ਮੱਧ 20 ਮਿੰਟ ਦਾ ਮੱਧ-ਅੰਤਰ ਹੋਵੇਗਾ ।
3. ਇਕ ਮੈਚ ਪੂਰਾ ਹੋਣ ਦੇ ਲਈ ਘੱਟ ਤੋਂ ਘੱਟ 5 ਓਵਰ ਹਰੇਕ ਟੀਮ ਰਾਹੀਂ ਪੂਰੇ ਕੀਤੇ ਜਾਣੇ ਜ਼ਰੂਰੀ ਹਨ ।
4. ਆਉਣ ਵਾਲੇ ਬੱਲੇਬਾਜ਼ ਨੂੰ 90 ਸੈਕਿੰਡ ਦੇ ਅੰਦਰ ਅਗਲੀ ਬਾਲ ਦਾ ਸਾਹਮਣਾ ਕਰਨਾ ਹੋਵੇਗਾ । ਇਸ ਲਈ ਮੈਚ ਦੇ ਦੌਰਾਨ ਟੀਮ ਨੂੰ ਪੈਵੇਲੀਅਨ ਦੇ ਸਥਾਨ ਤੇ ਸੀਮਾ-ਰੇਖਾ ਦੇ ਨਜ਼ਦੀਕ ਬੈਠਣਾ ਹੋਵੇਗਾ ।
5. ਦੋਵੇਂ ਟੀਮਾਂ ਨੂੰ ਆਪਣੀ-ਆਪਣੀ ਪਾਰੀ 75 ਮਿੰਟ ਵਿੱਚ ਖ਼ਤਮ ਕਰਨੀ ਹੋਵੇਗੀ । ਜੇਕਰ ਖੇਤਰਕਸ਼ਨ’ (Field) ਕਰਨ ਵਾਲੀ ਟੀਮ ਇਸ ਤਰ੍ਹਾਂ ਕਰਨ ਵਿੱਚ ਅਸਫਲ ਹੁੰਦੀ ਹੈ ਤਾਂ ਬੱਲੇਬਾਜ਼ੀ ਕਰਨ ਵਾਲੀ ਟੀਮ ਨੂੰ ਬੋਨਸ ਦੇ ਤੌਰ ਤੇ ਪ੍ਰਤੀ ਓਵਰ 6 ਰਨ ਪ੍ਰਦਾਨ ਕੀਤੇ ਜਾਣਗੇ ।
6. ਇਕ ਬੱਲੇਬਾਜ਼ ਨੂੰ ਮੈਦਾਨ ਵਿੱਚ ਪਹੁੰਚਣ ਦੇ ਲਈ 90 ਸੈਕਿੰਡ ਮਿਲਦੇ ਹਨ । ਜੇਕਰ ਉਹ ਇਸ ਤਰ੍ਹਾਂ ਨਹੀਂ ਕਰਦਾ, ਤਾਂ ਉਸਨੂੰ ਟਾਈਮ ਆਊਟ ਮੰਨਿਆ ਜਾਵੇਗਾ ।
7.ਪਹਿਲੇ 6 ਓਵਰ ਵਿੱਚ ਕੇਵਲ ਦੋ ਖੇਤਰ ਰੱਖਿਅਕ 30 ਗਜ਼ ਦੇ ਦਾਇਰੇ ਦੇ ਬਾਹਰ ਰਹਿ ਸਕਦੇ ਹਨ । ਬਾਕੀ 14 ਓਵਰ ਵਿੱਚ 5 ਤੋਂ ਜ਼ਿਆਦਾ ਖੇਤਰ ਰੱਖਿਅਕ 30 ਗਜ਼ ਦੇ ਦਾਇਰੇ ਤੋਂ ਬਾਹਰ ਨਹੀਂ ਰਹਿ ਸਕਦੇ ।
8. ਇਕ ਗੇਂਦਬਾਜ਼ ਅਧਿਕਤਮ 4 ਓਵਰ ਕਰ ਸਕਦਾ ਹੈ |
9. ਇਕ ਨੋ ਬਾਲ ਸੁੱਟੇ ਜਾਣ ਦੇ ਬਾਅਦ ਖੇਡਣ ਵਾਲੇ ਬੱਲੇਬਾਜ਼ ਨੂੰ ਇਕ ਫਰੀ ਹਿੱਟ ਦਿੱਤੀ ਜਾਵੇਗੀ । ਉਹ ਰਨ ਆਊਟ ਹੋਣ ਦੇ ਇਲਾਵਾ ਕਿਸੇ ਵੀ ਸਥਿਤੀ ਵਿੱਚ ਆਊਟ ਨਹੀਂ ਮੰਨਿਆ ਜਾਵੇਗਾ ।
10. ਜੇਕਰ ਮੈਚ ਟਾਈ ਹੋ ਜਾਂਦਾ ਹੈ ਤਾਂ ਪੈਨਲਟੀ ਸ਼ੂਟ ਆਊਟ ਲਾਗੂ ਕੀਤਾ ਜਾਵੇਗਾ | ਹਰੇਕ ਟੀਮ ਪੰਜ ਗੇਂਦਬਾਜ਼ਾਂ ਨੂੰ ਚੁਣੇਗੀ ਜਾਂ ਦੂਸਰੇ ਦੇ ਵਿਕੇਟ ਨੂੰ ਹਿੱਟ ਕਰਨਗੇ । ਪਰ ਕੋਈ ਬੱਲੇਬਾਜ਼ ਇਸਦਾ ਸਾਹਮਣਾ ਨਹੀਂ ਕਰੇਗਾ । ਜ਼ਿਆਦਾਤਰ ਪ੍ਰਹਾਰ ਕਰਨ ਵਾਲੀ ਟੀਮ ਵਿਜੇਤਾ ਘੋਸ਼ਿਤ ਕੀਤੀ ਜਾਵੇਗੀ । ਇਸਨੂੰ ਬਾਲ ਆਊਟ ਰੂਲ ਵੀ ਕਹਿੰਦੇ ਹਨ ।

ਖੇਡ ਦੀ ਸ਼ਬਦਾਵਲੀ
(Important Terminology of the Game)
1. ਓਵਰ (Overy-ਇਕ ਓਵਰ ਵਿਚ 6 ਵਾਰ ਗੇਂਦ ਸੁੱਟੀ ਜਾਂਦੀ ਹੈ । ਇਹ ਓਵਰ ਵਿਕਟ ਦੇ ਸਿਰੇ ਤੇ ਵਾਰੀ-ਵਾਰੀ ਦਿੱਤੇ ਜਾਂਦੇ ਹਨ | ਜੇਕਰ ਪਹਿਲਾਂ ਨਿਸਚਿਤ ਕਰ ਲਿਆ ਜਾਵੇ, ਤਾਂ ਇਕ ਵਾਰ ਓਵਰ ਵਿਚ ਅੱਠ ਗੇਂਦਾਂ ਖੇਡੀਆਂ ਜਾ ਸਕਦੀਆਂ ਹਨ । “ਨੋ ਬਾਲ’ ਅਤੇ ‘ਵਾਈਡ ਬਾਲ’ ਓਵਰ ਵਿਚ ਨਹੀਂ ਗਿਣੇ ਜਾਣਗੇ । ਜਿੰਨੇ ਨੋ ਬਾਲ ਉਸ ਓਵਰ ਵਿਚ ਹੋਣਗੇ, ਉੱਨੀਆਂ ਹੀ ਹੋਰ ਗੇਂਦਾਂ ਸੁੱਟੀਆਂ ਜਾਣਗੀਆਂ । ਇਕ ਇਨਿੰਗਜ਼ ਵਿਚ ਕੋਈ ਵੀ ਬਾਊਲਰ ਲਗਾਤਾਰ ਦੋ ਓਵਰ ਬਾਉਲ ਨਹੀਂ ਕਰ ਸਕਦਾ । ਜੇਕਰ ਅੰਪਾਇਰ ਤੋਂ ਓਵਰ ਦੀਆਂ ਬਾਲਾਂ ਦੀ ਗਿਣਤੀ ਵਿਚ ਭੁੱਲ ਹੋ ਜਾਂਦੀ ਹੈ, ਤਾਂ ਅੰਪਾਇਰ ਦੁਆਰਾ ਗਿਣਿਆ ਗਿਆ ਓਵਰ ਨਹੀਂ ਮੰਨਿਆ ਜਾਵੇਗਾ ।
2. ਵਿਕਟਾਂ ਦਾ ਡਿੱਗਣਾ all of wicketsਗੇਂਦ ਬੈਟਸਮੈਨ ਖੁਦ ਜਾਂ ਉਸ ਦਾ ਬੈਟ ਜਾਂ ਗੇਂਦ ਸਟੈਪਜ਼ ਦੇ ਉੱਪਰ ਦੀਆਂ ਦੋਨੋਂ ਗਿੱਲੀਆਂ ਡੇਗ ਦੇਣ ਜਾਂ ਜ਼ੋਰ ਨਾਲ ਸਟੰਪ ਧਰਤੀ ਤੋਂ ਉੱਖੜ ਜਾਵੇ ਤਾਂ ਵਿਕਟ ਡਿੱਗਣਾ ਕਿਹਾ ਜਾਂਦਾ ਹੈ ।
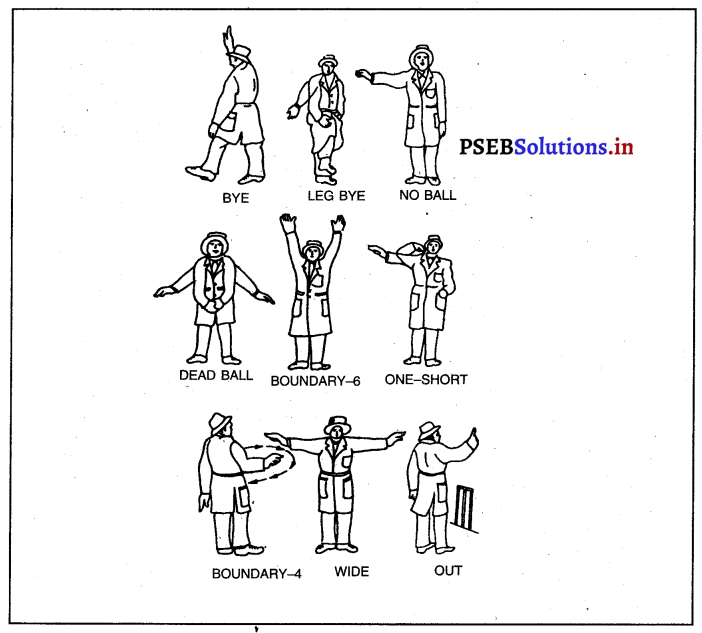
3. ਨੋ ਬਾਲ (No Ball-ਗੇਂਦ ਕਰਨ ਦੇ ਸਮੇਂ ਜੇਕਰ ਗੇਂਦਬਾਜ਼ ਦਾ ਅਗਲਾ ਪੁਰਾ ਪੈਰ ਬੈਟਿੰਗ ਕੀਜ਼ ਤੋਂ ਅੱਗੇ ਟੱਪ ਜਾਂਦਾ ਹੈ ਜਾਂ (Returning Crease) ਨੂੰ ਕੱਟਦਾ ਹੈ ਤਾਂ ਅੰਪਾਇਰ ਨੋ ਬਾਲ ਘੋਸ਼ਿਤ ਕਰ ਦਿੰਦਾ ਹੈ । ਬੈਟਸਮੈਨ ਨੋ ਬਾਲ ’ਤੇ ਹਿੱਟ ਲਗਾ ਕੇ ਜਿੰਨੀਆਂ ਵੀ ਦੌੜਾਂ ਸੰਭਵ ਹੋਣ, ਬਣਾ ਸਕਦਾ ਹੈ । ਇਸ ਤਰ੍ਹਾਂ ਬਣੀਆਂ ਦੌੜਾਂ ਨੂੰ ਕੁੱਲ ਸਕੋਰ ਵਿਚ ਜੋੜ ਲਿਆ ਜਾਵੇਗਾ । ਜੇਕਰ ਕੋਈ ਦੌੜ ਨਾ ਬਣੀ ਹੋਵੇ ਤਾਂ ਕੇਵਲ ਇਕ ਦੌੜ ਹੀ ਸਕੋਰ ਵਿਚ ਜੋੜੀ ਜਾਵੇਗੀ । ਅੰਪਾਇਰ ਆਪਣੀ ਇਕ ਭੁਜਾ ਫੈਲਾ ਕੇ ਨੋ ਬਾਲ ਦਾ ਇਸ਼ਾਰਾ ਦਿੰਦਾ ਹੈ ।
4. ਵਾਈਡ ਬਾਲ (wide Ball-ਜੇਕਰ ਬਾਉਲਰ ਬਾਲ ਨੂੰ ਵਿਕਟ ਤੋਂ ਇੰਨੀ ਉਚਾਈ ‘ਤੇ ਜਾਂ ਚੌੜਾਈ ‘ਤੇ ਸੁੱਟਦਾ ਹੈ ਕਿ ਅੰਪਾਇਰ ਦੇ ਵਿਚਾਰ ਵਿਚ ਇਹ ਬੈਟਸਮੈਨ ਦੀ ਪਹੁੰਚ ਤੋਂ ਬਾਹਰ ਹੈ, ਤਾਂ ਉਹ ਵਾਈਡ ਬਾਲ ਦੀ ਘੋਸ਼ਣਾ ਕਰ ਦਿੰਦਾ ਹੈ । ਜੋ ਦੌੜਾਂ ਵਾਈਡ ਬਾਲ ਦੇ ਸਮੇਂ ਬਣਨ ਉਨ੍ਹਾਂ ਨੂੰ ਵਾਈਡ ਬਾਲ ਵਿਚ ਗਿਣਿਆ ਜਾਂਦਾ ਹੈ । ਜੇਕਰ ਕੋਈ ਵੀ ਦੌੜ ਨਾ ਬਣੇ, ਤਾਂ ਇਕ ਦੌੜ ਸਮਝੀ ਜਾਂਦੀ ਹੈ । ਵਾਈਡ ਬਾਲ ਦਾ ਇਸ਼ਾਰਾ ਅੰਪਾਇਰ ਆਪਣੀਆਂ ਦੋਵੇਂ ਭੁਜਾਵਾਂ ਸਿੱਧੀਆਂ ਫੈਲਾ ਕੇ ਕਰਦਾ ਹੈ ।
5. ਬਾਈ ਅਤੇ ਲੈਗ ਬਾਈ (Bye and Leg-byਜੇਕਰ ਕੋਈ ਚੰਗੀ ਤਰ੍ਹਾਂ ਨਾਲ ਸੱਟੀ ਗੇਂਦ ਜਾਂ ਬੈਟਸਮੈਨ ਸਟਰਾਈਕਰ ਦੇ ਬੈਟ ਜਾਂ ਸਰੀਰ ਨੂੰ ਬਿਨਾਂ ਛੂਹੇ ਕੋਲੋਂ ਲੰਘ ਜਾਵੇ ਅਤੇ ਦੌੜ ਬਣ ਜਾਵੇ ਤਾਂ ਅੰਪਾਇਰ ਬਾਈ ਘੋਸ਼ਿਤ ਕਰੇਗਾ । ਪਰ ਨੋ ਬਾਲ ਜਾਂ ਵਾਈਡ ਬਾਲ ਨਹੀਂ ਹੋਣਾ ਚਾਹੀਦਾ | ਪਰ ਜੇਕਰ ਗੇਂਦ ਬੈਟਸਮੈਨ ਦੇ ਬੈਟ ਵਾਲੇ ਹੱਥ ਨੂੰ ਛੱਡ ਕੇ ਸਰੀਰ ਦੇ ਕਿਸੇ ਭਾਗ ਨੂੰ ਛੂਹ ਕੇ ਕੋਲੋਂ ਲੰਘ ਜਾਵੇ ਅਤੇ ਦੌੜ ਬਣ ਜਾਵੇ ਤਾਂ ਅੰਪਾਇਰ ਲੈਗ ਬਾਈ ਘੋਸ਼ਿਤ ਕਰੇਗਾ ।
6. ਆਪਣੇ ਖੇਤਰ ਤੋਂ ਬਾਹਰ (Out of his Area-ਬੈਟਸਮੈਨ ਆਪਣੇ ਖੇਤਰ ਤੋਂ ਬਾਹਰ ਮੰਨਿਆ ਜਾਵੇਗਾ, ਜਦੋਂ ਤਕ ਉਸ ਦੇ ਹੱਥ ਦੇ ਬੈਟ ਦਾ ਕੁੱਝ ਭਾਗ ਜਾਂ ਉਸ ਦਾ ਸਰੀਰ ਕਲਪਿਤ ਮੰਜ ਰੇਖਾ ਦੇ ਪਿੱਛੇ ਜ਼ਮੀਨ ਤੇ ਨਾ ਹੋਵੇ |
7. ਬੈਟਸਮੈਨ ਦਾ ਰਿਟਾਇਰ ਹੋਣਾ (Getting Retired of a batsmen)-ਬੈਟਸਮੈਨ ਕਿਸੇ ਵੀ ਸਮੇਂ ਜ਼ਖ਼ਮੀ ਜਾਂ ਬੀਮਾਰੀ ਦੀ ਹਾਲਤ ਵਿਚ ਰਿਟਾਇਰ ਹੋ ਸਕਦਾ ਹੈ । ਉਹ ਬੱਲੇਬਾਜ਼ੀ ਤਾਂ ਕਰ ਸਕਦਾ ਹੈ ਪਰ ਉਸ ਨੂੰ ਵਿਰੋਧੀ ਕਪਤਾਨ ਤੋਂ ਆਗਿਆ ਲੈਣੀ ਹੋਵੇਗੀ ਕਿ ਕਿੰਨਵੇਂ ਨੰਬਰ ਤੇ ਬੱਲੇਬਾਜ਼ੀ ਕਰੇ ।
8. ਬਾਊਲਡ (Bowled–ਜੇਕਰ ਵਿਕਟ ਗੇਂਦ ਕਰ ਕੇ ਡੇਗ ਦਿੱਤੀ ਜਾਵੇ, ਤਾਂ ਗੇਂਦ ਖੇਡਣ ਵਾਲਾ ਬਾਊਲਡ (Bowled Out) ਅਖਵਾਉਂਦਾ ਹੈ, ਭਾਵੇਂ ਗੇਂਦ ਪਹਿਲੇ ਉਸ ਦੇ ਪੈਰ ਜਾਂ ਸਰੀਰ ਨੂੰ ਛੂਹ ਚੁੱਕੀ ਹੋਵੇ ।
9. ਕੈਚ (Catchਜੇਕਰ ਗੇਂਦ ਬੈਟ ਦੇ ਵਾਰ ਨਾਲ, ਜਾਂ ਬੈਟ ਨਾਲੋਂ ਹੱਥ ਨਾਲ ਕਲਾਈ ਨਾਲ ਨਹੀਂ ਲਗ ਕੇ ਧਰਤੀ ਛੂਹਣ ਤੋਂ ਪਹਿਲਾਂ ਕਿਸੇ ਫੀਲਡਰ ਦੁਆਰਾ ਬੋਚ ਲਈ (ਲਪਕ) ਲਈ ਜਾਵੇ ਤਾਂ ਬੈਟਸਮੈਨ ਕੈਚ ਆਊਟ ਹੋਵੇਗਾ । ਕੈਚ ਦੇ ਸਮੇਂ ਰੱਖਿਅਕ ਦੇ ਦੋਵੇਂ ਪੈਰ ਪੂਰੀ ਤਰ੍ਹਾਂ ਮੈਦਾਨ ਵਿਚ ਹੋਣ । ਜੇਕਰ ਖੇਤਰ ਰੱਖਿਅਕ ਸੀਮਾ ਰੇਖਾ ਤੋਂ ਬਾਹਰ ਕੈਚ ਫੜਦਾ ਹੈ ਤਾਂ ਬੈਟਸਮੈਨ ਆਉਟ ਨਹੀਂ ਮੰਨਿਆ ਜਾਂਦਾ, ਸਗੋਂ ਉਸ ਨੂੰ 6 ਰਨ ਮਿਲਦੇ ਹਨ । ਜੇਕਰ ਗੇਂਦ ਵਿਕਟ ਕੀਪਰ ਦੇ ਪੈਰਾਂ ਵਿਚ ਜਾ ਵਸੇ ਤਾਂ ਵੀ ਬੈਟਸਮੈਨ ਆਉਟ ਮੰਨਿਆ ਜਾਵੇਗਾ |
10. ਗੇਂਦ ਨੂੰ ਹੱਥ ਲਾਉਣਾ (Handle the Ballਜੇਕਰ ਹੱਥਾਂ ਨਾਲ ਖੇਡਦੇ ਸਮੇਂ ਕੋਈ ਬੈਟਸਮੈਨ ਗੇਂਦ ਨੂੰ ਛੂਹ ਲੈਂਦਾ ਹੈ ਤਾਂ ਉਸ ਨੂੰ ਗੇਂਦ ਦੇ ਨਾਲ ਹੱਥ ਲਗਾਇਆ ਆਉਟ ਮੰਨਿਆ ਜਾਵੇਗਾ ।
11. ਗੇਂਦ ‘ਤੇ “ਦੋ ਵਾਰ (Hit the Ball twice-ਬੈਟਸਮੈਨ ਗੇਂਦ ਤੇ ਦੋ ਵਾਰ ਕਰਨ ਨਾਲ ਆਊਟ ਹੋਵੇਗਾ । ਜੇਕਰ ਗੇਂਦ ਉਸਦੇ ਸਰੀਰ ਦੇ ਕਿਸੇ ਭਾਗ ਨੂੰ ਲਗ ਕੇ ਰੁਕ ਜਾਂਦੀ ਹੈ ਜਾਂ ਉਹ ਉਸ ਤੇ ਦੁਬਾਰਾ ਜਾਣ ਬੁੱਝ ਕੇ ਵਾਰ ਕਰਦਾ ਹੈ । ਕੇਵਲ ਆਪਣੀ ਵਿਕਟ ਦੇ ਬਚਾਅ ਲਈ ਵੀ ਵਾਰ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ । ਪਰੰਤੂ ਇਹ ਸ਼ਰਤ ਹੈ ਕਿ ਅਜਿਹਾ ਵਿਕਟ ਦੇ ਬਚਾਅ ਲਈ ਕੀਤਾ ਗਿਆ ਹੋਵੇ ਇਸ ਪ੍ਰਕਾਰ ਜੇ ਕੋਈ ਰਨ ਬਣ ਵੀ ਜਾਵੇ ਤਾਂ ਉਹ ਗਿਣਿਆ ਨਹੀਂ ਜਾਂਦਾ ।
12. ਵਿਕਟ ‘ਤੇ ਵਾਰ (wicket is down or Hit wicketਜੇਕਰ ਗੇਂਦ ਖੇਡਦੇ ਸਮੇਂ ਬੈਟਸਮੈਨ ਆਪਣੇ ਬੈਟ ਜਾਂ ਸਰੀਰ ਦੇ ਕਿਸੇ ਭਾਗ ਨਾਲ ਵਿਕਟਾਂ ਡੇਗਦਾ ਹੈ, ਤਾਂ ਉਸ ਨੂੰ ‘ਵਿਕਟ ਤੇ ਵਾਰ’ ਆਊਟ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ । ਜੇਕਰ ਉਸ ਦੀ ਵਿਕਟ ਟੋਪੀ ਜਾਂ ਹੈਟ ਡਿੱਗਣ ਜਾਂ ਬੈਟ ਦੇ ਟੁੱਟੇ ਹੋਏ ਕਿਸੇ ਭਾਗ ਦੇ ਵੱਜਣ ਨਾਲ ਡਿਗ ਜਾਂਦੀ ਹੈ, ਤਾਂ ਉਸਨੂੰ ਵੀ ‘ਵਿਕਟ ਤੇ ਵਾਰ` ਮੰਨਿਆ ਜਾਵੇਗਾ ।
13. ਐੱਲ. ਬੀ.ਡਬਲਿਉ. ‘ (ਲੈਂਗ ਬਿਫੋਰ ਵਿਕੇਟ (Leg Before wicked-ਬੈਟਸਮੈਨ ਉਸ ਸਮੇਂ ਐੱਲ. ਬੀ. ਡਬਲਿਊ. ਆਉਟ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ, ਜਦੋਂ ਉਹ ਗੇਂਦ ਨੂੰ ਬੱਲੇ ਨਾਲ ਛੁਹਣ ਤੋਂ ਪਹਿਲਾਂ ਸਰੀਰ ਦੇ ਕਿਸੇ ਭਾਗ ਨਾਲ ਰੋਕਣ ਦਾ ਯਤਨ ਕਰਦਾ ਹੈ ਅਤੇ ਅੰਪਾਇਰ ਅਨੁਸਾਰ ਗੇਂਦ ‘ਤੇ ਵਿਕਟ ਸਿੱਧੀ ਰੇਖਾ ਵਿਚ ਹੈ । ਜੇਕਰ ਬੈਟਸਮੈਨ ਇਸ ਨੂੰ ਆਪਣੇ ਸਰੀਰ ਦੇ ਕਿਸੇ ਭਾਗ ਨਾਲ ਨਾ ਰੋਕਦਾ ਤਾਂ ਗੇਂਦ ਵਿਕਟ ‘ਤੇ ਹੀ ਲਗਦੀ ।
14. ਖੇਤਰ ਵਿਚ ਰੋਕ (Intervene in Area)-ਕੋਈ ਵੀ ਬੈਟਸਮੈਨ ਖੇਤਰ ਵਿਚ ਰੋਕ ਆਉਟ ਹੋ ਸਕਦਾ ਹੈ, ਜੇਕਰ ਉਹ ਜਾਣ-ਬੁੱਝ ਕੇ ਕਿਸੇ ਫੀਲਡਰ ਨੂੰ ਗੇਂਦ ਫੜਨ ਤੋਂ ਰੋਕਦਾ ਹੈ ।
15. ਸਟੰਪਡ (Stumped-ਬੈਟਸਮੈਨ ਦੇ ਹੱਥ ਦਾ ਬੈਟ ਜਾਂ ਉਸ ਦਾ ਪੈਰ ਮੰਨੀ ਗਈ ਮੰਜ ਰੇਖਾ ਦੇ ਪਿੱਛੇ ਧਰਤੀ ‘ਤੇ ਨਾ ਹੋਵੇ, ਤਾਂ ਉਹ ਖੇਤਰ ਤੋਂ ਬਾਹਰ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ । ਬੈਟਸਮੈਨ ਉਸ ਸਮੇਂ ਸਟੰਪ ਆਉਟ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ, ਜਦੋਂ ਗੇਂਦ ਨੋ ਬਾਲ ਨਾ ਹੋਵੇ ਅਤੇ ਬਾਉਲਰ ਦੁਆਰਾ ਸੁੱਟੀ ਗਈ ਹੋਵੇ ਅਤੇ ਉਹ ਦੌੜ ਬਣਾਉਣ ਦੀ ਕੋਸ਼ਿਸ਼ ਦੀ ਸਥਿਤੀ ਤੋਂ ਇਲਾਵਾ ਉਹ ਖੇਤਰ ਤੋਂ ਬਾਹਰ ਚਲਿਆ ਜਾਵੇ ਅਤੇ ਵਿਕਟ ਕੀਪਰ ਵਿਕਟ ਉਖਾੜ ਸੁੱਟੇ ।ਉਖਾੜ ਸੁੱਟੇ ਜਾਂ ਵਿਕਟਾਂ ਦੇ ਉੱਪਰ ਰੱਖੀਆਂ ਗੁੱਲੀਆਂ ਉਤਾਰ ਦੇਵੇ ।
16. ਰਨ ਆਊਟ (Run Out-ਜਿਸ ਸਮੇਂ ਗੇਂਦ ਮੈਦਾਨ ਵਿਚ ਹੋਵੇ ਤਾਂ ਬੈਟਸਮੈਨ ਭੱਜਦੇ ਹੋਏ ਖੇਤਰ ਤੋਂ ਬਾਹਰ ਚਲਿਆ ਜਾਏ ਅਤੇ ਵਿਰੋਧੀ ਟੀਮ ਦਾ ਖਿਡਾਰੀ ਉਸ ਦੀ ਵਿਕਟ ਡੇਗ ਦੇਵੇ, ਤਾਂ ਬੈਟਸਮੈਨ ਰਨ ਆਉਟ ਹੋ ਜਾਂਦਾ ਹੈ । ਜੇਕਰ ਬੈਟਸਮੈਨ ਇਕ ਦੂਜੇ ਨੂੰ ਪਾਰ ਕਰ ਜਾਣ, ਤਾਂ ਉਸ ਬੈਟਸਮੈਨ ਨੂੰ ਆਉਟ ਮੰਨਿਆ ਜਾਵੇਗਾ, ਜੋ ਡਿੱਗੀ ਹੋਈ ਵਿਕਟ ਵਲ ਦੌੜ ਰਿਹਾ ਹੋਵੇ ।
17. ਵਿਕਟ ਰੱਖਿਅਕ (wicket Keeper)-ਵਿਕਟ ਕੀਪਰ ਸਦਾ ਵਿਕਟਾਂ ਦੇ ਪਿੱਛੇ ਰਹੇਗਾ ਜਦੋਂ ਤਕ ਕਿ ਬਾਉਲਰ ਦੁਆਰਾ ਟੁੱਟੀ ਹੋਈ ਗੇਂਦ ਨੂੰ ਬੈਟਸਮੈਨ ਦੇ ਬੈਟ ਜਾਂ ਸਰੀਰ ਦੇ ਕਿਸੇ ਹਿੱਸੇ ਨਾਲ ਛੋਹ ਨਹੀਂ ਜਾਂਦੀ ਜਾਂ ਵਿਕਟ ਦੇ ਪਾਰ ਨਹੀਂ ਜਾਂਦੀ ਜਾਂ ਬੈਟਸਮੈਨ ਆਊਟ ਨਹੀਂ ਹੋ ਜਾਂਦਾ, ਵਿਕਟ ਰੱਖਿਅਕ ਗੇਂਦ ਨੂੰ ਨਹੀਂ ਪਕੜ ਸਕਦਾ ।
18. ਖੇਤਰ ਰੱਖਿਅਕ (Fielders)-ਖੇਤਰ ਰੱਖਿਅਕ ਆਪਣੇ ਸਰੀਰ ਦੇ ਕਿਸੇ ਵੀ ਹਿੱਸੇ ਨਾਲ ਗੇਂਦ ਨੂੰ ਰੋਕ ਸਕਦਾ ਹੈ । ਉਸ ਨੂੰ ਆਪਣੀ ਟੋਪੀ ਨਾਲ ਗੱਦ ਰੋਕਣ ਦੀ ਆਗਿਆ ਨਹੀਂ । ਜੇਕਰ ਉਹ ਇਸ ਤਰ੍ਹਾਂ ਕਰਦਾ ਹੈ, ਤਾਂ ਇਸ ਦੀ ਸਜ਼ਾ ਚਾਰ ਦੌੜਾਂ ਹੋਣਗੀਆਂ । ਜੇਕਰ ਉਸ ਦੀ ਕੋਈ ਦੌੜ ਨਾ ਬਣੀ ਹੋਵੇ, ਤਾਂ ਚਾਰ ਦੌੜਾਂ ਜੋੜ ਦਿੱਤੀਆਂ ਜਾਣਗੀਆਂ।

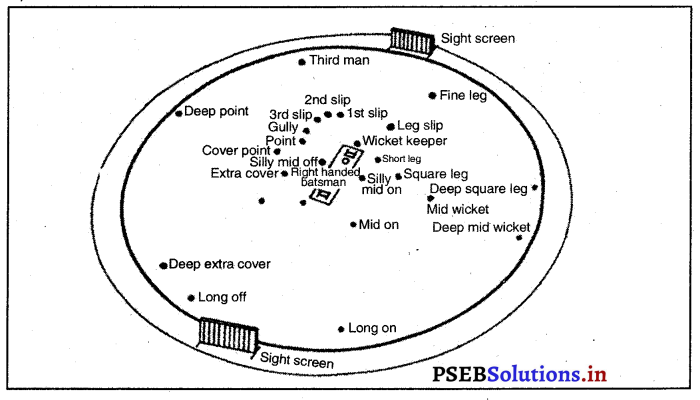
ਕ੍ਰਿਕੇਟ ਖੇਡ ਵਿਚ ਫੀਲਡ ਸੈਟਿੰਗ
19. ਮੈਡੇਟਰੀ ਓਵਰ (Mandatory Over-ਮੈਚ ਦੇ ਆਖ਼ਰੀ ਦਿਨ ਮੈਚ ਸਮਾਪਤ ਹੋਣ ਤੋਂ ਇਕ ਘੰਟਾ ਪਹਿਲਾਂ ਅੰਪਾਇਰ ਮੈਂਡੇਟਰੀ ਓਵਰ ਦਾ ਸੰਕੇਤ ਦਿੰਦਾ ਹੈ । ਉਸ ਤੋਂ ਬਾਅਦ 20 ਓਵਰਾਂ ਦੀ ਇਕ ਹੋਰ ਖੇਡ ਖੇਡੀ ਜਾਂਦੀ ਹੈ । ਹਰ ਇਕ ਓਵਰ ਵਿਚ 6 ਬਾਲ ਖੇਡੇ ਜਾਂਦੇ ਹਨ । ਜੇਕਰ ਮੈਚ ਬਰਾਬਰ ਹੁੰਦਾ ਪ੍ਰਤੀਤ ਹੋਵੇ, ਤਾਂ ਇਨ੍ਹਾਂ ਓਵਰਾਂ ਤੋਂ ਪਹਿਲਾਂ ਵੀ ਖੇਡ ਸ਼ਮਾਪਤ ਕੀਤੀ ਜਾ ਸਕਦੀ ਹੈ ।
20. ਡੈੱਡ ਬਾਲ (Dead Ballਬਾਲ ਉਨ੍ਹਾਂ ਹਾਲਤਾਂ ਵਿਚ ਹੀ ਰੈੱਡ ਮੰਨੀ ਜਾਂਦੀ ਹੈ, ਜਦ ਕਿ ਉਹ ਠੀਕ ਤਰ੍ਹਾਂ ਬਾਉਲਰ ਜਾਂ ਵਿਕਟ ਕੀਪਰ ਦੇ ਕਾਬੂ ਹੋ ਜਾਏ ਜਾਂ ਸੀਮਾ ਤੇ ਪਹੁੰਚ ਜਾਵੇ, ਅੰਪਾਇਰ ਜਾਂ ਬੈਟਸਮੈਨ ਦੇ ਕੱਪੜਿਆਂ ਵਿਚ , ਉਲਝ ਜਾਵੇ ਜਾਂ ਅੰਪਾਇਰ ਦੁਆਰਾ ਸਮੇਂ ਜਾਂ ਓਵਰ ਦੀ ਘੋਸ਼ਣਾ ਕਰ ਦਿੱਤੀ ਜਾਵੇ ; ਇਨ੍ਹਾਂ ਤੋਂ ਇਲਾਵਾ ਜਦ ਖਿਡਾਰੀ ਆਊਟ ਹੋ ਜਾਂਦਾ ਹੈ ਜਾਂ ਉਸ ਨੂੰ ਗੰਭੀਰ ਸੱਟ ਲੱਗ ਜਾਂਦੀ ਹੈ ।
21. ਮੈਦਾਨ ਦੀ ਅੜਚਨ (Obstructing the Field)-ਜੇਕਰ ਕੋਈ ਬੱਲੇ-ਬਾਜ਼ ਜਾਣ ਬੁੱਝ ਕੇ ਦੂਸਰੀ ਟੀਮ ਦੀ . ਖੇਡ ਵਿਚ ਅੜਚਨ ਪਾਉਂਦਾ ਹੈ, ਜਿਸ ਕਾਰਨ ਵਿਰੋਧੀ ਟੀਮ ਨੂੰ ਬਾਲ ਫੜਨ ਵਿਚ ਰੁਕਾਵਟ ਆਉਂਦੀ ਹੈ ਤਾਂ ਰੋਕਣ ਵਾਲੇ , ਬੈਟਸਮੈਨ ਨੂੰ ਆਊਟ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ | ਅਜਿਹਾ ਕਰਨੇ ਨੂੰ ਮੈਦਾਨ ਦੀ ਅੜਚਨ ਕਿਹਾ ਜਾਂਦਾ ਹੈ ।
22. ਇਕ ਦਿਨ ਦਾ ਮੈਚ (One Day Match-ਰਾਸ਼ਟਰੀ ਅਤੇ ਅੰਤਰ ਰਾਸ਼ਟਰੀ ਇਕ ਦਿਨ ਦਾ ਮੈਚ ਹੁੰਦਾ ਹੈ । ਜਿਸ ਵਿਚ ਦੋਵੇਂ ਟੀਮਾਂ 40-40 ਜਾਂ 50-50 ਓਵਰ ਦੇ ਮੈਚ ਖੇਡਦੀਆਂ ਹਨ, ਜੋ ਟੀਮ ਵੱਧ ਰਨ ਬਣਾ ਜਾਵੇ, ਉਹ ਜਿੱਤ ਜਾਂਦੀ ਹੈ ।
ਕ੍ਰਿਕਟ ਖੇਡ ਦੀਆਂ ਕੁੱਝ ਮਹੱਤਵਪੂਰਨ ਤਕਨੀਕਾਂ (Important techniques of Cricket Game):
ਕ੍ਰਿਕਟ ਵਿਚ ਬੈਟਿੰਗ ਮੁਹਾਰਿਤ ਅਤੇ ਤਕਨੀਕਾਂ ਕਿਸੇ ਵੀ ਹਿਟ ਨੂੰ ਸਫਲਤਾ ਪੂਰਵਕ ਖੇਡਣ ਲਈ ਬੈਟਸਮੈਨਾਂ ਨੂੰ ਤਿੰਨ ਗੱਲਾਂ ਦਾ ਧਿਆਨ ਰੱਖਣਾ ਚਾਹੀਦਾ ਹੈ ; ਉਸ ਨੂੰ ਜ਼ਰੂਰ ਹੀ ਪਹਿਲਾਂ ਬਾਲ ਨੂੰ ਲੱਭਣਾ ਚਾਹੀਦਾ ਹੈ ਅਤੇ ਫਿਰ ਬਾਲ ਵੱਲ ਧਿਆਨ ਰੱਖਣਾ । ਉਸ ਨੇ ਇਹ ਫੈਸਲਾ ਕਰਨਾ ਹੁੰਦਾ ਹੈ ਕਿ ਕਿਹੜੀ ਹਿੱਟ ਠੀਕ ਹੈ ।ਉਸ ਹਿੱਟ ਨੂੰ ਠੀਕ ਤਰ੍ਹਾਂ ਖੇਡਣ ਲਈ ਆਪਣੇ ਬਦਨ ਨੂੰ ਮੋੜਨਾ ਚਾਹੀਦਾ ਹੈ ।

ਕਹਿਣ ਨੂੰ ਤਾਂ ਕਾਫੀ ਆਸਾਨ ਹੈ, ਪਰ ਅਸਲ ਵਿਚ ਏਨਾ ਆਸਾਨ ਨਹੀਂ ਹੈ । ਇਹ ਗੱਲ ਸੋਚਣ ਲਈ ਤਾਂ ਆਸਾਨ ਹੈ ਕਿ ਤੁਸੀਂ ਬਾਲ ਵੱਲ ਵੇਖ ਰਹੇ ਹੋ । ਸੱਚਮੁੱਚ ਕਿਸੇ ਆ ਰਹੇ ਬਾਲ ਨੂੰ ਤੱਕਣਾ ਆਸਾਨ ਹੈ, ਬਸ਼ਰਤੇ ਕਿ ਤੁਸੀਂ ਆਪਣਾ ਮਨ ਬਣਾਇਆ ਹੋਇਆ ਹੋਵੇ | ਪਰ ਪੂਰੀ ਪਾਰੀ ਵਿਚ ਹਰੇਕ ਬਾਲ ਦੀ ਜਾਂਚ ਕਰਨ ਦੀ ਆਦਤ ਬਣਾਉਣੀ, ਸਹੀ ਅਰਥਾਂ ਵਿਚ ਜਾਂਚ ਕਰਨ ਦੀ, ਇਕ ਬੜਾ ਔਖਾ ਕੰਮ ਹੈ, ਤੁਸੀਂ ਅਜਿਹਾ ਸਿਰਫ ਆਪਣੇ ਹੱਥਾਂ ਵਿਚਲੇ ਕੰਮ ਉੱਤੇ ਧਿਆਨ ਕੇਂਦਰਿਤ ਕਰਨਾ ਸਿੱਖ ਕੇ ਹੀ ਕਰ ਸਕਦੇ ਹੋ । ਇਹ ਸੱਚਮੁੱਚ ਬੜਾ ਔਖਾ ਹੈ, ਪਰ ਜੇ ਤੁਸੀਂ ਇਸ ਤਰ੍ਹਾਂ ਕਰਨਾ ਸਿੱਖ | ਲੈਂਦੇ ਹੋ, ਤਾਂ ਉਹ ਤੁਹਾਨੂੰ ਕ੍ਰਿਕਟ ਵਿਚ ਹੀ ਸਹਾਈ ਸਿੱਧ ਨਹੀਂ ਹੋਵੇਗਾ, ਸਗੋਂ ਜ਼ਿੰਦਗੀ ਵਿਚ ਵੀ । ਠੀਕ ਇਸ ਤਰ੍ਹਾਂ ਇਹ ਫੈਸਲਾ ਕਰਨਾ ਕਿ ਕਿਸੇ ਵਿਸ਼ੇਸ਼ ਬਾਲ ਨੂੰ ਕਿਸ ਤਰ੍ਹਾਂ ਹਿੱਟ ਕਰਨਾ ਹੈ, ਇਹ ਇਕ ਤਰ੍ਹਾਂ ਨਾਲ ਅੰਤਰ-ਪ੍ਰੇਰਨਾ ਦਾ ਮਾਮਲਾ ਹੈ, ਜਾਂ ਜਿਸ ਨੂੰ ਅਕਸਰ ਕ੍ਰਿਕਟ ਵਿਚ ‘ਬਾਲ ਸੂਝ’ ਕਿਹਾ ਜਾਂਦਾ ਹੈ । ਪਰ ਇਹ ਮੁੱਖ ਤੌਰ ਤੇ ਤਜਰਬੇ ਦਾ ਕੰਮ ਹੈ ।
ਖਿਡਾਰੀ ਦੀ ਸਥਿਤੀ ‘
ਇਕ ਖਿਡਾਰੀ ਦੀ ਆਰਾਮਦਾਇਕ, ਤਣਾਅ-ਰਹਿਤ ਅਤੇ ਸੰਤਲਿਤ ਸਥਿਤੀ ਬੜੀ ਜ਼ਰੂਰੀ ਹੈ, ਬਾਲ ਦੀ ਸਹੀ ਪਰਖ ਕਰਨੀ ਅਤੇ ਹਰੇਕ ਸਟਰੋਕ ਲਈ ਪੈਰਾਂ ਦੀ ਹਿਲਜੁਲ ਇਸ ਉੱਤੇ ਹੀ ਨਿਰਭਰ ਕਰਦੀ ਹੈ ।
ਪੈਰ ਸਾਧਾਰਨ ਤੌਰ ‘ਤੇ ਕਰੀਜ਼ ਦੇ ਪਾਸਿਆਂ ਵੱਲ ਸਮਾਨਾਂਤਰ ਹੋਣੇ ਚਾਹੀਦੇ ਹਨ। ਅਤੇ ਉਨ੍ਹਾਂ ਦੇ ਪੰਜੇ ਨਿਸ਼ਾਨੇ ਵੱਲ ਹੋਣੇ ਚਾਹੀਦੇ ਹਨ ।
ਬੈਕ ਲਿਫਟ
ਇਕ ਸਹੀ ‘ਬੈਕ ਲਿਫਟ ਦੀ ਬਹੁਤ ਮਹੱਤਤਾ ਹੈ । ਖੱਬੀ ਬਾਂਹ ਅਤੇ ਗੁੱਟ ਨੂੰ ਹੀ ਸਾਰਾ ਕੰਮ ਕਰਨਾ ਚਾਹੀਦਾ ਹੈ ਅਤੇ ਬੈਟ ਦਾ ਸਾਹਮਣਾ ਪਾਸਾ ਨਿਸ਼ਾਨੇ ਵੱਲ, ਜਿਵੇਂ ਕਿ ਬੈਟ ਉਭਰਦਾ ਹੈ । ਸਿਰ ਅਤੇ ਬਦਨ ਬਿਲਕੁਲ ਸਥਿਰ ਹੋਣੇ ਚਾਹੀਦੇ ਹਨ | ਉਭਾਰ ਕੇ ਅਖੀਰ ਤੇ ਸੱਜੀ ਕੂਹਣੀ ਬਦਨ ਤੋਂ ਥੋੜ੍ਹੀ ਜਿਹੀ ਹਟੀ ਹੋਣੀ ਚਾਹੀਦੀ ਹੈ ਅਤੇ ਖੱਬਾ ਹੱਥ ਪੈਂਟ ਦੀ ਸੱਜੀ ਜੇਬ ਦੇ ਬਿਲਕੁਲ ਸਾਹਮਣੇ ਉੱਪਰ ਵੱਲ ਹੋਣਾ ਚਾਹੀਦਾ ਹੈ ।

ਸਿੱਧੇ ਬਾਲ ਲਈ ਸਾਹਮਣੀ ਸੁਰੱਖਿਆ ਹਿੱਟ
ਸਾਹਮਣੀ ਹਿੱਟ ਸੁਰੱਖਿਆ ਵਿਚ ਨਾ ਸਿਰਫ ਬਹੁ-ਕੀਮਤੀ ਹੈ, ਸਗੋਂ ਸਾਰੀਆਂ ਹਿੱਟਾਂ ਦਾ | ਆਧਾਰ ਵੀ ਹੈ, ਇਸ ਨੂੰ ਠੀਕ ਢੰਗ ਨਾਲ ਖੇਡਣਾ ਲਗਪਗ ਅੱਧਾ ਬੈਟਸਮੈਨ ਬਣਨ ਦੇ ਤੁਲ ਹੈ । ਉਦੇਸ਼ ਬਾਲ ਨੂੰ ਜਿੰਨਾ ਪੁਆਇੰਟ ਦੇ ਨੇੜੇ ਸੰਭਵ ਹੋ ਸਕੇ ਖੇਡਣਾ ਹੈ । ਸਿਰ ਅੱਗੇ ਵੱਲ ਵਧਾਉਂਦਿਆਂ, ਖੱਬਾ ਕੂਲਾ : ਤੇ ਮੋਢਾ ਬਾਲ ਦੀ ਰੇਖਾ ਤੋਂ ਬਾਹਰ ਰੱਖ ਕੇ ਬਾਲ ਨੂੰ ਬੈਟ ਤੇ ਖੱਬੇ ਪੈਰ ਦੇ ਕੁੱਝ ਇੰਚ ਸਾਹਮਣੇ ਲੈਣਾ ਹੁੰਦਾ ਹੈ ਅਤੇ ਪੈਰ ਮਿਡ-ਆਫ ਅਤੇ ਐਕਸਟਰਾ ਕਵਰ ਦੇ ਵਿਚਕਾਰ ਦੀ ਸੇਧ ਵਿਚ ਹੋਣਾ ਚਾਹੀਦਾ ਹੈ ।

ਬਦਨ ਦਾ ਭਾਰ ਮੁੜੇ ਹੋਏ ਖੱਬੇ ਗੋਡੇ ਨਾਲ ਬਿਲਕੁਲ ਸਾਹਮਣੇ ਵੱਲ ਹੋਣਾ ਚਾਹੀਦਾ ਹੈ । ਬਾਲ ਦੀ ਸਾਰਾ ਰਸਤਾ ਪਰਖ ਕਰੋ । ਇਸ ਤਰ੍ਹਾਂ ਕਰਨ ਲਈ ਤੁਹਾਨੂੰ ਆਪਣਾ ਸਿਰ ਜਿੱਥੇ ਤਕ ਹੋ ਸਕੇ ਸੰਤੁਲਨ ਵਿਚ ਰੱਖਣਾ ਚਾਹੀਦਾ ਹੈ । ਸਿਰ ਉੱਪਰ ਚੁੱਕਣ ਲਈ ਲਾਲਚ ਨੂੰ ਘੱਟ ਕਰੋ ।
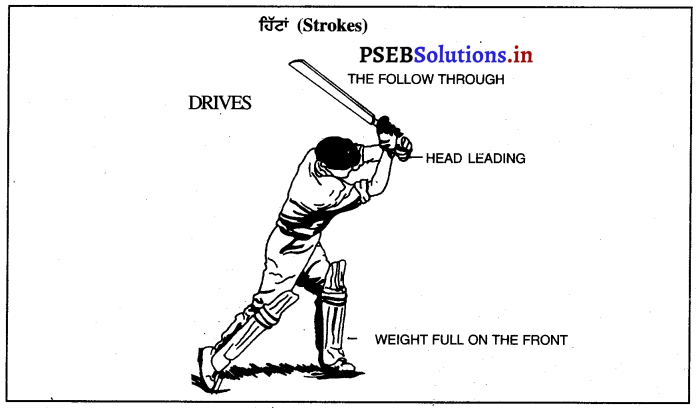
ਹਿੱਟਾਂ ਵਿਚ ਕੰਟਰੋਲ ਲਾਜ਼ਮੀ ਹੈ-ਜੇ ਤੁਸੀਂ ਮਜ਼ਬੂਤ ਹਿੱਟ ਮਾਰਨੀ ਚਾਹੁੰਦੇ ਹੋ, ਤਾਂ ਤੁਹਾਡੀ ਹਿੱਟ ਘੁੰਮਣ ਦੀ ਬਜਾਏ ਵਧੇਰੇ ਲੰਬੀ ਹੋ ਸਕਦੀ ਹੈ । | ਬਾਲ ਨੂੰ ਸਾਫ-ਸਾਫ ਤੇ ਸੌਖੀ ਤਰ੍ਹਾਂ ਹਿਟ ਕਰਨ ਲਈ, ਉਸ ਨੂੰ ਸੀਮਾ (ਬਾਊਂਡਰੀ) ਵਲ ਸੁੱਟਣ ਨਾਲੋਂ ਮੈਦਾਨ ਵਿਚ ਸੁੱਟਣਾ ਚਾਹੀਦਾ ਹੈ । ਜੇ ਬਾਲ ਕਾਫੀ ਦੂਰ ਉੱਪਰ ਹੈ ਤਾਂ ਹਿੱਟ ਇੱਕੋ ਲੰਬੇ ਕਦਮ ਨਾਲ ਮਾਰੀ ਜਾ ਸਕਦੀ ਹੈ, ਪਰ ਤੁਹਾਨੂੰ ਪਿੱਚ ਉੱਤੇ ਘੱਟ ਰਫਤਾਰ, ਤੇਜ਼ ਅਤੇ ਅਧੂਰੇ (Shorter) ਬਾਲ ਨੂੰ ਖੇਡਣ ਲਈ ਪੈਰਾਂ ਦੀ ਵਰਤੋਂ ਕਰਨੀ ਵੀ ਸਿੱਖਣੀ ਜ਼ਰੂਰੀ ਹੈ ।
ਸੁਰੱਖਿਆ ਲਈ ਬੈਕ ਸਟਰੋਕ
ਜਦੋਂ ਤਕ ਇਕ ਬੈਟਸਮੈਨ ਬਾਲ ਦੀ ਪਿੱਚ ਦੀ ਚੰਗੀ ਤਰ੍ਹਾਂ ਪਰਖ ਨਹੀਂ ਕਰ ਲੈਂਦਾ ਤਾਂ ਉਸ ਨੂੰ ਬੈਕ ਸਟਰੋਕ ਨਾਲ ਹੀ ਖੇਡਣਾ ਚਾਹੀਦਾ ਹੈ ਅਤੇ ਇਸ ਤਰ੍ਹਾਂ ਉਸ ਨੂੰ ਬਾਲ ਦੀ ਪਿੱਚ ਤੋਂ ਬਾਅਦ ਜਾਂਚ ਕਰਨ ਦਾ ਸਮਾਂ ਵੀ ਮਿਲੇਗਾ | ਹੌਲੀ ਬਾਲ ਅਤੇ ਵਧੇਰੇ ਮੁਸ਼ਕਿਲ ਵਿਕਟ ਵਿਚ ਉਸ ਨੂੰ ਜ਼ਰੂਰ ਹੀ ਬੈਕ ਸਟਰੋਕ ਉੱਤੇ ਨਿਰਭਰ ਕਰਨਾ ਚਾਹੀਦਾ ਹੈ ।

ਸੱਜਾ ਪੈਰ ਕਰੀਜ਼ ਵੱਲ ਪੰਜਾ ਸਮਾਨਅੰਤਰ ਰਹਿੰਦਿਆਂ ਬਾਲ ਦੀ ਰੇਖਾ ਦੇ ਅੰਦਰ ਅਤੇ ਪਿੱਛੇ ਵੱਲ ਚੰਗੀ ਤਰ੍ਹਾਂ ਹਿਲਜੁਲ ਕਰ ਸਕਦਾ ਹੈ | ਬਦਨ ਦਾ ਭਾਰ ਇਸ ਪੈਰ ਉੱਤੇ ਬਦਲੀ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ, ਪਰ ਸਿਰ ਅੱਗੇ ਵੱਲ ਥੋੜਾ ਝੁਕਿਆ ਹੋਣਾ ਚਾਹੀਦਾ ਹੈ । ਖੱਬਾ ਪੈਰ ਪੰਜੇ ਪਰਨੇ ਹੁੰਦਿਆਂ ਹੋਇਆਂ ਇਕ ਸੰਤੁਲਨਕਾਰ ਵਜੋਂ ਕੰਮ ਕਰਦਾ ਹੈ ।

ਬਾਲ ਨਜ਼ਰਾਂ ਤੋਂ ਥੋੜ੍ਹਾ ਜਿਹਾ ਹੇਠਾਂ ਮਿਲਣਾ ਚਾਹੀਦਾ ਹੈ, ਜਿਹੜਾ ਕਿ ਜਿੰਨਾ ਸੰਭਵ ਪੱਧਰ ਹੋ ਸਕੇ ਹੋਣਾ ਚਾਹੀਦਾ ਹੈ, ਕਿਉਂਕਿ ਉਹ ਬਾਲ ਨੂੰ ਹੇਠਾਂ ਪਿੱਚ ਵੱਲ ਤੱਕਦੀਆਂ ਹਨ । ਹਿੱਟ ਉੱਤੇ ਕੰਟਰੋਲ ਖੱਬੇ ਹੱਥ ਤੇ ਬਾਂਹ ਵਲੋਂ ਕੂਹਣੀ ਉੱਪਰ ਚੁੱਕ ਕੇ ਕੀਤਾ ਜਾਂਦਾ ਹੈ । ਸੱਜਾ ਹੱਥ ਅੰਗੂਠੇ ਤੇ ਉਂਗਲਾਂ ਦੀ ਪਕੜ ਵਿਚ ਅਰਾਮਦਾਇਕ ਹੁੰਦਾ ਹੈ । ਬਦਨ ਨੂੰ ਜਿੰਨਾ ਸੰਭਵ ਹੋ ਸਕੇ ਪਾਸਿਆਂ ਵੱਲ ਰੱਖਣਾ ਚਾਹੀਦਾ ਹੈ ।
ਸਮਤਲ ਬੈਕ ਸਟਰੋਕ
ਇਕ ਲੜਕਾ ਜਦ ਤਕ ਸਿੱਧੀ ਹਿੱਟ ਮਾਰਨੀ, ਨਹੀਂ ਸਿੱਖਦਾ, ਤਦ ਤਕ ਬੈਟਸਮੈਨ ਨਹੀਂ ਬਣਦਾ, ਪਰ ਉਸ ਨੂੰ ਮਾੜੇ ਭਾਵ ਗਲਤ ਬਾਲ ਨਾਲ ਖੇਡਣ ਦੀ ਜਾਂਚ ਵੀ ਹੋਣੀ ਚਾਹੀਦੀ ਹੈ ਅਤੇ ਉਹ ਗੱਲ ਕਰਾਸ-ਬੈਟ ਹਿੱਟਾਂ ਰਾਹੀਂ ਅਕਸਰ ਵਧੇਰੇ ਅਸਰਦਾਰ ਹੋ ਸਕਦੀ ਹੈ । ਇਹ ਗੱਲ ਵਿਸ਼ੇਸ਼ ਕਰਕੇ ਲੰਬੇ ਟੱਪਿਆਂ ਅਤੇ ਪੂਰਨ ਉਛਾਲ ਵਿਚ ਸੱਚੀ ਲੱਗਦੀ ਹੈ ਅਤੇ | ਖ਼ਾਸ ਕਰਕੇ ਜੂਨੀਅਰ ਵਿਕਟ ਵਿਚ ਚੌਕੇ ਮਾਰਨ ਦੇ ਉੱਤਮ ਮੌਕੇ ਪ੍ਰਦਾਨ ਕਰਦੀ ਹੈ । ਇਹ ਹਿੱਟਾਂ ਵਧੇਰੇ ਆਸਾਨ ਹੁੰਦੀਆਂ ਹਨ, ਕਿਉਂਕਿ ਇਹ ਸਿੱਧੀਆਂ ਬੈਟ ਹਿੱਟਾਂ ਨਾਲੋਂ ਵਧੇਰੇ ਕੁਦਰਤੀ ਹੁੰਦੀਆਂ ਹਨ, ਪਰ ਇਨ੍ਹਾਂ ਨੂੰ ਦ੍ਰਿੜ੍ਹਤਾ ਨਾਲ ਖੇਡਣ ਵਾਸਤੇ ਤੁਹਾਨੂੰ ਦਰੁਸਤੀ ਨਾਲ ਖੇਡਣ ਦੀ ਜਾਂਚ ਸਿੱਖਣੀ ਚਾਹੀਦੀ ਹੈ ।
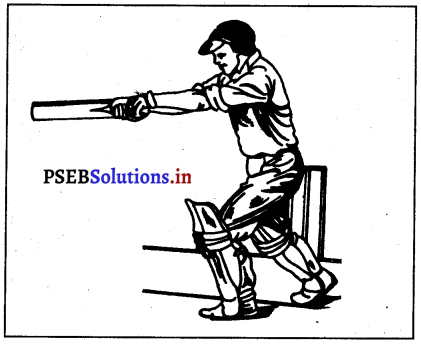
ਪਿਛਲੇ ਪੈਰ ਦਾ ਸੁਏਰ ਕੱਟ
ਬਾਲ ਰੇਖਾ ਅਤੇ ਪੁਆਇੰਟ ਉੱਤੇ ਸਾਹਮਣੇ ਤੋਂ ਜਾਂ ਪਿੱਛੇ ਮਿਲਦੇ ਬਾਲ ਨਾਲ ਨਿਪਟਣ ਲਈ ਸੱਜਾ ਪੈਰ ਕੂਲ਼ੇ ਦੀ ਰੇਖਾ ਦੇ ਆਰ-ਪਾਰ ਘੁੰਮਦਾ ਹੈ । ਫਿਰ ਗੁਟ ਅਤੇ ਹੱਥਾਂ ਨੂੰ ਇਕ ਉੱਚੇ ਬੈਟ ਲਿਫ਼ਟ ਤੋਂ ਹੇਠਾਂ ਮੋੜਿਆ ਜਾਂਦਾ ਹੈ ਅਤੇ ਸਿਰ ਦੇ ਬਦਨ, ਝੁਕੇ ਹੋਏ ਸੱਜੇ ਗੋਡੇ ਤੇ ਸਟਰੋਕ ਦੀ ਰੇਖਾ ਵਿਚ ਘੁੰਮਦਾ ਹੈ ।

ਲੇਟ ਕੱਟ
ਇਹ ਹਿੱਟ ਵੀ ਉੱਪਰ ਵਾਲੀ ਹਿੱਟ ਵਰਗੀ ਹੀ ਹੈ, ਸਿਵਾਏ ਇਸ ਦੇ ਕਿ ਇਹ ਖੱਬੇ ਮੋਢੇ ਦੇ ਵਧੇਰੇ ਮੋੜ ਨਾਲ ਸ਼ੁਰੂ ਹੁੰਦੀ ਹੈ ਅਤੇ ਸੱਜਾ ਪੈਰ ਥਰਡ ਸਲਿਪ ਵੱਲ ਪੰਜੇ ਦੇ ਰੁਖ ਨਾਲ ਧਰਤੀ ਉੱਤੇ ਹੁੰਦਾ ਹੈ | ਬਾਲ ਵਿਕਟਾਂ ਦੀ ਸਤਹ ਦੇ ਬਰਾਬਰ ਮਿਲਦਾ ਹੈ ਅਤੇ ਗੁੱਟ ਅੱਗੇ ਵਧਾਉਂਦਿਆਂ ਬੈਟਸਮੈਨ ਇਸ ਨੂੰ ਗਲੀ ਜਾਂ ਸੈਕਿੰਡ ਸਲਿਪ ਦੀ ਦਿਸ਼ਾ ਵਿਚ ਹਿੱਟ ਕਰਦਾ ਹੈ । ਇਨ੍ਹਾਂ ਦੋਹਾਂ ਕੱਟਾਂ ਵਿਚ ਖੱਬਾ ਪੈਰ ਪੰਜੇ ਉੱਤੇ ਆਰਾਮ ਦੀ ਹਾਲਤ ਵਿਚ ਰਹਿੰਦਾ ਹੈ ਅਤੇ ਭਾਰ ਝੁਕੇ ਹੋਏ ਸੱਜੇ ਗੋਡੇ , ਉੱਤੇ ਪੂਰੀ ਤਰ੍ਹਾਂ ਰਹਿੰਦਾ ਹੈ ।
ਸਪਰੋਟਸ ਅਵਾਰਡ (Sports Award)
ਅਰਜੁਨ ਪੁਰਸਕਾਰ ਜੇਤੂਆਂ ਦੀ ਸੂਚੀ (List of Arjuna Award Winners)-ਸਲੀਮ ਦੁਰਾਨੀ (1961), ਮਨਸੂਰ ਅਲੀ ਖ਼ਾਨ ਪਟੌਦੀ (1964), ਵਿਜੈ ਮਾਂਜਰੇਕਰ (1965), ਚੰਦਰਕਾਂਤ ਜੀ, ਬੋਰਡੇ(1966), ਅਜੀਤ ਵਾਡੇਕਰ (1967), ਈ.ਏ.ਐਸ. ਨਾ (1968), ਬਿਸ਼ਨ ਸਿੰਘ ਬੇਦੀ (1969), ਡੀ. ਐੱਨ. ਸਰਦੇਸਾਈ (1970), ਐੱਸ. ਵੈੱਕਟਰਾਘਵਨ (1971), ਏਕਨਾਥ ਸੈਲਕਰ (1972), ਬੀ.ਐੱਸ. ਚੰਦਰਸ਼ੇਖਰ (1973), ਅੰਜਨ ਭੱਟਾਚਾਰਜੀ ਡੀਫ ਐਂਡ ਡੈਮ) (1974), ਸੁਨੀਲ ਗਵਾਸਕਰ (1975), ਸ਼ਾਂਤਾ ਰੰਗਸੁਆਮੀ (1976), ਜੀ.ਆਰ. ਵਿਸ਼ਵਨਾਥ (1977-78), ਕਪਿਲ ਦੇਵ ਨਿਖੰਜ (1979-80), ਸੀ.ਪੀ.ਐੱਸ. ਚੌਹਾਨ (1980-81), ਸੈਯਦ ਐੱਮ.ਐੱਚ. ਕਿਰਮਾਨੀ (1980-81), ਦਲੀਪ ਵੈਂਗਸਰਕਰ (1981), ਮੋਹਿੰਦਰ ਅਮਰਨਾਥ (1982), ਡਾਇਨਾ ਇਡੁਲਜੀ (1983), ਰਵੀ ਸ਼ਾਸਤਰੀ (1984), ਐੱਸ. ਡੀ. ਕੁਲਕਰਨੀ (1985), ਮੁਹੰਮਦ ਅਜ਼ਹਰੂਦੀਨ, ਸੰਧਿਆ ਅਗਰਵਾਲ (1986), ਮਦਨ ਲਾਲ (1989), ਮਨੋਜ ਪ੍ਰਭਾਕਰ (1993), ਕਿਰਨ ਮੋਰੇ (1993), ਸਚਿਨ ਤੇਂਦੁਲਕਰ (1994), ਅਨਿਲ ਕੁੰਬਲੇ (1995), ਜਵਾਗਲ ਨਾਥ (1996),ਰਾਹੂਲ ਵਿਡ,ਨਯਨ ਮੋਗਿਆ (1999), ਵੈਂਕਟੇਸ਼ ਪ੍ਰਸ਼ਾਦ (2000), ਵੀ.ਵੀ.ਐੱਸ. ਲਕਸ਼ਮਣ (2002), ਵਰਿੰਦਰ ਸਹਿਵਾਗ (2003), ਹਰਭਜਨ ਸਿੰਘ (2004), ਅੰਜੂ ਜੈਨ (2006), ਗੌਤਮ ਗੰਭੀਰ(2009), ਹਰਭਜਨ ਸਿੰਘ ਅਤੇ ਜ਼ਹੀਰ ਖ਼ਾਨ (2010) । ਦਰੋਣਾਚਾਰੀਆ ਅਵਾਰਡ-ਡੀ.ਪੀ. ਆਜ਼ਾਦ, ਗੁਰਚਰਨ ਸਿੰਘ, ਆਰ. ਆਚਰੇਕਰ, ਸੁਨੀਤਾ ਸ਼ਰਮਾ (2005), ਸਚਿਨ ਤੇਂਦੁਲਕਰ ।
PSEB 12th Class Physical Education Practical ਕ੍ਰਿਕੇਟ (Cricket)
ਪ੍ਰਸ਼ਨ 1.
ਕ੍ਰਿਕਟ ਖੇਡ ਵਿਚ ਕੁੱਲ ਕਿੰਨੇ ਖਿਡਾਰੀ ਹੁੰਦੇ ਹਨ ?
ਉੱਤਰ:
11.
ਪ੍ਰਸ਼ਨ 2.
ਵਿਕਟ ਦੀ ਚੌੜਾਈ ਕਿੰਨੀ ਹੁੰਦੀ ਹੈ ?
ਉੱਤਰ:
9 (22.9 ਸੈਂਟੀ ਮੀਟਰ)
ਪ੍ਰਸ਼ਨ 3.
ਕ੍ਰਿਕਟ ਗੇਂਦ ਦਾ ਵਜ਼ਨ ਕਿੰਨਾ ਹੁੰਦਾ ਹੈ ?
ਉੱਤਰ:
155.9 ਗਰਾਮ ਤੋਂ 163 ਗਰਾਮ ਤੱਕ ।
ਪ੍ਰਸ਼ਨ 4.
ਪਹਿਲੇ ਕ੍ਰਿਕਟ ਕਲੱਬ ਦਾ ਕੀ ਨਾਮ ਸੀ ?
ਉੱਤਰ:
ਹੈਬਲਡਨ ।
ਪ੍ਰਸ਼ਨ 5.
ਭਾਰਤ ਵਿਚ ਪਹਿਲਾ ਵਨ-ਡੇ ਮੈਚ ਕਦੋਂ ਖੇਡਿਆ ਗਿਆ ?
ਉੱਤਰ:
5 ਜਨਵਰੀ, 1971.

ਪ੍ਰਸ਼ਨ 6.
ਐੱਲ. ਬੀ. ਡਬਲਯੂ. (LBW) ਦਾ ਪੂਰਾ ਨਾਂ ਕੀ ਹੈ ?
ਉੱਤਰ:
ਲੈਗ ਬੀਫੇਅਰ ਵਿਕਟ (Leg before wicket)
ਪ੍ਰਸ਼ਨ 7.
ਕਿਸੇ ਚਾਰ ਕ੍ਰਿਕਟ ਸਟਰੋਕ ਦੇ ਨਾਮ ਦੱਸੋ ।
ਉੱਤਰ:
- ਆਨ ਡਾਈਵ
- ਬੈਕ ਸਟਰੋਕ
- ਸਮਤਲ ਬੈਕ ਸਟਰੋਕ
- ਲੇਟ ਕੱਟ ।
ਪ੍ਰਸ਼ਨ 8.
ਕ੍ਰਿਕਟ ਵਿਚ ਕਿੰਨੇ ਅੰਪਾਇਰ ਹੁੰਦੇ ਹਨ ?
ਉੱਤਰ:
3.
ਪ੍ਰਸ਼ਨ 9.
ਕ੍ਰਿਕਟ ਪਿੱਚ ਅਤੇ ਵਿਕਟ ਵਿਚਕਾਰ ਕਿੰਨੀ ਲੰਬਾਈ ਹੁੰਦੀ ਹੈ ?
ਉੱਤਰ:
22 ਗਜ਼ (20.12 ਮੀਟਰ)
ਪ੍ਰਸ਼ਨ 10.
ਪਹਿਲਾ ਟੈਸਟ ਮੈਚ ਕਦੋਂ ਖੇਡਿਆ ਗਿਆ ?
ਉੱਤਰ:
1877 ਵਿਚ ਅਸਟ੍ਰੇਲੀਆ ਅਤੇ ਇੰਗਲੈਂਡ ਵਿਚਕਾਰ)
ਪ੍ਰਸ਼ਨ 11.
ਕਿਸ ਦੀ ਕਪਤਾਨੀ ਵਿਚ ਭਾਰਤ ਨੂੰ ਪਹਿਲਾ ਵਰਲਡ ਕੱਪ ਮਿਲਿਆ ਸੀ ?
ਉੱਤਰ:
ਕਪਿਲ ਦੇਵ (1983 ਵਿਚ)
ਪ੍ਰਸ਼ਨ 12.
ਕ੍ਰਿਕਟ ਵਿਚ ਕਿੰਨੇ ਪ੍ਰਕਾਰ ਦੇ ਮੈਚ ਹੁੰਦੇ ਹਨ ?
ਉੱਤਰ:
ਇਕ ਦਿਨ ਦਾ ਮੈਚ, ਟੈਸਟ ਮੈਚ, 20-20 ਕੱਪ |
ਪ੍ਰਸ਼ਨ 13.
ਬਾਊਲਿੰਗ ਕੀਜ਼ ਦੀ ਲੰਬਾਈ ਕਿੰਨੀ ਹੁੰਦੀ ਹੈ ?
ਉੱਤਰ:
8′ 8″ (2.64 ਮੀਟਰ)
ਪ੍ਰਸ਼ਨ 14.
ਛੋਟੇ ਸਰਕਲ ਦਾ ਖੇਤਰ ਕਿੰਨਾ ਹੁੰਦਾ ਹੈ ?
ਉੱਤਰ:
22.4 ਮੀਟਰ ।
ਪ੍ਰਸ਼ਨ 15.
ਮੈਦਾਨ ਤੋਂ ਵਿਕਟ ਦੀ ਉਚਾਈ ਕਿੰਨੀ ਹੁੰਦੀ ਹੈ ?
ਉੱਤਰ:
28’’ (71 ਸੈਂ.ਮੀ.)।

![]()


![]()
![]()
![]()
![]()
![]()
















 ]
]
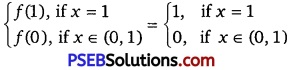 gof(x) = g(f(x))= g(1) [∵ x > 0]
gof(x) = g(f(x))= g(1) [∵ x > 0]